Krypton difluorid
| Krypton difluorid | ||

| ||
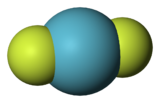 | ||
| Struktura difluoridu kryptonu | ||
| Identifikace | ||
|---|---|---|
| N O CAS | ||
| ÚSMĚVY |
[Kr] (F) F , |
|
| InChI |
InChI: InChI = 1 / F2Kr / c1-3-2 |
|
| Chemické vlastnosti | ||
| Hrubý vzorec | KrF 2 | |
| Molární hmotnost | 121 795 ± 0,002 g / mol F 31,2%, Kr 68,8%, |
|
| Fyzikální vlastnosti | ||
| Objemová hmotnost | 3240 kg · m -3 až 15 ° C | |
| Jednotky SI a STP, pokud není uvedeno jinak. | ||
Kryptonu difluorid vzorce Krf 2, je první kryptonová sloučenina, která má být identifikována. Je to bezbarvá těkavá pevná látka, jejíž molekula má lineární strukturu F-Kr-F s 188,9 µm vazbami . Vytváří soli kationů KrF+ a Kr 2 F 3+ se silnými Lewisovými kyselinami .
Krypton difluorid je silné fluorační činidlo, které je schopné přeměňovat xenon a jod, respektive xenon hexafluorid a pentafluorid jod :
Xe+ 3 KrF 2→ XeF 6 + 3 kr I 2+ 5 KrF 2→ 2 POKUD 5 + 5 krKationt KrF+ je také jediným známým činidlem schopným dostat zlato do oxidačního stavu +5:
8 KrF 2 + 2 k → 2 KrF+ AuF 6- + 6 kr+ F 2 KrF+ AuF 6- → AuF 5 + Kr+ F 2při teplotě nad 60 ° CPoznámky a odkazy
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- AV Grosse, AD Kirschenbaum, AG Streng, LV Streng, „Krypton Tetrafluoride: Preparation and Some Properties“, Science, 1963, svazek 139, strany 1047-1048, DOI : 10.1126 / science.139.3559.1047
- JF Lehmann, DA Dixon, GJ Schrobilgen, „Rentgenové krystalové struktury α-KrF 2, [KrF] [MF 6 ](M = Co, Sb, Bi), [Kr 2 F 3 ] [SbF 6 ] • Krf 2, [Kr 2 F 3 ] 2 [SbF 6 ] 2 • KrF 2, a [Kr 2 F 3 ] [AsF 6 ] • [KrF] [AsF 6 ]; Syntéza a charakterizace [Kr 2 F 3 ] [PF 6 ] • nKrF 2; a teoretická studia KrF 2, KrF+ , Kr 2 F 3+ a [KrF] [MF 6 ](M = P, As, Sb, Bi) Ion Pairs ", Anorganic Chemistry 2001, svazek 40, strany 3002-3017, DOI : 10,1021 / ic001167w