Chlorid zirkoničitý
| Chlorid zirkoničitý | |||
| |||
|
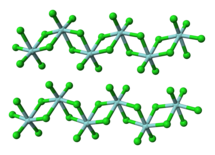
__ Zr 4+ __ Cl - struktura chloridu zirkoničitého |
|||
| Identifikace | |||
|---|---|---|---|
| N O CAS | |||
| Ne o ECHA | 100.030.041 | ||
| Ne o EC | 233-058-2 | ||
| N O RTECS | ZH7175000 | ||
| PubChem | 24817 | ||
| ÚSMĚVY |
Cl [Zr] (Cl) (Cl) Cl , |
||
| InChI |
Std. InChI: InChI = 1S / 4ClH.Zr / h4 * 1H; / q ;;;; + 4 / p-4 Std. InChIKey: DUNKXUFBGCUVQW-UHFFFAOYSA-J |
||
| Chemické vlastnosti | |||
| Hrubý vzorec | ZrCl 4 | ||
| Molární hmotnost | 233,036 ± 0,01 g / mol Cl 60,85%, Zr 39,15%, |
||
| Fyzikální vlastnosti | |||
| T. fúze | 437 ° C | ||
| Objemová hmotnost | 2,8 g · cm -3 až 15 ° C | ||
| Opatření | |||
| SGH | |||
  Nebezpečí H302, H314, EUH014, P280, P301 + P330 + P331, P305 + P351 + P338, P309 + P310, H302 : Zdraví škodlivý při požití H314 : Způsobuje těžké poleptání kůže a poškození očí EUH014 : Prudce reaguje s vodou P280 : Noste ochranné rukavice / ochranný oděv / ochranné brýle / na obličej. P301 + P330 + P331 : Při požití: vypláchněte ústa. Nevyvolávejte zvracení. P305 + P351 + P338 : Při zasažení očí: Několik minut opatrně vyplachujte vodou. Vyjměte kontaktní čočky, pokud je oběť nosí a lze je snadno vyjmout. Pokračujte v oplachování. P309 + P311 : Při expozici nebo necítíte-li se dobře: okamžitě volejte TOXIKOLOGICKÉ INFORMAČNÍ STŘEDISKO nebo lékaře. |
|||
| NFPA 704 | |||
| 0 3 1 Ž | |||
| Doprava | |||
80 : korozivní materiál nebo materiál vykazující menší stupeň korozivity UN číslo : 2503 : ZIRCONIUM TETRACHLORIDE Třída: 8 Štítek: 8 : Žíravé látky Balení: Obalová skupina III : látky s nízkým nebezpečím.  |
|||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||
Chlorid zirkonu ( IV ), nebo chlorid zirkoničitý , je chemická sloučenina podle vzorce ZrCl 4. Zdá se, ve formě bílého prášku, který prudce reaguje s vodou a s' hydrolýzou rychle v otevřeném prostoru, dávat oktahydrát z zirkonylchloridu ZrOCl 2 · 8H 2 O. Na rozdíl od chloridu titaničitého TiCl 4, ZrCl 4pevné přijímá polymerní struktura , ve které každý Zr 4+ kation znamená octahedral koordinovány v pruhované nebo vrstvené struktury podobné tomu hafnia chlorid HfCl 4. Tato struktura je snadno degradován Lewisovy báze , které se štěpí na vazby Zr-Cl-Zr .
Zirkonium ( IV ) chlorid je důležitá sloučenina použitá v zirkonia chemii . Je možno získat chlorací z oxidu zirkoničitého ZrO 2,. Ten se potom zpracuje s koksem v elektrické obloukové peci , čímž se získá zirkonia karbonitridů, který se pak nechá reagovat s chlorem Cl 2 za vzniku chloridu zirkoničitého:
ZrO 2+ 2 C + 2 Cl 2⟶ ZrCl 4+ 2 CO při teplotě 900 ° C .Zirkoničitý může být také chlorované při 650 ° C s chlorem nebo při 500 ° C, s olova (II) chloridu PbCl 2 :
Zr + 2 Cl 2⟶ ZrCl 4na 650 ° C . Zr + 2 PbCl 2⟶ ZrCl 4+ 2 Pb při teplotě 500 ° C .Další syntetická cesta reaguje oxid zirkoničitý s tetrachlormethanem CCl 4v proudu dusíku mezi 450 a 500 ° C :
ZrO 2+ 2 CCl 4⟶ ZrCl 4+ 2 COCI 2z 450 , aby 500 ° C .Zirkonium ( IV ) chlorid je meziprodukt při konverzi zirkonia rud (zejména oxidy ) do kovového zirkonia v procesu Kroll . To je také prekurzorem nejběžnější pro ukládání chemických par z oxidu zirkoničitého ZrO 2nebo zirkoniumdiborid ZrB 2. V organické syntéze se používá jako slabá Lewisova kyselina pro Friedel-Craftsovu reakci , Diels-Alderovu reakci a intramolekulární cyklizační reakce . Je také výchozím bodem pro syntézu mnoha organokovových komplexů zirkonia. Obvykle se převádí na molekulární komplex, takže jej lze použít navzdory své polymerní povaze. S tetrahydrofuranem tvoří pevný komplex 1: 2, který taje při teplotě asi 175 - 177 ° C ( CAS č. ). Cyklopentadienid sodný NAC 5 H 5 reaguje s tímto ZrCl 4 (THF) 2 komplexčímž se získá zirkonocendichloridu ZrCl 2 (C 5 H 5 ) 2, použitý v mnoha reakcích.
Poznámky a odkazy
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- " zirkonium (IV) chlorid sloučenina list , reaktor stupně, více než 99,5% (kovy základ) " , na Alfa Aesar (zobrazena 14. srpna 2020 ) .
- Záznam „Zirkonium (IV) chlorid“ v chemické databázi GESTIS IFA (německý orgán odpovědný za bezpečnost a ochranu zdraví při práci) ( německy , anglicky ), přístup k 14. srpnu 2020 (je nutný JavaScript)
- (v) NN Greenwood a A. Earnshaw, Chemistry of prvků , 2 th ed. , Butterworth-Heinemann, 1997 ( ISBN 978-0-7506-3365-9 )
- (de) Georg Brauer, ve spolupráci s Marianne Baudler, Handbuch der Chemie Präparativen anorganischen , 3 e ed. přepracované, sv. II, Ferdinand Enke, Stuttgart, 1978, str. 1358 . ( ISBN 3-432-87813-3 )
- (en) WS Hummers et al. „Zirconium and hafnium tetrachlorides“, JC Bailar Jr., Anorganic Syntheses , sv. 4, McGraw-Hill, 1953, str. 121-126 .
- (in) E. Randich , „ chemická pára Usazené boridy formy (Ti, Zr) B 2 a (Ta, Ti) B 2 ” , Thin Solid Films , roč. 63, n O 2Listopad 1979, str. 309-313 ( DOI 10.1016 / 0040-6090 (79) 90034-8 , Bibcode 1979TSF .... 63..309R , číst online )
- (in) Utpal Bora , „ Zirconium Tetrachloride “ , Synlett , roč. 7, 2003, str. 1073-1074 ( DOI 10.1055 / s-2003-39323 , číst online )
- (in) Ilan Marek, Nové aspekty zirkonia obsahujícího organické sloučeniny. Topics in Organometallic Chemistry , 10, Springer, 2005. ( ISBN 978-3-540-22221-7 )
- Sigma-Aldrich list ze sloučeniny zirkonium (IV) chlorid tetrahydrofuranového komplexu (1: 2) 99% , konzultovat 14. srpna 2020.
- (in) THE Manzer Joe Deaton, „Tetrahydrofuran Complex of Selected Early Transition Metals“ Anorganické syntézy , 21, 1985, s. 135-140 . ( ISBN 978-0-470-13252-4 )
- (in) G. Wilkinson a JM Birmingham , „ Bis-cyklopentadienylové sloučeniny Ti, Zr, V, Nb a Ta “ , Journal of the American Chemical Society , sv. 76, n o 17, Září 1954, str. 4281-4284 ( DOI 10.1021 / ja01646a008 , číst online )
