Chlór
| Chlór | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chlor v ampuli. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Název IUPAC | chlór | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o ECHA | 100 029 053 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o EC | 231-959-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O E | E925 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | zelenožlutý plyn, štiplavý zápach | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hrubý vzorec |
Cl 2 [izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární hmotnost | 70,906 ± 0,004 g / mol Cl 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T. fúze | -101 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° vroucí | -34,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpustnost |
14,6 g · l -1 ve vodě při 0 ° C , 7,3 g · l -1 při 20 ° C , 5,7 g · l -1 při 30 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
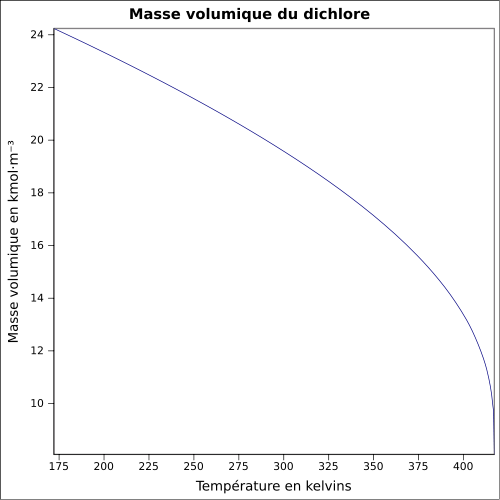
| Objemová hmotnost | 2,48 (hustota vzhledem ke vzduchu) při 20 ° C , 6,864 atm : 1,4085 g · cm -3 (liq.) Při -35 ° C , 0,9949 atm : 1,5649 g · cm - 3 (liq.) rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak nasycených par |
6,766 bar při 20 ° C 8,8 bar při 30 ° C 14,3 bar při 50 ° C rovnice:
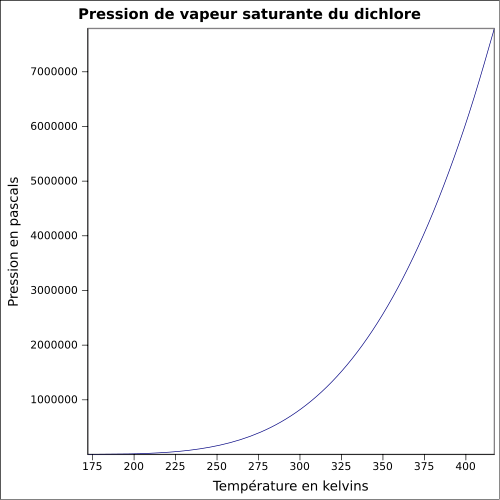
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritický bod |
143,81 ° C 79,914 bar 0,57688 kg · s -1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trojitý bod |
-100,98 ° C 0,01387 bar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 206 m · s -1 ( 0 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° |
20,41 kJ · mol -1 ( 1 atm , -34,04 ° C ); 17,65 kJ · mol -1 ( 1 atm , 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C str |
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionizační energie | 11,480 ± 0,005 eV (plyn) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pearsonův symbol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Křišťálová třída nebo vesmírná skupina | CMCA ( n o 64) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Strukturbericht | A14 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Typická struktura | I 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opatření | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    Nebezpečí H270, H315, H319, H331, H335, H400, H270 : Může způsobit nebo zesílit požár; oxidant H315 : Způsobuje podráždění kůže H319 : Způsobuje vážné podráždění očí H331 : Toxický při vdechování H335 : Může způsobit podráždění dýchacích cest H400 : Vysoce toxický pro vodní organismy |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, D1A, E, A : Absolutní tlak par stlačeného plynu při 50 ° C = 750 kPa D1A : Vysoce toxický materiál s vážnými okamžitými účinky Přeprava nebezpečných věcí: třída 2.3 E : Žíravina Přeprava nebezpečných věcí: třída 8 Zveřejnění 1,0% podle údajů o složce seznam komentářů: jak je uvedeno ve výkladu zdravotní politiky v Kanadě, symbol nebezpečí D1 (lebka) nemusí být uveden na štítku dodavatele. Všechna nebezpečí pro zdraví a bezpečnost, která tento výrobek představuje, však musí být uvedena na štítku a v bezpečnostním listu. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 4 0 VŮL | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doprava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
265 : jedovatý a oxidační plyn (podporuje požár) UN číslo : 1017 : CHLOR Třída: 2.3 Klasifikační kód: 2 TOC : Zkapalněný plyn, toxický, oxidující, korozivní. Štítky: 2.3 : Toxické plyny (odpovídá skupinám označeným velkým T, tj. T, TF, TC, TO, TFC a TOC). 5.1 : Oxidační látky 8 : Žíravé látky    |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalace | dusivý zápach | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoxikologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CL 50 | 1 hodina: krysa 293 ppm myš 137 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prahová hodnota zápachu | nízká: 0,02 ppm vysoká: 3,4 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Chlór ( Cl 2 ) je plyn žlutozelená v standardních podmínek teploty a tlaku ( chloros prostřednictvím „zelených“ v Řekovi ). Je 2,5krát hustší než vzduch . Má velmi nepříjemný dusivý zápach a je extrémně toxický, protože se rekombinuje s vlhkostí ve sliznicích a plicích za vzniku kyselin, které napadají tkáně.
Chlór objevil Carl Wilhelm Scheele v roce 1774 . To bylo používáno v první světové válce jako bojový plyn , bertholit .
Chlor je rozpustný ve vodě za vzniku chlórové vody , ale není rozpustný ve slané vodě.
Molekula chloru je vytvořen ze dvou atomů z chloru .
Výroba
Chlór lze snadno vyrobit elektrolýzou roztoku chloridu sodného ( chloralkali proces ):
2Na + + 2C - + 2 H 2 O→ 2NaOH + Cl 2 + H 2Scheele to syntetizoval reakcí oxidu manganičitého (MnO 2 ) s kyselinou chlorovodíkovou (HCl).
Může být také vyroben v malých množstvích reakcí kyseliny chlorovodíkové s manganistanem draselným .
Navíc, když je kyselina nalita do bělidla , je pozorováno uvolňování chloru (ale v přítomnosti močoviny přítomné v moči uvolňuje trichloramin (NCI 3 ); velmi dráždivý plyn). Chlormetrický stupeň bělícího roztoku je objem chloru uvolněného jedním litrem tohoto roztoku (přebytek kyseliny).
Cl - > + ClO - + 2H + → Cl 2 + H 2 Opoužití
Chlor se používá jako surovina k výrobě kyseliny chlorovodíkové reakcí mezi chlorem a dihydrogenem .
Cl 2 + H 2 → 2HClPoužívá se také k výrobě polyvinylchloridu (PVC).
Používá se při výrobě produktů s vazbou uhlík-chlor, jako je chladivo R12 dichlorodifluormethan .
Slouží také k desinfekci na pitnou vodu místo bělidla .
Byl používán jako bojový plyn (protože dráždí horní dýchací cesty a je toxický) během první světové války, kdy zanechal pět tisíc mrtvých a patnáct tisíc přeživších, a ve většině případů zanechal oběti celoživotní následky. .
Vlastnosti
Chlor má tu vlastnost, že mění barvu roztoku indiga a několika dalších organických látek. Barva mnoha organických barviv pochází z rozdílů mezi mnoha energetickými hladinami jejich konjugovaných vazeb . Chlór však oxiduje dvojné vazby uhlík-uhlík, které tvoří systémy konjugovaných vazeb.
Reference
- CHLOR , bezpečnostní list (y) Mezinárodního programu pro bezpečnost chemických látek , konzultován 9. května 2009
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (en) Robert H. Perry a Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- (in) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , Vázaná kniha ( ISBN 978-1-4200-9084-0 )
- (in) David R. Lide, Příručka chemie a fyziky , Boca Raton, CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205
- „ The Molecular Iodine (I2) Crystal Structure (A14) “ , na adrese http://cst-www.nrl.navy.mil/ (zpřístupněno 17. prosince 2009 )
- Indexové číslo v tabulce 3.1 přílohy VI nařízení ES n o 1272/2008 (16. prosince 2008)
- „ Chlor “ v databázi chemických produktů Reptox z CSST (quebecká organizace odpovědná za bezpečnost a ochranu zdraví při práci), přístup k 25. dubnu 2009
- „ Chlor “ na adrese hazmap.nlm.nih.gov (přístup 14. listopadu 2009 )
- „ Soubor: Bleach - Vodný roztok chlornanu sodného “ [PDF] , Národní komora bělidla, květen 2010, str. 8 , § 7: Bezpečnost pro člověka, na eaudejavel.fr
- „ Individuální a skupinové vystavení parám chlóru “, Belgické toxikologické centrum
- „ Plyn: 22. dubna 1915 v Ypres (Belgie) “ , o Velké válce
- Chemie, povinný terminál S, program 2002 , Nathan, kol. "Sírius",2008, 351 s. ( ISBN 978-2-09-172496-6 ) , str. 248