Dehydratační reakce
V chemii, je dehydratační reakce je chemická reakce , ve které se výchozí činidlo ztrácí atom vodíku a hydroxylovou skupinu , nebo molekulu vody , na zadní stranu hydratační reakce . Dehydratační reakce jsou podkategorií eliminačních reakcí .
Vzhledem k tomu, hydroxylová skupina (-OH), je špatná odstupující skupina , která má Bronstedovy kyseliny jako katalyzátoru podporuje protonace skupiny, převést ji do -OH 2 + , tím lepší odstupující skupinu. Dehydratačními činidly běžně používanými v organické syntéze jsou koncentrovaná kyselina sírová, koncentrovaná kyselina fosforečná , horký oxid hlinitý a horká keramika.
Kondenzační reakce může někdy uvolnit molekulu vody jako produkt. Toto se někdy označuje jako syntéza dehydratací. To je například případ dvou monosacharidů , jako je glukóza nebo fruktóza , které se mohou kondenzovat na disacharid ( sacharózu ) pomocí syntézy dehydratací. Reverzní reakcí je pak hydrolýza , přičemž voda se rekombinuje se dvěma hydroxylovými skupinami, přičemž disacharid se převede na dva monosacharidy.
Příklady
V organické syntéze existuje mnoho příkladů dehydratační reakce, například dehydratace alkoholů nebo cukrů.
| Dehydratační reakce | ||
| Reakce | Rovnice | Příklady |
|---|---|---|
| Přeměna alkoholů na ethery | 2 R-OH → ROR + H 2 O | |
| Konverze alkoholů na alkeny | R-CH 2- CHOH-R → R-CH = CH-R + H 2 O | například přeměna glycerolu na akrolein :
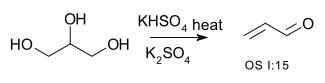 nebo dehydratace 2-methyl-1-cyklohexanolu na (hlavně) 1-methylcyklohexen :  |
| Konverze karboxylových kyselin na anhydridy kyselin | 2 RCOOH → (RCO) 2 O + H 2 O | |
| Konverze amidů na nitrily | RCONH 2 → R-CN + H 2 O | |
| Dienol-benzen přesmyk | 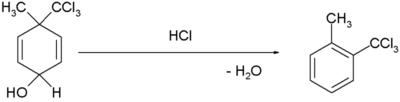 |
|
Poznámky a odkazy
- Organické syntézy OS I: 15 Odkaz
- Dehydratace 2-methyl-1-cyklohexanolu: nové poznatky z populárního vysokoškolského laboratorního experimentu J. Brent Friesen a Robert Schretzman J. Chem. Educ., 2011, 88 (8), str. 1141–1147 DOI : 10.1021 / ed900049b
- H. Plieninger a Gunda Keilich, „ Die Dienol-Benzol-Umlagerung “, Angew. Chem. , sv. 68, n o 19,1956, str. 618–618 ( DOI 10.1002 / angel.19560681914 )
- Margaret Jevnik Gentles, Jane B. Moss, Hershel L. Herzog a EB Hershberg, „ Dienol-benzenové přeskupení. Some Chemistry of 1,4-Androstadiene-3,17-dione “, J. Am. Chem. Soc. , sv. 80, n o 14,1958, str. 3702–3705 ( DOI 10.1021 / ja01547a058 )
- ( fr ) Tento článek je částečně nebo zcela převzat z článku Wikipedie v angličtině s názvem „ Dehydratační reakce “ ( viz seznam autorů ) .