Spektrofotometrie
Spektrofotometrie je pole, které studie měření energie dopravované na elektromagnetické záření v oblasti viditelného světla. Spektrometrie nebo spektroskopie, je kvantitativní a kvalitativní analytická metoda, která zahrnuje měření absorbance nebo optické hustoty chemické látky dané, obvykle v roztoku . Čím je vzorek koncentrovanější, tím více světla absorbuje v mezích proporcionality stanovených zákonem Beer-Lambert .
Optická hustota vzorků se stanoví spektrometrem předem kalibrovaným na vlnovou délku absorpce studované látky.
Zásada
Další podrobnosti najdete v článku Beer-Lambertův zákon .
Když intenzivní světlo prochází roztokem, jeho část je absorbována rozpuštěnými látkami. Intenzita procházejícího světla je proto menší než . Absorbanci roztoku definujeme jako:
.Mluvíme také o propustnosti definované vztahem:
to znamená .Absorbance je kladná hodnota bez jednotky. Čím větší, tím nižší je vysílaná intenzita.
Vztah Beer-Lambert popisuje, že při dané vlnové délce λ je absorbance roztoku úměrná jeho koncentraci a délce optické dráhy (vzdálenosti, kterou světlo prochází roztokem).
Takže u čirého roztoku obsahujícího jedinou absorpční látku:
- je absorbance nebo optická hustota (bez jednotky) roztoku pro vlnovou délku λ;
- (v mol.m −3 ) je koncentrace absorpční látky;
- (v cm) je délka optické dráhy ;
- (v m 3 .mol -1 .cm -1 ) je molární extinkční koeficient absorbující látky v roztoku. Představuje schopnost této látky absorbovat světlo při vlnové délce λ.
Podle zákona Beer-Lamberta je absorbance aditivní (nikoli však propustná). U roztoku obsahujícího několik absorpčních látek je tedy absorbance roztoku součtem jejich absorbance. Pro n absorpčních látek:
.UV viditelný rozsah spektrometrie
Další podrobnosti najdete v článku Spektroskopie
Barevná látka nebo chromofor absorbuje viditelné světlo ( vlnové délky mezi 400 a 800 nm ). Některá řešení absorbují ultrafialové záření (vlnové délky menší než 380 nm ), toto se nazývá UV spektrometrie . Infračervené se nepoužívá ve spektroskopii, protože závisí především na teplotě roztoku a ne jeho koncentraci , nýbrž se vztahuje na infračervenou spektroskopií. Spektrofotometrie je specifičtější než spektroskopie, která pokrývá jiné vlnové délky elektromagnetického spektra .
Spektrometr
Další podrobnosti najdete v článku Spektrometr
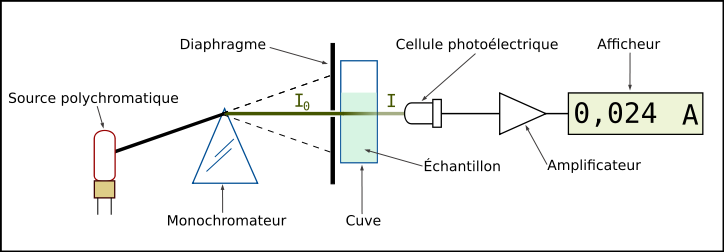 Schéma jednopaprskového UV-viditelného spektrometru
Schéma jednopaprskového UV-viditelného spektrometru
Spektrometr měří absorbance roztoku při dané vlnové délce. Zařízení monochromátoru umožňuje generovat z viditelného nebo ultrafialového zdroje světla monochromatické světlo , jehož vlnovou délku volí uživatel. Dopadající jednobarevné světlo o intenzitě pak prochází nádrží obsahující studovaný roztok a přístroj měří intenzitu procházejícího světla. Hodnota zobrazená spektrofotometrem je absorbance na požadované vlnové délce. Spektrofotometr lze použít k okamžitému měření absorbance při dané vlnové délce nebo k vytvoření absorpčního spektra (skenovací spektrofotometr). V druhém případě monochromátorové zařízení v krátké době popisuje všechny vlnové délky mezi dvěma hodnotami zvolenými operátorem.
Limity
Několik faktorů může degradovat Beer-Lambertův zákon a omezit platnost spektrofotometrie:
- ideální rozsah měření je pro hodnoty T mezi 20 a 60%;
- několik optických aberací spojených s rozptylem , odrazem a difrakcí světla může měření narušit;
- mohou rušit fluorescenční jevy i další chemické zvláštnosti spojené s absorpčními látkami;
- čím větší je hustota rozpuštěné látky, tím více se paprsek dopadajícího světla lome s danou hodnotou. Tato tendence je obvykle malá, ale při vyšších koncentracích se stává výraznější. Refrakce tedy snižuje intenzitu procházejícího světla a přístroj falešně indikuje vyšší absorbanci. Obecně se tomuto jevu lze vyhnout prací s koncentracemi pod 0,01 mol.L −1 .
Důležitost difuzního jevu
Viz.
Jak uvádí zákon Beer-Lambert, síla média blokovat průchod světla je kvantifikována extinkčním koeficientem daným rovnicí:
Tato impedance je generována dvěma odlišnými jevy: absorbance a difúze.
- K rozptylu dochází, když je světlo odkloněno částicemi v médiu tak, že nedosahuje na druhou stranu vzorku.
- Absorbance je proces, při kterém je světelná energie absorbována molekulami ve vzorku, než je uvolněna jako teplo nebo uložena jako chemické vazby.
Takže koeficient předchozí rovnice je složen z koeficientu difúze ( ) a koeficientu absorpce ( ), to znamená:
Koeficient difúze lze vyjádřit součinem koncentrace částic ,, a průřezu z druhé, (za předpokladu, že tyto částice jsou homogenní a rovnoměrně rozděleny v médiu), máme:
Průřez, který je měřítkem podílu světla rozptýleného na částici, je funkcí jejich velikosti. Ve skutečnosti u malých částic (např. Jejich průměr představuje 10% dopadající vlnové délky) převládá Rayleighův rozptyl . Rayleighův rozptyl závisí na délce dráhy, koncentraci rozptylových částic, vlnové délce a jejich polarizaci . Pro ideálně sférickou částici je napsán Rayleighův průřez:
- je průměr částic,
- je vlnová délka,
- je index lomu .
Tato rovnice předpovídá, že krátké vlnové délky budou nejvíce rozptýleny.
U částic větších než je vlnová délka podléhají složitějšímu jevu zvanému Mieův rozptyl . Vzhledem k tomu, že světlo bude rozptýleno v různých úhlech, je v tomto případě nutno v průřezu zohlednit tvar částic. Maximální efektivní část se získá, když se velikost částice blíží dopadající vlnové délce. Rozptyl se s rostoucím rozdílem mezi velikostí částic a vlnovou délkou stále více zmenšuje (to je případ molekulární spektrofotometrie).
Aplikace
Stanovení neznámé koncentraceZnáme absorpční spektrum chemické látky, můžeme měřit na jedné z jejích vlnových délek (kde je absorpce maximální) odchylky v intenzitě světelného paprsku procházejícího stejnou tloušťkou. Řešení různých koncentrací.
To umožňuje experimentálně stanovit křivku vztahující se k absorbanci a koncentraci studované látky (s ) provedením měření různých koncentrací. Tato křivka je kalibrační křivka .
Experimentální kalibrační křivka pak umožňuje určit neznámou koncentraci roztoku této látky jednoduchým měřením jeho absorbance a vynesením do grafu .
Lambert-Beerův zákon má limity. Je lineární pouze v rozsahu snížené koncentrace, který seskupuje hodnoty nižší než 10 −2 mol.L −1 .
Sledování kinetiky chemické reakceKdyž během chemické reakce, pro kterou chceme studovat kinetiku jedné z chemických látek v roztoku, je možné pomocí absorpční spektrofotometrie sledovat koncentraci této látky (obvykle barevné). Pokud je tato látka činidlem , absorbance roztoku v průběhu času klesá. Pokud naopak jde o produkt reakce, absorbance roztoku se časem zvyšuje.
Příklady
- Můžeme sledovat kinetiku oxidačně-redukční reakce v kyselém prostředí , mezi kyselinou šťavelovou C 2 H 2 O 4 manganistanovým iontem MnO 4 - (fialové zbarvení) měřením poklesu jeho absorbance pro vlnovou délku λ = 540 nm .
Reference
James Henkel, Základy kvality léčivých přípravků (str. 130 133). 1978, The Mosby Company, ( ISBN 0801600316 ) .
- Srov. G. Bruhat (2005), Optika , šesté vydání, Dunod: § Spectrophotometry.
- (in) Rozptyl světla a molekulární spektrofotometrie
Bibliografie
- Georges Bruhat , Optique , šesté vydání, sbírka referenčních kurzů, Dunod, 2005, 1152 s.
Podívejte se také
Související články
externí odkazy
- Simulace spektrofotometru ( Ang )



























