Tetrafluorohydrazin
| Tetrafluorohydrazin | |
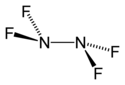   Struktura tetrafluorohydrazinu |
|
| Identifikace | |
|---|---|
| Název IUPAC | 1,1,2,2-tetrafluorhydrazin |
| Synonyma |
Perfluorhydrazin |
| N O CAS | |
| Ne o ECHA | 100 030 091 |
| Ne o EC | 233-114-6 |
| PubChem | 24845 |
| ÚSMĚVY |
N (N (F) F) (F) F , |
| InChI |
InChI: InChI = 1S / F4N2 / c1-5 (2) 6 (3) 4 |
| Chemické vlastnosti | |
| Hrubý vzorec | N 2 F 4 |
| Molární hmotnost | 104,007 ± 0,0004 g / mol F 73,07%, N 26,93%, |
| Fyzikální vlastnosti | |
| T. fúze | -164,5 ° C |
| T ° vroucí | -73 ° C |
| Kritický bod | 37,5 bar , 35,85 ° C |
| Jednotky SI a STP, pokud není uvedeno jinak. | |
Tetrafluorohydrazine je chemická sloučenina podle vzorce N 2 F 4. Je to fluorovaný analog hydrazinu . Vypadá to jako velmi reaktivní bezbarvý plyn, který exploduje při kontaktu s organickou hmotou, což činí manipulaci obzvláště nebezpečnou.
Tetrafluorohydrazine se připraví z dusitý NF 3v přítomnosti fluorid kovu, jako je měď (I), fluorid CUF nebo železa (II), fluorid FEF 2, například :
2 NF 3+ 2 CuF → N 2 F 4+ 2 CuF 2při 375 ° CN 2 F 4 zasahuje jako meziprodukt nebo jako katalyzátor v určitých procesech chemické syntézy.
Tetrafluorohydrazin byl používán v padesátých a šedesátých letech jako energetický oxidant v astronautickém výzkumu zaměřeném na vývoj vysoce výkonných pohonných látek v kontextu studené války . Kapalná paliva tvořen systémem N 2 F 4 / B 5 H 9( pentaboran ) byl zvláště studován, zejména v SSSR , předtím, než byl opuštěn kvůli jeho ceně ( bór je drahý prvek) a bezpečnostním problémům vyvolaným použitím těchto pohonných látek (manipulace s tetrafluorohydrazinem samotným je obzvláště nebezpečná a jeho spalování s pentaboranem produkuje mimo jiné fluorovodík HF, velmi toxický a vysoce korozivní).
Související články
Poznámky a odkazy
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- „ Vlastnosti různých plynů “ na adrese flexwareinc.com (přístup 12. dubna 2010 )