Octan palladnatý
| Octan palladnatý | ||
| ||
 | ||
| prášek octanu palladnatého v trimerické formě | ||
| Identifikace | ||
|---|---|---|
| Systematický název | diethanoát palladnatý | |
| Synonyma |
diacetát palladnatý, diacetatopalladium |
|
| N O CAS | ||
| Ne o ECHA | 100 020 151 | |
| N O RTECS | AJ1900000 | |
| PubChem | 167845 | |
| ÚSMĚVY |
[Pd + 2]. [O-] C (= O) C. [O-] C (= O) C , |
|
| InChI |
InChI: InChI = 1S / 2C2H4O2.Pd / c2 * 1-2 (3) 4; / h2 * 1H3, (H, 3,4); / q ;; + 2 / p-2 InChIKey: YJVFFLUZDVXJQI-UHFFFAOYSA |
|
| Vzhled | červenohnědý (trimerní forma) nebo světle růžový (polymerní forma) prášek | |
| Chemické vlastnosti | ||
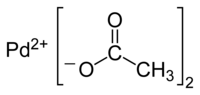
| Hrubý vzorec | Pd (CH 3 COO) 2 | |
| Molární hmotnost | 224,51 ± 0,01 g / mol C 21,4%, H 2,69%, O 28,51%, Pd 47,4%, |
|
| Fyzikální vlastnosti | ||
| T. fúze | 216,3 až 223,7 ° C | |
| T ° vroucí | 204 ° C (rozklad) | |
| Rozpustnost | 0,92 g · L -1 (voda, 20 ° C ) | |
| Opatření | ||
| SGH | ||
 H318, P280, P305 + P351 + P338 + P310,
H318 : Způsobuje vážné poškození očí
H318, P280, P305 + P351 + P338 + P310,
H318 : Způsobuje vážné poškození očí P280 : Noste ochranné rukavice / ochranný oděv / ochranné brýle / obličejový štít. P305 + P351 + P338 + 310 : Při zasažení očí: Několik minut opatrně vyplachujte vodou. Vyjměte kontaktní čočky, pokud je oběť nosí a lze je snadno vyjmout. Pokračujte v oplachování. Okamžitě volejte TOXIKOLOGICKÉ INFORMAČNÍ STŘEDISKO nebo lékaře. |
||
| Ekotoxikologie | ||
| DL 50 |
2100 mg · kg -1 (myš, orální ) 5110 mg · kg -1 (krysa, orální ) |
|
| Jednotky SI a STP, pokud není uvedeno jinak. | ||
Octanu palladnatého (II) je organická sloučenina o palladia obecného vzorce [Pd (CH 3 COO) 2 ] n, zkráceně [Pd (OAc) 2 ] n . Je reaktivnější než jeho platinový analog . V závislosti na své stechiometrii existuje ve dvou různých formách se značně odlišnými vlastnostmi.
Struktura
S poměrem jednoho atomu palladia ke dvěma acetátovým ligandům existuje sloučenina v molekulární a polymerní formě. Palladium přebírá v obou případech čtvercovou rovinnou molekulární geometrii .
Ve formě, kterou připravil Wilkinson a jeho tým v roce 1965 a kterou charakterizovali Skapski a Smart v roce 1970 rentgenovou krystalografií , je octan palladnatý (II) červenohnědá pevná látka, která krystalizuje ve formě monoklinických plaků. Má trimerní strukturu, přičemž tři atomy palladia tvoří rovnostranný trojúhelník, každý spojený se dvěma páry acetátových ligandů přemosťujících atomy palladia, v motýlí konformaci.
Octan palladnatý lze také připravit ve formě světle růžového prášku. Práškové difrakční rentgenové řekněme, že tato forma je polymerní.
-
Časová forma
-
Polymerní forma
Syntéza
Palladium (II) acetát může být připraven v jeho trimerní formě tak, že se pěna z palladia se směsí kyseliny dusičné horké a kyseliny octové . Palladium musí být v přebytku nebo musí být přítomen proud dusíku, aby se zabránilo kontaminaci směsí nitritoacetátu (Pd 3 (OAc) 5 NO 2 ):
palladium + 4 HNO 3 → Pd (NO 3 ) 2 + 2 NO 2 + 2 H 2 O Pd (NO 3 ) 2 + 2 CH 3 COOH → Pd (O 2 CCH 3 ) 2 + 2 HNO 3Octan trimelový má jinou rozpustnost a katalytickou aktivitu ve srovnání s jeho variantou obsahující směs dusičnanu a octanu. Zabránění jeho tvorbě nebo kontrola jeho množství je důležitým aspektem bezpečného používání octanu palladnatého.
Palladium propanoát (II) se připraví analogicky jako v; další karboxyláty se připravují zpracováním octanu palladnatého s vhodnou karboxylovou kyselinou . Naopak může být acetát připraven zpracováním ostatních karboxylátů palladia (II) kyselinou octovou. Tato metoda výměny ligandu s jinými čištěnými karboxyláty je životaschopnou alternativou pro syntézu octanu palladnatého bez nitro kontaminantu.
Acetát palladnatý (II), který se zahřívá v přítomnosti alkoholů nebo se dlouho vaří v jiných rozpouštědlech, se rozloží na palladium.
Použití
Katalýza
Octanu palladnatého se používá jako katalyzátor v mnoha organických reakcí , zejména ty s alkenů , dienů , alkyl , aryl a vinylových halogenidy za vzniku reaktivních aduktů .
Z reakcí katalyzovaných octanem paladnatým lze uvést:
- vinylace, například Heckova reakce a související procesy;
- přesmyk acyklických dienů, například přesmyk Cope ;
- karbonylační reakce , například tvorba esterů z aryljodidů, oxidu uhelnatého , alkoholu nebo fenolu (molekula) ;
- redukční aminace z aldehydů nebo ketonů s mravenčanem draselným ;
- proces Wacker , to znamená, že oxidace ethylenu u vody pro acetaldehyd , prekurzor poly (vinylacetát) .
- Buchwald-Hartwigova reakce mezi arylovou hlogenide nebo pseudohalogen s aminem ;
- přeměnou arylbromidů na trimethylsilany, funkční skupinu nacházející se v mnoha organických sloučeninách včetně fungicidu "Latitude".
Pd (O 2 CCH 3 ) 2 je kompatibilní s elektronickými vlastnostmi arylbromidy, a na rozdíl od jiných metod syntézy, tento způsob nevyžaduje vysoký tlak zařízení.
Prekurzor jiných sloučenin palladia
Octan palladnatý se používá k výrobě dalších sloučenin palladia (II), například octanu fenylpalladia použitého k isomerizaci allylalkoholů na aldehydy. Je připraven následovně:
Hg (C 6 H 5 ) (OAc) + Pd (OAc) 2 → Pd (C 6 H 5 ) (OAc) + Hg (OAc) 2Octan palladnatý reaguje s acetylacetonem (ligand "acac") za vzniku Pd (acac) 2 .
Lze jej použít k výrobě éalementu Hermannův katalyzátor (en) se používá zejména při Heckově reakci . Za tímto účelem reagujeme s acetátem s tris (o-tolyl) fosfinem (en) :
2 Pd (OAc) 2 + 2 P (C 6 H 4 -2-CH 3 ) 3 → 2 HOAc + Pd 2 (OAc) 2 [P (C 6 H 4 -2-CH 2 ), (C 6 H 4 - 2-CH 3 ) 2 ] 2Světlo nebo teplo redukuje octan hlinitý za vzniku tenkých vrstev palladia. Tuto vlastnost lze použít k výrobě nanodrátů a koloidů .
Poznámky a odkazy
- (en) Tento článek je částečně nebo zcela převzat z článku Wikipedie v angličtině s názvem „ octan palladnatý (II) “ ( viz seznam autorů ) .
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- Sigma-Aldrichův list sloučeniny octanu palladnatého (II) , konzultováno 14. srpna 2020.
- Gigiena i Sanitariya. Let. 51 (12), str. 88, 1986.
- Směrnice OECD pro testování 401
- T. A. Stephenson , SM Morehouse, AR Powell, JP Heffer a G. Wilkinson, „ 667. Karboxyláty palladia, platiny a rhodia a jejich adukty “, Journal of the Chemical Society (Resumed) ,1965, str. 3632 ( DOI 10.1039 / jr9650003632 )
- Skapski, A C. a ML Smart, „ Krystalová struktura octanu trimerického palladia (II) “, J. Chem. Soc. D , n o 11,1970, str. 658b - 659 ( DOI 10.1039 / C2970000658b )
- Kirik, SD, Mulagaleev, SF a Blokhin, AI, „ [Pd (CH 3 COO) 2] n z rentgenových práškových difrakčních dat “, Acta Crystallogr. C , sv. 60, n o 9,2004, m449 - m450 ( DOI 10.1107 / S0108270104016129 )
- Bakhmutov, VI, Berry, JF, bavlna, FA Ibragimov, S. a Murillo, CA, " netriviální chování palladium (II) acetát ," Dalton Transactions , n O 11,2005, str. 1989–1992 ( PMID 15909048 , DOI 10,1039 / b502122g )
- " Homogenní katalyzátor vysoké čistoty " [ archiv17. března 2006] , Engelhard ,Září 2005(zpřístupněno 24. února 2006 )
- Stephen K. Ritter , „ Chemici představují uživatelskou příručku pro octan palladnatý, “ Chemical & Engineering News , sv. 94, n o 18,2. května 2016, str. 20–21 ( DOI 10.1021 / cen-09418-scitech1 )
- Suggs, J W. „Palladium: Organokovová chemie.“ Encyclopedia of Anorganic Chemistry. Ed. R B. King. 8 letů. Chichester: Wiley, 1994.
- Kirill V. Nikitin , Andryukhova, NP, Bumagin, NA a Beletskaya, IP, „ Syntéza arylesterů Pd-katalyzovanou karbonylací aryljodidů “, Mendeleev Communications , sv. 1, n O 4,1991, str. 129 až 131 ( DOI 10,1070 / MC1991v001n04ABEH000080 )
- Linli He, Shawn P. Allwein, Benjamin J. Dugan, Kyle W. Knouse, Gregory R. Ott, Craig A. Zificsak, „ Syntéza α-karbolinu “, Org. Synth. , sv. 93,2016, str. 272 ( DOI 10.15227 / orgsyn.093.0272 )
- „ Křížová vazebná reakce Buchwald-Hartwig “ , Portál organické chemie
- Gooben, L J. „Research Area“ New Pd-Catalyzed Cross-Coupling Reactions ““ 28. února. 2006 < http://www.mpi-muelheim.mpg.de/kofo/bericht2002/pdf/2.1.8_gossen.pdf > „ https://web.archive.org/web/20070712180504/http://www.mpi -muelheim.mpg.de/kofo/bericht2002/pdf/2.1.8_gossen.pdf ” ( Archiv • Wikiwix • Archive.is • Google • Co dělat? ) ,12. července 2007.
- Herrmann, WA, Brossmer, C., Reisinger, C.-P., Riermeier, TH, Öfele, K. a Beller, M., „ Palladacycles: Efficient New Catalysts for the Heck Vinylation of Aryl Halides “, Chemistry - A European Journal , roč. 3, n o 8,1997, str. 1357–1364 ( DOI 10.1002 / chem.19970030823 )
- Richard F. Heck , Aldehydy z allylalkoholů a fenylpalladiumacetátu: 2-methyl-3-fenylpropionaldehyd , Org. Synth. , kol. „let. 6 ”, str. 815