Oxid siřičitý
| Oxid siřičitý | |
   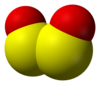 Struktura oxidu uhelnatého. (dole: „dimer“ peroxid S 2 O 2) |
|
| Identifikace | |
|---|---|
| N O CAS | |
| PubChem | 114845 |
| ChEBI | 45822 |
| ÚSMĚVY |
O = S , |
| InChI |
InChI: InChI = 1S / OS / c1-2 InChIKey: XTQHKBHJIVJGKJ-UHFFFAOYSA-N |
| Chemické vlastnosti | |
| Hrubý vzorec | S O |
| Molární hmotnost | 48,064 ± 0,005 g / mol O 33,29%, S 66,72%, |
| Jednotky SI a STP, pokud není uvedeno jinak. | |
Síry uhelnatý je chemická sloučenina podle vzorce tak. Tato molekula je termodynamicky nestabilní a jako taková existuje pouze ve zředěném plynném stavu ; se dimerizuje v S 2 O 2v kondenzovaném stavu, někdy nazývaném peroxid síry . To je důvod, proč byl oxid sírový detekován ve vesmíru, ale na Zemi přirozeně neexistuje .
SO molekula se vyznačuje triplet základní stav , jako je O 2 molekuly, to znamená, že každá molekula má dva nepárové elektrony paralelního otáčení , každý na své vlastní atomové oběžné dráze . SO vazba je 148,1 um v délce , delší než S 2 O molekul ( 146 hodin ) , SO 2 ( 143,1 pm ) a SO 3 ( 142 hodin ) .
Molekula může být excitována v singletovém stavu absorpcí infračerveného fotonu . Tento stav singlet Předpokládá se, že reaktivnější než stát triplet, jak bylo pozorováno pro O 2 molekuly..
Oxid siřičitý lze vyrábět v laboratoři žhavým výbojem přes páry síry smíchané s oxidem siřičitým SO 2a lze je detekovat sonoluminiscencí v roztoku koncentrované kyseliny sírové obsahující vzácné plyny . Na základě reakcí byl také publikován chemiluminiscenční detektor oxidu uhelnatého.
SO + O 3→ SO 2 *+ O 2, SO 2 *→ SO 2+ h ν .Oxid sírový se přirozeně vyskytuje v prostředí satelitu Io planety Jupiter , a to jak v jeho atmosféře, tak v jeho exosféře , a byl detekován v atmosféře Venuše , komety Hale-Bopp a mezihvězdného média .
Poznámky a odkazy
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (v) Norman N. Greenwood, A. Earnshaw, " Chemistry of prvků ", Butterworth-Heinemann, 2 e vydání, Oxford, 1997 ( ISBN 0080379419 ) .
- (in) „ Teplota sonoluminiscence s jednou bublinou “ KS Suslick a Flannigan DJ v The Journal of the Acoustical Society of America , (2004) 116 , 4, 2540.
-
(in) Richard L. Benner, Donald H. Stedman , „ Chemický mechanismus a účinnost detektoru chemiluminiscence síry “ , Applied Spectroscopy , sv. 48, n o 7,
Červenec 1994, str. 14A-21A a 775-903 ( číst online )
DOI : 10,1366 / 0003702944029901 -
(in) Lellouch , „ Urey Prize Reading. Io's Atmosphere: Not Yet Understood “ , Icarus , sv. 124, n o 1,
Listopadu 1996, str. 1-21 ( číst online )
DOI : 10.1006 / icar.1996.0186 -
(in) CT Russell a MG Kivelson , „ Detection of SO in Io's Exosphere “ , Science , sv. 287, n O 5460,
17. března 2000, str. 1998-1999 ( ISSN 0036-8075 , číst online )
DOI : 10.1126 / science.287.5460.1998 -
(in) Chan Y. Na, Larry W. Esposito , Thomas E. Skinner , „ International Ultrafialet Explorer Observation of Venus SO 2
and SO ” , Journal of Geophysical Research - Atmospheres , vol. 95, n o D61990, str. 7485-7491 ( číst online )
DOI : 10.1029 / JD095iD06p07485 -
(in) DC Lily, DM Mehringer, D. Benford, Gardner, TG Phillips, D. Bockelée-Morvan, N. Biver, P. Colom, J. a D. Crovisier Despois a kol . , „ New Molecular Species in Comet C / 1995 O1 (Hale-Bopp) Observed with the Caltech Ssubmillimeter Observatory “ , Earth, Moon and Planets , vol. 78, n kost 1-3,
1998, str. 13-20 ( číst online )
DOI : 10.1023 / A: 1006281802554 -
(in) AC Gottlieb, Gottlieb EW, Mr. Litvak, JA Ball a H. Penfield , „ Pozorování mezihvězdného oxidu uhelnatého “ , Astrophysical Journal, část 1 , sv. 219,
1 st 01. 1978, str. 77-94
DOI : 10,1086 / 155757