Kyselina boritá
Boronová kyselina je kyselina boritá substituovaná skupinou alkyl nebo aryl . Tyto sloučeniny proto obsahují vazbu uhlík-bór a patří do širší třídy organoboranů .
Boronové kyseliny působí jako Lewisovy kyseliny . Jejich jedinečnou vlastností je, že jsou schopné reverzibilně tvořit kovalentní komplexy s osami , aminokyselinami , hydroxamovými kyselinami atd., Molekulami, které mají donory Lewisových bazických skupin ( alkohol , amin , karboxylát ) substituované (1, 2) ( vicinální ) nebo příležitostně ( 1,3). PK boronových kyselin je obvykle v blízkosti 9, ale některé z nich mohou tvořit čtyřboké boronáty a mají pK asi 7.
Příležitostně se používají v oblasti molekulárního rozpoznávání k vazbě na sacharidy pro fluorescenční detekci nebo selektivní transport sacharidů přes membrány.
Boronové kyseliny jsou široce používány v organické chemii jako chemické a meziproduktové stavební bloky, zejména při Suzukiho vazbě . Klíčovým konceptem v jejich chemii je transmetalace organických zbytků přechodným kovem .
Bortezomib , který má skupinu kyseliny boronové je droga používá v chemoterapii . Atom boru této molekuly je klíčovou substrukturou, protože jsou blokovány určité proteazomy, které by degradovaly proteiny.
Boronové kyseliny
Mnoho boronových kyselin, které jsou stabilní na vzduchu, je komerčně dostupné. Jednou z jejich charakteristik je vysoká teplota tání . Jelikož boronové kyseliny snadno ztrácejí molekulu vody za vzniku trimerových anhydrátů , komerční vzorky často tyto anhydráty obsahují, ale to neovlivňuje jejich reaktivitu.
| Kyselina boritá | R | molární hmotnost | Číslo CAS | teplota tání (° C) | |
|---|---|---|---|---|---|
| kyselina fenylboritá | fenyl | 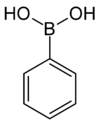 |
121,93 | 216–219 | |
| 2-thienylboronová kyselina | thiofen |  |
127,96 | 138–140 | |
| kyselina methylboritá | methyl |  |
59,86 | 91–94 | |
| kyselina cis-propenylboritá | propen | 85,90 | 65–70 | ||
| kyselina trans-propenylboritá | propen | 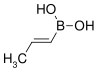 |
85,90 | 123–127 |
Syntéza
Boronové kyseliny lze získat různými způsoby. Nejběžnější metodou je reakce organokovových sloučenin na bázi lithia ( organolithia ) nebo hořčíku ( Grignardova činidla ) s estery boritanu . Například kyselina fenylboritá se vyrábí z fenylmagnesiumbromidu a trimethylborátu , následovaná hydrolýzou :
PhMgBr + B (OMe) 3 → PhB (OMe) 2 + MeOMgBr PhB (OMe) 2 + 2 H 2 O → PhB (OH) 2 + 2MeOH.Další metodou je reakce z arylsilane (RSiR 3 ) se bromid boritý (BBR 3 ) v transmetalací k RBBr 2 a následnou hydrolýzou v kyselém prostředí.
Třetí metoda je reakce katalyzovaná pomocí palladiem s arylhalogenidu a triflátů s diboronyle esterů pomocí spojovací reakce . Alternativou k esterům v této metodě je použití kyseliny diboronové nebo tetrahydroxydiboronu ([B (OH 2 )] 2 ).
Boronové estery
Tyto boronové estery nebo estery boronátem jsou estery vytvořené mezi kyselinou a jeden nebo více alkoholů nebo diolu . Kyselina fenylboritá může sama kondenzovat za vzniku cyklického trimeru zvaného trifenyl anhydrid nebo trifenylboroxin .
| Boronový ester | Diol | Strukturní vzorec | Molární hmotnost | Číslo CAS | bod varu (° C) |
|---|---|---|---|---|---|
| pinakolický ester kyseliny allylboronové | pinacol |  |
168,04 | 50–53 (5 mmHg) | |
| trimethylenglykolester kyseliny fenylborité | trimethylenglykol |  |
161,99 | 106 ( 2 mmHg ) | |
| Diisopropoxymethylboran | isopropanol | 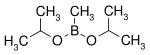 |
144,02 | 105-107 |
Sloučeniny s 5-kruhem obsahujícím skupinu COBOC se nazývají dioxaborolany a sloučeniny s 6- dioxaborinanovým kruhem .
Poznámky a odkazy
- ( fr ) Tento článek je částečně nebo zcela převzat z anglického článku Wikipedie s názvem „ Boronová kyselina “ ( viz seznam autorů ) .
- Boronové kyseliny . Editoval Dennis G. Hall 2005 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ( ISBN 3-527-30991-8 )
- Příklad: Jesper Langgaard Kristensen, Morten Lysén, Per Vedsø a Mikael Begtrup Günter Seidel a Alois Fürstner Publikováno v Org. Synth. 2005, 81, 134 Org. Synth. 2009 Sb. Let. 11, 1015 odkaz
- Příklad: Chinolin, 3- (3-pyridinyl) - Wenjie Li, Dorian P. Nelson, Mark S.Jensen, R. Scott Hoerrner, Dongwei Cai a Robert D. Larsen, Scott E. Dánsko, Geoff T. Halvorsen, a Jeffrey M. Kallemeyn Zveřejněno v Org. Synth. 2005, 81, 89 Org. Synth. 2009 Sb. Let. 11, 393 Odkaz
- Cyklopropanemethanol, 2-fenyl-, (1S-trans) - André B. Charette a Hélène Lebel Kevin Minbiole, Patrick Verhoest a Amos B. Smith, III Zveřejněno v Org. Synth. 1999, 76, 86 Org. Synth. 2004, Sb. Let. 10, 613 Odkaz
- Wahsburn, RM; Levens, E.; Albright, CF; Billig, FA, anhydrid benzenboritanu , Org. Synth. , kol. „let. 4 ",1963, str. 68
- Pilarski, LT a Szabó, KJ (2011), Palladium-Catalyzed Direct Synthesis of Organoboronic Acid . Angewandte Chemie International Edition, 50: 8230–8232. DOI : 10,1002 / anie.201102384
- Palladium katalyzovaná přímá syntéza kyseliny borité z arylchloridů: zjednodušená cesta k různým derivátům esteru boronátu Gary A. Molander, Sarah LJ Trice, Spencer D. Dreher Journal of the American Chemical Society 2010 132 (50), 17701-17703 DOI : 10.1021 / ja1089759
- Robert M. Washburn, Ernest Levens, Charles F. Albright a Franklin A. Billig, benzeneboronanhydrid , Org. Synth. , kol. „let. 4 ",1963, str. 68