Fluoren
| Fluoren | |
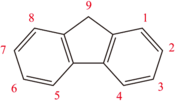  Struktura fluorenu. |
|
| Identifikace | |
|---|---|
| Název IUPAC | 9 H fluorenu |
| Synonyma |
9 H fluorenu; |
| N O CAS | |
| Ne o ECHA | 100 001 541 |
| Ne o EC | 201-695-5 |
| ÚSMĚVY |
c1ccc-2c (c1) Cc3c2cccc3 , |
| InChI |
InChI: InChI = 1S / C13H10 / c1-3-7-12-10 (5-1) 9-11-6-2-4-8-13 (11) 12 / h1-8H, 9H2 InChIKey: NIHNNTQXNPWCJQ -UHFFFAOYAW |
| Vzhled | bílé krystaly |
| Chemické vlastnosti | |
| Hrubý vzorec |
C 13 H 10 [izomery] |
| Molární hmotnost | 166,2185 ± 0,0111 g / mol C 93,94%, H 6,06%, |
| pKa | 22,6 (v DMSO) |
| Magnetická susceptibilita | 110,5 × 10 -6 cm 3 · mol -1 |
| Fyzikální vlastnosti | |
| T. fúze | 113 až 115 ° C |
| T ° vroucí | 295 ° C |
| Rozpustnost | 1,8 mg · L -1 (voda) |
| Objemová hmotnost | 1,2 g · cm -3 |
| Bod vzplanutí | 152 ° C |
| Tlak nasycených par | 13 mbar při 146 ° C |
| Opatření | |
| SGH | |
 Varování H410, P273, P501, H410 : Vysoce toxický pro vodní organismy, s dlouhodobými účinky P273 : Zabraňte uvolnění do životního prostředí. P501 : Odstraňte obsah / obal do ... |
|
| Klasifikace IARC | |
| Skupina 3: Nezařaditelné z hlediska jeho karcinogenity pro člověka | |
| Související sloučeniny | |
| Izomer (y) | Fenalen |
| Jednotky SI a STP, pokud není uvedeno jinak. | |
Fluoren nebo 9H-fluoren je chemická sloučenina z rodiny polycyklických aromatických uhlovodíků (PAU). Je ve formě bílých krystalů, které vydávají zápach podobný zápachu naftalenu .
Na rozdíl od toho, co by mohl naznačovat její název, nemá tato molekula nic společného s chemickým prvkem fluor, který jí chybí. Název fluoren pochází ze skutečnosti, že za ultrafialového (UV) světla sloučenina fluoreskuje fialovým světlem .
Vlastnosti
Fluoren je téměř nerozpustný ve vodě, ale je rozpustný v benzenu a etheru. Dva atomy vodíku v poloze 9 jsou kyselé, s pK A 22,6 v DMSO . Reakcí báze s fluorenem se tedy získá aromatický anion (velmi výrazné oranžové barvy), který je velmi nukleofilní . Fluorenový aniont se používá podobně jako u cyklopentadienu nebo indenu jako ligand v organokovové chemii .
Výskyt
Fluoren je přirozeně přítomen v dehtu , přesněji ve frakcích s vysokou teplotou varu. Získává se destilací těchto frakcí. Rovněž se nachází v malém množství, spolu s dalšími polycyklickými uhlovodíky, v produktech topení nebo spalování organických látek s nedostatkem kyslíku. Vyskytuje se také při spalování benzínu nebo nafty .
Použití
Fluoren se používá k výrobě plastů, barviv a pesticidů. Používá se k syntéze fluorenonu , fluorenolu a fluoren-9-methanolu
Skupina fluorenylmethoxykarbonyl (Fmoc) je ochranná skupina, která se používá při syntéze peptidů k ochraně aminových funkcí .
Polyfluroren se používá jako fosfor v organických diodách emitujících světlo (O-LED). Fluorenové kopolymery se také studují pro výrobu fotovoltaických článků .
Poznámky a odkazy
- Rovnovážné kyselosti v roztoku dimethylsulfoxidu, FG Bordwell, Acc. Chem. Res. ; 1988 ; 456-463, DOI : 10.1021 / ar00156a004
- (in) Hyp Daubensee J., Jr., James D. Wilson a John L. Laity, „ Diamagnetic Susceptibility Exaltation in Hydrocarbons “ , Journal of the American Chemical Society , sv. 91, n o 8,9. dubna 1968, str. 1991-1998
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- Záznam „Fluoren“ v chemické databázi GESTIS IFA (německý orgán odpovědný za bezpečnost a ochranu zdraví při práci) ( německy , anglicky ), zpřístupněno 12. 5. 2009 (vyžadován JavaScript)
- Pracovní skupina IARC pro hodnocení karcinogenních rizik pro člověka, „ Globální hodnocení karcinogenity pro člověka, skupina 3: Nezařaditelné z hlediska jejich karcinogenity pro člověka “ , na adrese http://monographs.iarc.fr , IARC,16. ledna 2009(zpřístupněno 22. srpna 2009 )
- SIGMA-ALDRICH
- (de) Tento článek je částečně nebo zcela převzat z německého článku na Wikipedii s názvem „ Fluoren “ ( viz seznam autorů ) .
- ( fr ) Tento článek je částečně nebo zcela převzat z anglického článku Wikipedie s názvem „ Fluoren “ ( viz seznam autorů ) .
