Jodometan
| Jodometan | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Struktura jodmethanu |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Název IUPAC | methyljodid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyma |
Methyl monojodmethan |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o ECHA | 100 000 745 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o EC | 200-819-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ÚSMĚVY |
CI , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3I / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | bezbarvá kapalina s charakteristickým zápachem. při vystavení světlu a vlhkosti zhnědne. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hrubý vzorec |
C H 3 I [izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární hmotnost | 141,939 ± 0,001 g / mol C 8,46%, H 2,13%, I 89,41%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolární moment | 1,59 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T. fúze | -66,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° vroucí | 42,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpustnost | ve vodě při 20 ° C : 14 g · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametr rozpustnosti δ | 9,9 kcal 1/2 · cm -3/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objemová hmotnost | 2,3 g · cm -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota samovznícení | 352 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Meze výbušnosti ve vzduchu | 8,5 - 66% | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak nasycených par | při 20 ° C : 50 kPa , 24,09 psi při 55 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritický bod | 65,9 bar , 254,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C str |
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionizační energie | 9,538 eV (plyn) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Index lomu | 1,5304 ( 20 ° C , D) 1,5293 ( 21 ° C , D) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opatření | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Nebezpečí H301, H312, H315, H331, H335, H351, H301 : Toxický při požití H312 : Zdraví škodlivý při styku s kůží H315 : Způsobuje podráždění kůže H331 : Toxický při vdechování H335 : Může dráždit dýchací cesty H351 : Podezření na vyvolání rakoviny (uveďte cestu expozice, pokud je formálně prokázáno, že neexistuje jiná cesta expozice) vede ke stejnému nebezpečí) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Neklasifikovaný produktKlasifikace tohoto produktu dosud nebyla ověřena zveřejněním toxikologické adresářové služby na 0,1% podle seznamu zveřejněných složek |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doprava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2644 : METHYL JODID |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klasifikace IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina 3 : Nezařaditelné z hlediska jeho karcinogenity pro člověka | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoxikologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1,51 - 1,69 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Jodmethanu , také známý jako methyljodidu , je chemická sloučenina vzorce CH 3 I, někdy si mě všiml. Jedná se o haloalkan odvozený od methanu , kde jeden z atomů vodíku byl nahrazen atomem jodu . Je ve formě bezbarvého hustého, prchavé kapaliny s etherickým zápach, který bere na purpurově pleť, když je vystaven světlu v důsledku přítomnosti I 2 diody.. Jodomethan se běžně používá v organické syntéze jako donor methylové skupiny při reakcích nazývaných methylace . Přirozeně je emitován v malém množství rýží .
Jodomethan hydrolyzuje při 270 ° C za vzniku jodovodíku , oxidu uhelnatého a oxidu uhličitého .
Použití
Methylační reakce
Jodmethan se používá zejména pro methylaci jiných sloučenin, u S N 2 reakcích typu . Může být snadno stericky napaden nukleofily a jodid je dobrá nukleofuga .
Může být například použit pro methylaci karboxylových kyselin (transformace na karboxylmethanoát ) nebo fenolů (tvorba methoxybenzenů):

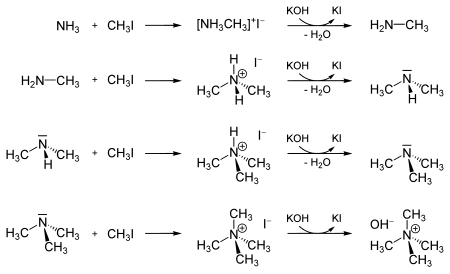
Může být také použit pro methylaci amoniaku a odvozených aminů na jodamonium. Tato reakce může pokračovat, dokud se nevytvoří hydroxid tetramethylamonný.
Jodomethan je také prekurzorem methylmagnesiumjodidu nebo „MeMgI“, Grignardova činidla často používaného v organické syntéze . MeMgI se tvoří poměrně snadno, takže se poměrně často používá jako příklad při výuce přípravy těchto reagencií. Použití MeMgI však bylo nahrazeno použitím methyllithia .
V procesu Monsanto se MeI vytváří in situ reakcí methanolu a jodovodíku . Poté reaguje s oxidem uhelnatým v přítomnosti rhodia za vzniku ethanoyljodidu , prekurzoru kyseliny octové (získaného hydrolýzou ). Velká část kyseliny octové produkované na světě se vyrábí touto metodou.
jiný
Kromě jeho použití jako methylačního činidla někteří navrhují použít jodmethan jako fungicid , herbicid , insekticid , nematicid nebo dokonce v hasicích přístrojích . Může být použit jako dezinfekční prostředek na půdu, který nahrazuje brommethan (jehož použití bylo zakázáno Montrealským protokolem ) a v mikroskopii má vlastnosti spojené s indexem lomu.
Výroba a syntéza
Jodomethan může být syntetizován exotermickou reakcí reakcí jodu s methanolem v přítomnosti fosforu . Diidoda se poté in situ transformuje na trijodid fosforitý . Následuje nukleofilní substituce methanolem:
Další metodou je reakce dimethylsulfátu s jodidem draselným v přítomnosti uhličitanu vápenatého :
Jodmethan lze poté získat destilací po promytí thiosíranem sodným, aby se odstranil přebytek jódu.
Jodomethan může být také produkován při jaderných nehodách reakcí organických sloučenin s „fúzním jodem“.
Volba jodmethanu jako methylačního činidla
Jodomethan je vynikající methylační činidlo, ale má určité nevýhody. Kromě jeho toxicity ; ve srovnání s jinými halogenmethany ( zejména chlormethanem ) je jeho ekvivalentní hmotnost vyšší: jeden mol MeI váží téměř třikrát více než jeden mol MeCl. Chlormethan je však plyn (jako brommethan ), díky čemuž je jejich použití delikátnější než kapalina jodmethan. Chlormethan je mnohem slabší methylační činidlo než MeI, ale ve většině reakcí je dostačující.
Jodidy jsou obecně mnohem dražší než jejich chloridové nebo bromidové ekvivalenty, ale dostupný jodmethan není. V komerčním měřítku je výhodný dimethylsulfát , i když je toxický, protože je levný i tekutý.
Během reakcí nukleofilních substitucí může odchod odstupující skupiny I - vést k vedlejším reakcím , protože je to silný nukleofil . Nakonec je MeI kvůli své vysoké reaktivitě nebezpečnější pro personál, který s ním zachází, než jeho bromované a chlorované ekvivalenty.
Toxicita a biologické účinky
Jodmethanu DL 50 podle perorálním podání o 76 mg · kg -1 pro krysy, a v játrech, je rychle konvertován na S-methyl- glutathionu . Ve Spojených státech je jodmethan považován za potenciálně karcinogenní podle klasifikace ACGIH (en) , NTP a EPA . IARC ji zařazuje do skupiny 3 ( „neklasifikovatelný o jejich karcinogenity u lidí“).
Vdechování par jodmethanu může způsobit poškození plic, jater, ledvin a nervového systému. Způsobuje nevolnost, závratě, kašel a zvracení. Dlouhodobý kontakt s pokožkou způsobuje popáleniny. Masivní vdechování může způsobit plicní edém .
Poznámky a odkazy
- (fr) Tento článek je částečně nebo zcela převzat z článku anglické Wikipedie s názvem „ Methyljodid “ ( viz seznam autorů ) .
- METHYL IODIDE , bezpečnostní listy Mezinárodního programu pro chemickou bezpečnost , konzultovány 9. května 2009.
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (in) Nicholas P. Chopey, Handbook of Chemical Engineering Calculation , McGraw-Hill,2004, 3 e ed. , 800 s. ( ISBN 978-0-07-136262-7 ) , str. 1.43.
- (in) „ Vlastnosti různých plynů “ na flexwareinc.com (přístup 12. dubna 2010 ) .
- (in) Carl L. Yaws, Příručka termodynamických diagramů: Anorganické sloučeniny a prvky , sv. 1, 2 a 3, Huston, Texas, Gulf Pub. Co.,1996, 384 s. ( ISBN 0-88415-857-8 , 0-88415-858-6 a 0-88415-859-4 ).
- (in) David R. Lide, Příručka chemie a fyziky , Boca Raton, CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205.
- Pracovní skupina IARC pro hodnocení karcinogenních rizik pro člověka , „ Hodnocení Globales de la Carcinogenicité pour l'Homme, skupina 3 : Nezařazení, pokud jde o jejich karcinogenitu pro člověka “ , na http://monographs.iarc.fr , IARC,16. ledna 2009(zpřístupněno 22. srpna 2009 ) .
- Indexové číslo v tabulce 3.1 z přílohy VI části nařízení ES n o 1272/2008 (16. prosince 2008).
- „ Jodomethan “ v databázi chemických produktů Reptox z CSST (quebecká organizace odpovědná za bezpečnost a ochranu zdraví při práci), zpřístupněno 25. dubna 2009.
- (en) KR Redeker, NY Wang, JC Low, A. McMillan, SC Tyler a RJ Cicerone, „ Emise methylhalogenidů a methanu z rýžových polí “ , Science , sv. 290,2000, str. 966–969 ( PMID 11062125 , DOI 10.1126 / science.290.5493.966 ).
- (in) CS King, WW Hartman: Methyljodid . In: Organic Synthesis , 1943, 2, S. 399 ( článek ).
- (in) Johnson, K., „ Metabolismus jodmethanu u krysy “ , Biochem J. , sv. 98,1966, str. 38–43.
Bibliografie
- Adams, RE, Browning Jr, WE, Cottrell, WB, & Parker, GW (1965) Uvolňování a adsorpce methyljodidu při maximální důvěryhodné nehodě HFIR (č. ORNL-TM-1291) . Národní laboratoř Oak Ridge Národní laboratoř Oak Ridge. Tenn.





