Wohl-Zieglerova reakce
Wohl-Ziegler nebo bromací Wohl-Ziegler , pojmenoval německé chemiky Alfred Wohl a Karl Ziegler , je reakcí radikál substituce vedoucí k bromačního allylových nebo benzylového uhlovodíku za použití N -bromoimide s radikálovým iniciátorem (konvenčně AIBN nebo benzoylperoxid ) nebo ozáření .
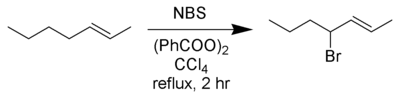
Nejlepší výtěžky této reakce byly získány s použitím N -bromsukcinimid (NBS) v roztoku v CCU 4bezvodý. Allylové a benzylové radikály vytvořené během reakce jsou stabilnější než ostatní uhlíkové radikály a převládajícími produkty jsou allylové a benzylbromidy.
Implementace
Typickým provedením této reakce je přidání stechiometrického množství N- bromsukcinimidu a malého množství iniciátoru do roztoku substrátu v CCI4 ., potom se směs míchá a přivede k varu. Zahájení reakce je indikováno intenzivnějším varem, který někdy nutí zastavit zahřívání. Jakmile se veškerý N- bromsukcinimid (hustší než rozpouštědlo) převede na sukcinimid (který plave v rozpouštědle), reakce končí.
Médium musí zůstat přísně bezvodé po celou dobu reakce, přičemž požadovaný produkt je snadno hydrolyzovatelný . Uhličitan barnatý se často používá, aby tyto bezvodé podmínky a nekyselé.
Reakční mechanismus
Zde prezentovaný mechanismus je mechanismus bromace cyklohexenu .
Zahájení:
- Rozklad AIBN na radikál dinitrogen a kyanid

- Reakce radikálu s NBS a tvorba bromového radikálu
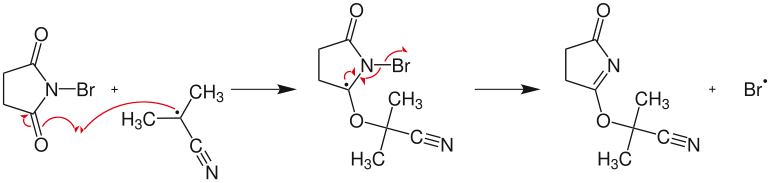
Šíření řetězce:
- Radikální reakce mezi bromovým radikálem a cyklohexenem za vzniku bromovodíku a cyklohexenylovým radikálem:

- Reakce mezi NBS za vzniku sukcinimidu a dibromu

- Radikální přidání bromu do cyklohexenylu za vzniku konečného produktu ( bromcyklohexenu ) s regenerací bromového radikálu umožňující opětovné spuštění řetězového mechanismu:

Regioselektivita
Wohl-Zieglerova reakce přednostně bromuje nejvíce přeplněnou pozici, pokud má substrát několik allylových pozic. Tato regioselektivita odpovídá tvorbě nejvíce stabilizovaného radikálu.
Pokud má molekula aromatický kruh , tvoří Wohl-Zieglerova reakce výlučně produkt bromace benzylové polohy bez jakékoli bromace kruhu.
Poznámky a odkazy
- (De) A. Wohl , " Bromierung ungesättigter Verbindungen mit N-Brom-acetamid, ein Beitrag zur Lehre vom Verlauf chemischer Vorgänge " , Ber. Dtsch. Chem. Ges. , sv. 52, n o 1,1919, str. 51-63 ( ISSN 0009-2940 , DOI 10,1002 / cber.19190520109 ).
- (De) K. Ziegler , „ Die Synthese des Cantharidins “ , Liebigs Ann. Chem. , sv. 551, n o 1,1942, str. 1–79 ( ISSN 0075-4617 , DOI 10.1002 / jlac.19425510102 ).
- (in) FL Greenwood a MD Kellert , „ 4-brom-2-hepten “ , Org. Synth. , sv. 58,1958, str. 8 ( ISSN 0078-6209 , DOI 10.15227 / orgsyn.038.0008 ).
- (in) C. Djerassi , „ Brominace N-bromsukcinimidem a souvisejícími sloučeninami. Wohl-Zieglerova reakce “ , Chem. Rev. , sv. 43, n O 21948, str. 271–317 ( ISSN 0009-2665 , DOI 10.1021 / cr60135a004 ).
- (De) L. Horner a EM Winkelman , „ Neuere Methoden der präparativen organischen Chemie II 14. N-Bromsukcinimid, Eigenschaften und Reaktionsweisen Studien zum Ablauf der Substitution XV “ , Angew. Chem. , sv. 71, n o 11,1959, str. 349-365 ( ISSN 1433 - 7851 , DOI 10,1002 / ange.19590711102 ).
- (in) RW Binkley a GS Goewey , „ vybráno regioselektivní otevírání kruhu benzylidenacetálů. Fotochemicky iniciovaná reakce pro částečnou deprotekci sacharidů “ , J. Org. Chem. , sv. 49, n O 6,1984, str. 992–996 ( ISSN 0022-3263 , DOI 10.1021 / jo00180a008 ).
- Kürti a Czakó 2005 , s. 492
- (en) / (de) Tento článek je částečně nebo zcela převzat z článků s názvem v angličtině „ Wohl - Ziegler bromination “ ( viz seznam autorů ) a v němčině „ Wohl-Ziegler-Reaktion “ ( viz seznam autorů ) .
Bibliografie
- (en) László Kürti a Barbara Czakó , Strategické Aplikace pojmenované reakcí in Organic Synthesis: Pozadí a mechanismy jejich , Amsterdam, Elsevier Academie Press,2005, 758 s. ( ISBN 0-12-429785-4 )