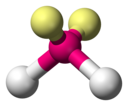
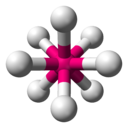
Teorie VSEPR
VSEPR teorie (zkratka anglického Valence Shell elektronový pár odpuzování , ve francouzském RPECV „odpuzování elektronických párů valenční vrstvy“) je metoda určená k predikci geometrie molekuly založené na teorii odpuzování elektronů SE K valenční skořápka . Je také známá pod názvem „Gillespie theory“ (nebo Nyholm - Gillespie theory ).
Počátky
Byl to Brit Nevil Sidgwick a Herbert Powell z Oxfordské univerzity, kteří v roce 1940 navrhli korelaci mezi molekulární geometrií a počtem valenčních elektronů. V roce 1957 na University College London , Ronald Gillespie a Ronald Sydney Nyholm používají tuto myšlenku přijít s podrobnějším teorie. V roce 1958 se Gillespie přestěhoval na McMaster University v Ontariu a pokračoval ve vývoji a zdokonalování teorie, takže je považován za skutečného původce této teorie. Metoda VSEPR je pokračováním myšlenek na chemické vazby GN Lewise (1916).
Předpoklady a předpoklady
Metoda VSEPR je založena na určitém počtu předpokladů, zejména pokud jde o povahu vazeb mezi atomy:
- atomy v molekule jsou spojeny páry elektronů;
- dva atomy mohou být spojeny více než jedním párem elektronů. Mluvíme pak o více odkazech;
- některé atomy mohou mít také páry elektronů, které nejsou zapojeny do vazby. Mluvíme o nezávazných dubletech ;
- elektrony tvořící tyto vazebné nebo nevázané dublety vyvíjejí na sebe odpudivé elektrické síly. Dublety jsou proto uspořádány kolem každého atomu tak, aby se minimalizovaly hodnoty těchto sil;
- nezávazné dublety zabírají více místa než vazebné dublety;
- více vazeb zabírá více místa než jednoduché vazby.
Zápisy
Ve zbývající části tohoto úseku, a v závislosti na používané metody VSEPR, jeden na vědomí, centrální atom molekuly studovaného .
Nezávazné dublety, to znamená páry elektronů patřících k centrálnímu atomu A, které nejsou zapojeny do vazeb, budou označeny E a jejich počtem m .
Pojiva dublety, to znamená, že páry elektronů jsou zapojeny do vazby mezi centrální atom A a další atom označíme X . Počet vázaných dubletů bude označen n .
Poznámka: Pokud jde o geometrii molekuly multi-vazba je podobný jednoduchou vazbou, která znamená, že n je jednoduše roven počtu atomů vázaných na A .
Jednoduché molekuly, jejichž geometrii lze snadno definovat pomocí metody VSEPR, mají tedy tvar: AX n E m
Údaje o odpuzování
Metoda AX
Metoda AX umožňuje definovat následující obrázky. Molekulární geometrie jsou pojmenovány pouze po atomových pozicích, ne po elektronovém uspořádání. Například popis AX 2 E 2 jako ohnuté molekuly znamená, že tři atomy AX 2 nejsou v přímé linii, přestože volné dublety pomáhají určit geometrii.
| Typ | Geometrie | Příklady |
|---|---|---|
| AX 1 E 0 (AX 1 ) | Lineární | HF |
| AX 1 E 1 | Lineární | CN - |
| AX 1 E 2 | Lineární | O 2 |
| AX 1 E 3 | Lineární | HCl |
| AX 2 E 0 (AX 2 ) | Lineární | BeCl 2 , CO 2 |
| AX 2 E 1 | Loket | SO 2 , O 3 |
| AX 2 E 2 | Loket | H 2 O |
| AX 2 E 3 | Lineární | KrF 2 , XeF 2 |
| AX 3 E 0 (AX 3 ) | Trigonale plán | BF 3 , AlCl 3 |
| AX 3 E 1 | Trigonální pyramida | NH 3 |
| AX 3 E 2 | Tvar | ClF 3 , BrF 3 |
| AX 4 E 0 (AX 4 ) | Čtyřstěn | CH 4 |
| AX 4 E 1 | Houpačka | SF 4 |
| AX 4 E 2 | Čtverec (plán) | XeF 4 |
| AX 5 E 0 (AX 5 ) | Trigonální bipyramid | PCl 5 |
| AX 5 E 1 | Čtvercová pyramida | BrF 5 |
| AX 6 E 0 (AX 6 ) | Osmistěn | SF 6 |
| AX 6 E 1 | Pětiúhelníková pyramida | XeOF 5 - |
| AX 7 E 0 (AX 7 ) | Pětiúhelníkový bipyramid | POKUD 7 |
| AX 5 E 2 | Pentagon (plán) | XeF 5 - |
| AX 8 E 0 (AX 8 ) | Čtvercový antiprismatický | [XeF 8 ] 2- |
Geometrie
Dvojrozměrné molekuly|
Sterické číslo m + n |
Základní geometrie 0 nezávazný dublet m = 0 |
1 nezávazný dublet m = 1 |
2 nezávazné dublety m = 2 |
3 nezávazné dublety m = 3 |
|---|---|---|---|---|
| 1 |
lineární |
|||
| 2 |
lineární |
lineární |
||
| 3 |
 trojúhelník (rovina) |
 loket |
 lineární |
|
| 4 |
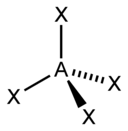 čtyřstěn |
 trigonální pyramida |
 loket |
 lineární |
| 5 |
 trigonální bipyramid |
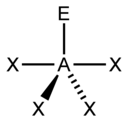 houpačka |
 Tvar |
 lineární |
| 6 |
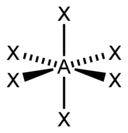 osmistěn |
 čtvercová pyramida |
 čtverec (plán) |
|
| 7 |
 pětiúhelníkový bipyramid |
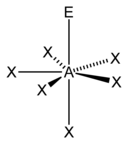 pětiboká pyramida |
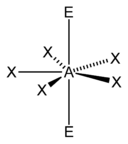 pětiúhelník (letadlo) pětiúhelník (letadlo)
|
|
| 8 |
čtvercový antiprismatický |
Vylepšení modelu
Délka dluhopisů
Dosud jsme uvažovali, že vazby mezi atomy mají stejnou délku, hrubou aproximaci a jsou daleko od reality. Délka vazby se skutečně liší v závislosti na použitých atomech a typu vazby (jednoduchá vazba, dvojná vazba , trojná vazba , aromatická vazba ...)
Je možné určit vzdálenost oddělující dva atomy experimentálně, i když to není konstantní a závisí na médiu. Je však možné definovat průměrnou hodnotu.
Metoda s kovalentními paprskyJako první aproximaci můžeme asimilovat atomy do koulí, jejichž poloměr se rovná poloměru kovalence . Délka vazby pak bude dána součtem poloměrů kovalence zúčastněných atomů:
s kovalentním poloměrem prvního atomu a kovalentním poloměrem druhého atomu.
Metoda zohledňující rozdíl v elektronegativitěProtože každý z atomů má jinou elektronegativitu , ovlivňuje to také délku vazeb; konkrétněji silný rozdíl v elektronegativitě znamená významné zkrácení vazby. Můžeme tedy stanovit následující (empirický) vzorec:
s kovalentním poloměrem prvního atomu (v pikometrech ) a kovalenčním poloměrem druhého atomu (v pikometrech), což je rozdíl v elektronegativitě mezi dvěma atomy (podle Paulingovy stupnice ).
Vliv více dluhopisůVýše uvedené vzorce umožňují vypočítat délky jednotlivých vazeb s relativně nízkou chybovostí. Z těchto měření lze snadno získat údaje z více odkazů.
Dvojná vazba je v průměru 86% z délky jednoduché vazby. Trojná vazba je v průměru 78% délky jednoduché vazby.
Aromatické vazby, například vazby přítomné v molekule benzenu , jsou například mezi jednoduchými vazbami a dvojnými vazbami:
- kovalentní poloměr uhlíku: 77 pm ;
- délka jednoduché vazby uhlík-uhlík (vypočítaná): 154 um;
- délka dvojné vazby uhlík-uhlík (vypočítaná): 133 um;
- délka vazeb uhlík-uhlík v molekule benzenu (experimentální): 140 µm.
Omezení modelu
I když metoda VSEPR umožňuje uspokojivě předpovídat geometrii jednoduchých molekul, pro které je snadný výběr centrálního atomu, zůstává obtížnější ji aplikovat a je nedostatečná, pokud jde o předpovídání geometrie složitějších molekul. Například, všechny atomy z ethylenu molekuly (CH 2 = CH 2 ), jsou umístěny ve stejné rovině, která nemůže být předpovězena s modelem. Pokročilejší modely umožňují překonat tyto nedostatky, jako je teorie molekulárních orbitalů .
Kromě toho molekuly, atomy, elektrony, nukleony nejsou pevné struktury v čase a prostoru. Jejich relativní polohy se mění v čase a v závislosti na médiu (viz infračervená spektroskopie - elektron ). Je třeba si uvědomit, že tato teorie je ve srovnání s kvantovou chemií a digitální chemií zjednodušující .
Poznámky a odkazy
- Sargent-Welch Scientific Canada Limited, Periodická tabulka prvků , Londýn, Ontario,1992
- Bernard Valeur, Molekulární struktury , Paříž, Inženýrské techniky,2004
externí odkazy
- (fr) „ Na geometrii molekul “ ( Archiv • Wikiwix • Archive.is • Google • Co dělat? )
- ( fr ) Teorie VSEPR na webových stránkách University of Sheffield