Kyanid
| Kyanid | |
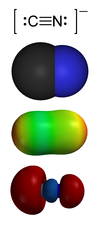
| |
| Identifikace | |
|---|---|
| N O CAS | |
| PubChem | 5975 |
| ChEBI | 17514 |
| ÚSMĚVY |
[C -] # N , |
| InChI |
InChI: InChI = 1 / CN / c1-2 / q-1 InChIKey: XFXPMWWXUTWYJX-UHFFFAOYAF Std. InChI: InChI = 1S / CN / c1-2 / q-1 standardní InChIKey: XFXPMWWXUTWYJX-UHFFFAOYSA-N |
| Chemické vlastnosti | |
| Hrubý vzorec |
C N - |
| Molární hmotnost | 26,0174 ± 0,001 g / mol C 46,16%, N 53,84%, |
| Elektronické vlastnosti | |
| 1 re ionizační energie | 13,5984 eV (plyn) |
| Terapeutické úvahy | |
| Protijed | Thiosíran sodný |
| Jednotky SI a STP, pokud není uvedeno jinak. | |
V chemii termín kyanid - z řeckého slova κυανός ( kyanos ), což znamená modrá - označuje:
- kyanid ion C≡N - , An anion se skládá z uhlíkového atomu , které jsou spojeny s trojnou vazbou k dusíku, atomu a nesoucí záporný elementární náboj ; konjugovaná báze kyanovodíku HC3N, jejíž vodný roztok se nazývá kyselina kyanovodíková;
- se solí tohoto iontu, jako je kyanid draselný (KCN), ze sodné soli (NaCN) nebo stříbro (AgCN);
- jsou organické molekuly , které mají skupinu kyano -C = N, formálně nazvaný nitrily .
V běžném jazyce termín kyanid obecně označuje jednu z forem otravy kyanidem : plynný kyanovodík, kyanid draselný nebo kyanid sodný.
Zdroj a použití
V přírodě
Kyanidy mohou být produkovány bakteriemi , plísněmi a řasami a nacházejí se v mnoha potravinách a rostlinách. V rostlinách jsou kyanidy normálně vázány na molekuly cukru ve formě kyanogenních glykosidů a slouží v rostlinách jako obrana proti býložravcům . Kořeny manioku a lněná semínka obsahují kyanogenní glukosidy a často je nutné je před konzumací ošetřit (obvykle prodlouženým vařením).
Jámy peckovin , jako jsou třešně nebo meruňky , často obsahují kyanidy nebo kyanogenní glykosidy . Jablečná semínka ho také obsahují. Tyto hořké mandle , které jsou vyrobeny na mandlový olej také obsahují Kyanogenní glykosid, amygdalin .
Požití 50 hořkých mandlí může způsobit smrt člověka při otravě kyanidem . Mnoho enzymů hydrogenázy obsahuje na svých aktivních místech kyanidové ligandy .
Lepidoptera rodiny Zygaenidae vydávat kapalný kyanid když zaútočil.
Podle Kanadské agentury pro kontrolu potravin se cyanogenní glykosid v mandlích peckovin stává toxickým, když se v těle změní na kyselinu kyanovodíkovou. Letální dávka kyanidu se pohybuje mezi 0,5 a 3 mg na kilogram tělesné hmotnosti.
Průmyslová produkce
Z amoniaku a metanu , jiných uhlovodíků nebo oxidu uhelnatého viz kyanovodík .
Kyanid sodný se také vyrábí reakcí mezi amidem sodným a uhlíkem .
Tyto nitrily se často vyrábí oxidací z uhlovodíků s amoniakem ( např. Akrylonitril ) nebo dehydratací z amidů .
Chemie
Koordinační chemieKyanid je velmi nukleofilní ligand, který tvoří komplexy s mnoha přechodnými kovy . Vysokou afinitu kovů ke kyanidu lze připsat jeho negativnímu náboji a jeho schopnosti vstoupit do vazby pí.
Struktura komplexních kyanidů- Oktokyanidy [M (CN) 8 ] 4- (M = Mo, W), které mají dodekahedrální tvar;
- Hexacyanides [M (CN) 6 ] 3- (M = Ti, V, Cr, Mn, Fe, Co), které mají oktaedrický tvar ;
- Tetracyanidy [M (CN) 4 ] 2- (M = Ni, Pd, Pt), které mají rovinný čtvercový tvar ;
- Dikyanidy [M (CN) 2 ] - (M = Cu, Ag, Au), které mají lineární tvar .
Tyto ferrokyanidy (nebo hexakyanoželeznatan II ), Fe (CN) 6 4 - jsou prakticky neškodný. Hexakyanoželeznatan sodný , z draslíku a vápníku jsou potravinové přísady ( protispékavá ), v tomto pořadí odkazuje E 535, E 536 a E 538. hexakyanoželeznatan draselný je povoleno v vinařství pro lepení z vína bílých nebo růžových vín, které mají přebytečné železo nebo měď.
Tyto ferikyanidy (nebo hexakyanoželezitan III ), Fe (CN) 6 3 mají také nízkou toxicitu, jsou používány v fotografování , jako oslabení činidlo pro tisky stříbrné černé a bílé, a jako aktivní složky pro kyanotypie a cyanographie .
Pruská modř je tmavě modrý pigment používá jako barvivo, kyanid komplexu je železo. Je to on, kdo je aktivní v kyanotypové emulzi a cyanografii . Pruská modř může produkovat vodík kyanid působením kyselin .
Redoxní vlastnostiKyanid iont je redukční činidlo a je oxidován pomocí silných oxidačních činidel , jako je molekulární chlor (Cl 2 ), chlornan (ClO - ) a peroxid vodíku (H 2 O 2 ). Tyto oxidanty se používají ke zničení kyanidu v odpadních vodách ze zlatých dolů . Tyto Měďnaté ionty (Cu 2+ ) katalyzují oxidaci kyanidů, že se vytvoří komplex meziproduktu. Anionty kyanidu (CN - ) se nejprve oxiduje na kyanát ([OCN] - ), který pak může být rozložen do amoniak (NH 3 ) a nakonec do dusíku plynu (N 2 ).
Organické kyanidyTyto organické molekuly , které mají kyanoskupinu -C = N, se nazývají nitrily .
V organické syntéze jsou nitrily syntetické meziprodukty pro homologační reakce , to znamená pro zvýšení délky uhlíkového řetězce o jednu jednotku .
Hutnictví
Kyanid se používá v hornictví a v průmyslu k extrakci zlata a stříbra . Kyanid se také používá k provádění elektrodepozice ( elektrolýzou ) určitých kovů (stříbro, zlato, kadmium, měď, rtuť atd.).
bezpečnostní
Toxicita
Soli kyanidu je velmi toxický , jakož i kyanovodík a jeho řešení, kyseliny kyanovodíkové.
Tyto ferikyanidy a ferrokyanidy nejsou toxické, protože ligandy jsou pevně spojeny s centrálním iontem, ale mohou rozkládat za působení kyseliny nebo tepla a pak uvolnit kyanovodík.
Kyanidový iont se váže na atomy železa obsažené v hemoglobinu a cytochromoxidáze (iont Fe 2+ / Fe 3+ ). Ten je zodpovědný za transport a použití kyslíku v mitochondriálním dýchacím řetězci . Je třeba poznamenat, že pokud vazba kyanidu na hemoglobin posune křivku nasycení hemoglobinu doleva a tím sníží extrakci kyslíku tkáněmi, je tento mechanismus mírný při smrti intoxikací.
Je zvláště / impozantní ve formě kyanovodíku , těkavé a velmi toxické sloučeniny. Tento plyn vzniká zejména při okyselení kyanidů (po požití v roztoku nebo žaludeční šťávou). Může být použit pro své anoxické vlastnosti jako chemická zbraň .
Otrava kyanidem může nastat jednoduše během požití určitých rostlin ( maniok , maniok atd.) A kamenů určitých druhů ovoce . Obsahují molekulu kyanogenu , amygdalin , který se ve střevě štěpí účinkem beta-glukosidáz na glukózu , aldehyd a kyanid . Hořká mandle sama o sobě má na vzduchu aktivovanou beta-glukosidázu, uvolňuje vůni kyanovodíku a benzaldehydu , je to ta druhá, která vydává zápach hořkých mandlí, které se běžně připisují kyanidu. - dokonce.
Amygdalin a laetril jsou nesprávně prezentovány jako přírodní protirakovinné léky, aniž by prokázaly svou účinnost in vivo , a představují vysoké riziko otravy kyanidem.
Při spalování určitých polymerů ( polyurethany , vinyly , vlna) se uvolňuje kyanovodík a může dojít k otravě, zejména v případech „požárů v posteli“ (lidé kouří v posteli, usínají, cigarety způsobují pomalé spalování. Deky), kde oběti umírají na otravu před spálením. Použití kyanidových solí v metalurgii také zvýšilo riziko otravy.
Kyanidy, zejména kyanidy draselné a sodné, se používají jako pesticidy pro tyto toxické vlastnosti a lze je přesměrovat k nezákonným účelům, jako je kyanidový rybolov. Cyklon B , použitý nacisty během druhé světové války jako jed v plynové komoře , obsahuje kyseliny kyanovodíkové.
Reaktivita
Kyanidové ionty již vázané na železnaté ( ferokyanidové ) nebo železité ( ferricyanidové ) ionty se normálně neváží na železo v hemoglobinu a cytochromech . Podobně jako ty spojené s kobaltem, například ve vitaminu B12 .
Kyanidové ionty mohou být oxidovány pomocí kyslíku na méně toxické kyanáty , které pak může hydrolyzovat na oxid uhličitý a amoniak . Síry oxidu v kyanidů thiokyanát méně toxické.
Kyanidová skupina se váže na alkylovou nebo arylovou skupinu . V případě nitrilů, jako je acetonitril nebo polyakrylonitril , je kyanidová skupina dostatečně navázána, aby již neútočila na železo, protože neexistují žádné skupiny, které by poskytovaly elektrony, které by kompenzovaly odchod kyanidu.
U kyanohydrinů však kyslík alkoholové funkce snadno ztrácí svůj kyselý proton a takto uvolněný elektronový pár se může stát pí vazbou karbonylové skupiny (CO). Kyanidu anion pak opustí s párem elektronů, které je spojené s karbonylový uhlík.
Protilátky
Existují následující antidota:
- amylnitrit kombinovaný s dusitanem sodným a thiosíranem sodným ,
- hydroxokobalamin , který zachycuje kyanid, čímž se získá vitaminu B 12 , a netoxické vylučuje močí,
- kobaltové soli .
- dicobaltic EDTA
Je nutné rychle reagovat a v případě zástavy dýchání dýchat kyslík a v žádném případě necvičit z úst do úst, protože při výdechu existuje riziko intoxikace.
Působení kyanidových antidot je založeno na následujících mechanismech:
- Amylnitrit a dusitan sodný indukují tvorbu methemoglobinu, který na rozdíl od nativního hemoglobinu váže ionty kyanidu. To umožňuje odstranění části kyanidu z cíle. Tento mechanismus účinku činí použití tohoto antidota nebezpečným, pokud je spojena otrava oxidem uhelnatým, která již snižuje podíl aktivního hemoglobinu. Tato související intoxikace je však častá (ko-intoxikace kouřem z ohně).
- Thiosíran umožňuje metabolismus kyanidu na netoxický tyokyanát. Jedná se o pomalejší akci, takže toto antidotum se nepoužívá samostatně v případě nouze.
- Hydroxokobalamin a soli kobaltu zachycují kyanidový iont a umožňují jeho vylučování močí.
Nomenklatura
- CAS číslo: 151-50-8
- Toxikologický list INRS: FT111
- CAS číslo: 143-33-9
- Toxikologický list INRS: FT111
Dějiny
- Na konci druhé světové války spáchalo několik nacistů sebevraždu požitím kapsle s kyanidem, zejména Richard Glücks (1889-1945), Heinrich Himmler (1900-1945), Eva Braun (1912-1945), Hermann Göring (1893-1946) ); Magda Goebbels (1901-1945) a Joseph Goebbels otrávili svých šest dětí kyanidem a následně spáchali sebevraždu, ale střelili si do hlavy.
- Pokus otrávit Rasputina kyanidem byl neúspěšný, ale není známo, zda se uchýlil k mithridatizaci, nebo zda kyanid reagoval na pečení cukrem koláče, do kterého byl umístěn.
- 914 následovníků sekty Lidového chrámu zemřelo na absorpci kyanidu při hromadné sebevraždě v roce 1978.
- The 30. ledna 2000Jeden z nejhorších ekologických katastrof v Evropě se konal: na Únik kyanidu v Baia Mare , Rumunsko .
- The 12. srpna 2015V Tchien-ťinu ve východní Číně zničily dvě silné exploze sklad obsahující 700 tun kyanidu sodného .
- The 29. listopadu 2017Zatímco Slobodan Praljak , bývalý chorvatský důstojník, který byl souzen u Mezinárodního trestního tribunálu pro bývalou Jugoslávii (ICTY), obviněn z válečných zločinů, po vynesení rozsudku najednou vytáhl z kapsy malou lahvičku a spolkl její obsah. Rychle se o něj postarala pohotovostní služba, ale nepřežil. O několik hodin později zemřel. Pitva provedená na jeho těle prokázala, že tekutina požitá generálem Praljakem obsahovala kyanid.
V detektivních románech
- V románu „ Le Grand Sommeil “ od Raymonda Chandlera je jedna z postav otrávena kyanidem smíchaným s whisky.
- V seriálu Henderson's Boys of Robert Muchamore se používá ve formě pilulky v případech krajní nouze.
Agatha Christie
- Práškový kyanid draselný rozpuštěný v šampaňském se používá ke spáchání dvou vražd v Champagne Murder .
- První a pátá vražda Deseti malých černochů jsou spáchány s kyanidem (pro jednoho šampaňské, pro druhé injekční stříkačkou).
- Druhá vražda ve hře Smrt v oblacích se provádí s kyanidem, jen aby byla maskovaná jako sebevražda.
- V The otravných Feather paní Symmington končí svůj život požitím kyanidu určen pro zahradničení.
- U žluté duhovky je oběť zabita kyanidem draselným ve směsi se šampaňským.
Poznámky a odkazy
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (in) David R. Lide, Příručka chemie a fyziky , Boca Raton, CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205.
- Praktický průvodce toxikologií, F.-X. Reichl, R. Perraud, Ed. Krahé, 2004, str. 134 .
- Kanadská agentura pro kontrolu potravin - Přírodní toxiny v čerstvém ovoci a zelenině .
- Young, CA, & Jordan, TS (1995, květen). Sanace kyanidů: současné a minulé technologie. In: Sborník z 10. výroční konference o výzkumu nebezpečných odpadů (str. 104–129). Kansas State University: Manhattan, KS. https://engg.ksu.edu/HSRC/95Proceed/young.pdf
- (in) Dmitrij Yermakov, „ Kyanidové ničení | SRK Consulting ” , na srk.com (přístup 2. března 2021 )
- Botz Michael M. Přehled metod zpracování kyanidem. Elbow Creek Engineering, Inc. http://www.botz.com/MEMCyanideTreatment.pdf
- Kyanidace a zlato: Rozpuštění vodou? : vysvětlující článek publikovaný společností Culturesciences-Chimie École Normale Supérieure - DGESCO.
- (in) Judith E Tintinalli David Cline et al. , Tintinalli je Emergency Medicine Manual: 7 th edition , New York, McGraw-Hill Professional,2012, 7 th ed. , 969 s. ( ISBN 978-0-07-178184-8 , OCLC 755056524 ).
- (in) „ Kyanid: snadný smrtící cíl chytání ryb “ na WWF ,29. ledna 2003(zpřístupněno 31. března 2019 )
- (in) „Smrt řeky“ , BBC ,15. února 2000.
- „ Tianjin: Čínské úřady potvrzují přítomnost stovek tun kyanidu “, Le Monde.fr ,16. srpna 2015( ISSN 1950-6244 , číst online , přístup k 16. srpnu 2015 ).
- „ Exploze v Číně: přítomnost vysoce toxického kyanidu sodného “, Le Point ,15. srpna 2015( číst online ).
Podívejte se také
Související články
externí odkazy
- Toxikologický list INRS pro kyanidy sodíku a draslíku [PDF]
- Tisková zpráva společnosti Euromines, která stanoví pozici evropského komisaře pro životní prostředí, pana Potočnika, v návaznosti na usnesení Evropského parlamentu o obecném zákazu používání technologií založených na kyanidech v Evropské unii [PDF] ; Brusel,1 st 07. 2010,
- Mezinárodní kodex pro správu kyanidů [PDF] (verze 11. ledna 2011, napsaná a podporovaná „skupinou společností na těžbu zlata a producentů kyanidů po celém světě“), která se prosazuje jako „iniciativa členství dobrovolná pro průmysl těžby zlata, producenty a přepravci kyanidů používaných při těžbě zlata. Jeho cílem je doplnit stávající předpisy, které jsou závazné pro všechny těžební společnosti. Dodržování pravidel, předpisů a zákonů příslušných jurisdikcí je povinné; účelem tohoto kodexu není porušovat tyto zákony “; PDF, 12 s. , Konzultováno 2014-02-25
Bibliografie
- Úmluva o zákazu vývoje, výroby, hromadění zásob a použití chemických zbraní a o jejich zničení (konzultováno dne 5. 7. 2010).
- Kruhový n o 700 / NWMO / PES / PPS ze dne 7. listopadu 2008 o národní zaměstnanosti doktríny nouzových zařízení a péče o obličej akci terorista zavedením chemikálie.
- Rauber C, Kupferschmidt H. (2008) Otrava kyanidem [PDF] Švýcarské centrum pro toxikologické informace; Leden 2008 (konzultováno 27. 7. 2010)
- INRS (2006) Kyanovodík a vodné roztoky . List toxikologických údajů FT 4, vydání 2006.
- INRS (2006) Kyanid sodný a kyanid draselný . List toxikologických údajů FT 111, vydání 2006.
- INERIS (2006). Kyanidy a deriváty List toxikologických a environmentálních údajů o chemických látkách. (v n o 1 ze dne 27. července 2006)
- Benaissa L, Hantson P, Laforge M, Borron S, Baud F. (1999) Kyanid a kyanogenní toxické látky . v Encyclopédie Médico-Chirurgicale pracovní a environmentální patologie. Paříž: Elsevier Masson SAS, 16-048-C-20 ,: 7 str.
- Cavallo JD, Fuilla C, Dorandeu F, Laroche P, Vidal D. (2010) CBRN-E riskuje, že bude vědět, zda má jednat . Paříž: vydání Xaviera Montaubana; 336 s.
- INRS (2004) acetonitril . List toxikologických údajů FT 104, vydání z roku 2004.
- INRS (2004) akrylonitril . List toxikologických údajů FT 105, vydání z roku 2004.
- Lgifrance Vyhláška n o 88-448, ve znění vyhlášky n o 95-608 na ochranu pracovníků vystavených plynů pro fumigaci.
- Falcy M, Malard S. (2005) Porovnání čichových prahových hodnot chemických látek s bezpečnostními indikátory používanými na pracovišti (ND 2221) . INRS . Průmyslová hygiena a bezpečnost. Notebooky na dokumenty; 1 st čtvrtletí 2005; 198: 7-21.
- Renard C, Dorandeu F, Borron S, Baud F, Rüttmann M, Vest P a kol. (2003) Novinky o otravě kyanovodíky . Medicine and the Armmi; 31 (3): 218-26.
- [Rivièrea, F., Bohanda, S., Fuillab, C., Petitc, JL, Lapostolled, F., Lamberte, Y .... & Larochea, P. (2010). Otrava kyanovodíky: přemýšlejte o tom! [PDF] . medicína a armády, 38 (5), 387-396.