Oxid wolframový
| Oxid wolframový | |
| |
|
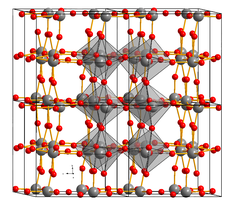
__ W 6+ __ O 2– Krystalová struktura oxidu wolframového |
|
| Identifikace | |
|---|---|
| N O CAS | |
| Ne o ECHA | 100 013 848 |
| Ne o EC | 215-231-4 |
| N O RTECS | YO7760000 |
| PubChem | 14811 |
| ÚSMĚVY |
O = [W] (= O) = O , |
| InChI |
Std. InChI: InChI = 1S / 3O.W Std. InChIKey: ZNOKGRXACCSDPY-UHFFFAOYSA-N |
| Vzhled | žlutá až zelená krystalická pevná látka |
| Chemické vlastnosti | |
| Hrubý vzorec |
O 3 Ž |
| Molární hmotnost | 231,84 ± 0,01 g / mol O 20,7%, W 79,3%, |
| Fyzikální vlastnosti | |
| T. fúze | 1472 ° C |
| T ° vroucí | 1837 ° C |
| Objemová hmotnost | 7,16 g · cm -3 až 20 ° C |
| Opatření | |
| SGH | |
 Varování H315, H319, H335, P261, P280, P302 + P352, P305 + P351 + P338, H315 : Dráždí kůži H319 : Způsobuje vážné podráždění očí H335 : Může dráždit dýchací systém P261 : Zamezte vdechování prachu / dýmu / plynu / mlhy / par / aerosolů. P280 : Noste ochranné rukavice / ochranný oděv / ochranné brýle / obličejový štít. P302 + P352 : Při styku s kůží: omyjte velkým množstvím vody a mýdla. P305 + P351 + P338 : Při zasažení očí: Několik minut opatrně vyplachujte vodou. Vyjměte kontaktní čočky, pokud je oběť nosí a lze je snadno vyjmout. Pokračujte v oplachování. |
|
| Jednotky SI a STP, pokud není uvedeno jinak. | |
Oxid wolframový nebo wolframu oxid (VI) , je chemická sloučenina podle vzorce WO 3. Jedná se o krystalickou pevnou látku, která při pokojové teplotě vykazuje intenzivní žlutozelené zbarvení a při zahřívání se mění na oranžovou. Je nerozpustný ve vodě a kyselinách , ale může reagovat s vodou za vzniku kyseliny wolframové H 2 WO 4, Který je vlastně jeho mono hydrát WO 3 · H 2 O. Toto je také forma hydrátů, která se nachází v přírodě, prostřednictvím anorganických vzácných látek, jako je wolframit (en) WO 3 · H 2 O(monohydrát) a meymacite WO 3, 2 H 2 O(dihydrát). Spolu s alkalickými a kovů alkalických zemin , tvoří soli zvané wolframany .
Krystalová struktura z oxidu wolframového závisí na teplotě: je triklinický od -50 , aby 17 ° C , jednoklonné z 17 , aby 330 ° C , kosočtverečné z 330 , aby 740 ° C a tetragonální nad 740 ° C . Jeho nejběžnější forma je monoklinická, s prostorovou skupinou P 2 1 / n .
Oxid wolframový je meziprodukt při výrobě wolframu z jeho rud po ošetření bázemi a před redukcí na kovový wolfram uhlíkem nebo vodíkem :
2 WO 3+ 3 C → 2 W + 3 CO 2 (vysoká teplota) ; WO 3+ 3 H 2→ W + 3 H 2 O( 550 až 850 ° C ).Oxid wolframu lze získat několika způsoby. Je například možné reagovat s scheelitem nebo wolframanem vápenatým CaWO 4, s kyselinou chlorovodíkovou HC1 za získání kyseliny wolframové H 2 WO 4, který dehydratuje při vysoké teplotě:
CaWO 4+ 2 HCl → CaCl 2+ H 2 WO 4 ; H 2 WO 4→ H 2 O+ WO 3.Další běžně používané způsob, jak produkovat oxid wolframový, je praženého amonný parawolframan (NH 4 ) 10 (H 2 W 12 O 42 ) 4H 2 Ov oxidačním prostředí :
(NH 4 ) 10 (H 2 W 12 O 42 ) 4H 2 O→ 12 WO 3+ 10 NH 3+ 10 H 2 O.Oxid wolframu se běžně používá k výrobě wolframanu pro luminiscenční potah rentgenových obrazovek , pro textilie zpomalující hoření a v detektorech plynů. Používá se také jako pigment v keramice a barvách díky své silné žluté barvě.
Oxid wolframu se také používá k výrobě elektrochromního skla . Jedná se o sklo, jehož optické přenosové vlastnosti lze modulovat v závislosti na aplikovaném elektrickém napětí .
Poznámky a odkazy
- Záznam „Oxid wolframu“ v chemické databázi GESTIS IFA (německý orgán odpovědný za bezpečnost a ochranu zdraví při práci) ( německy , anglicky ), přístup k 9. únoru 2019 (je nutný JavaScript)
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- „ List sloučeniny wolframu (VI) oxidu, Puratronic®, 99,998% (na bázi kovů kromě Mo), Mo 100 ppm “ , na Alfa Aesar (přístup 9. února 2019 ) .
- (en) Erik a Wolf-Dieter Schubert Lassner, Tungsten: Properties, Chemistry, Technology of the Element, Alloys, and Chemical Compounds , Kluwer Academic, New-York, 1999. ( ISBN 0-306-45053-4 )
- (en) Pradyot Patnaik, Handbook of Anorganic Chemical Compounds , McGraw-Hill, 2003. ( ISBN 0-07-049439-8 )
- (in) David E. Williams, Simon R. Aliwell Keith FE Pratt, Daren J. Caruana, Roderic L. Jones, R. Anthony Cox, pan Graeme Hansford a John Halsall , „ Modelování reakce polovodiče na bázi oxidu wolframu jako plynový senzor pro měření ozonu “ , Measurement Science and Technology , roč. 13, n O 6, Červen 2002, str. 923-931 ( DOI 10.1088 / 0957-0233 / 13/6/314 , Bibcode 2002MeScT..13..923W , číst online )
- (en) WJ Lee YK Fang, Jyh-Jier Ho, WT Hsieh, SF Ting, Daoyang Huang a Fang C. Ho , „ Účinky povrchové pórovitosti je oxid wolframový (WO 3 ) Electrochromic performance Movies " , Journal of Electronic Materials , sv. 29, n O 2Únor 2000, str. 183-187 ( DOI 10.1007 / s11664-000-0139-8 , Bibcode 2000JEMat..29..183L , číst online )