Cyklopropanace
V organické chemii se cyklopropanací rozumí jakýkoli proces vedoucí k vytvoření cyklopropanového kruhu . Tyto metody jsou důležité v moderní chemii, protože tento motiv obsahuje mnoho užitečných sloučenin. To je například případ s pyrethroidy , rodině insekticidů , nebo mnoha antibiotik chinolonu třídy ( ciprofloxacin , sparfloxacin , atd ). Vzhledem k cyklickému napětí jsou tyto reakce obecně obtížně proveditelné a vyžadují použití vysoce reaktivních látek, jako jsou karbeny , ylidy nebo karbanionty . Mnoho z těchto reakcí má způsob působení chélotrope (in) .
Přístupy
Z alkenů a karbenoidů
Existuje několik metod pro přeměnu alkenů na cyklopropan pomocí činidel karbenového typu . Posledně jmenované jsou zvláště reaktivní a je běžné je používat ve stabilizované formě, zvané karbenoidy (en) .
Simmons-Smithova reakceV Simmons-Smithově reakci je karbenoidním činidlem jodmethylzinc jodid , typicky vytvořený reakcí mezi dijodmethanem a párem zinek-měď .

Byly vyvinuty levnější alternativy, jako je použití dibromomethanu , diazomethanu a jodidu zinečnatého . Reaktivitu systému lze také zvýšit použitím diethylzinku místo dvojice zinek-měď. Existují také asymetrické varianty .
Použití diazo sloučeninNěkteré diazosloučeniny , jako je diazomethan , mohou reagovat s alkeny za vzniku cyklopropanů ve dvoustupňových procesech. První krok spočívá v 1,3-dipolární cykloadici za vzniku pyrazolinu . Ten pak podléhá denitrogenaci, buď fotochemicky nebo tepelným rozkladem , za vzniku cyklopropanu. Tepelně, často používaný jako katalyzátor KOH a platina , je také známý pod názvem Kishnerova syntéza cyklopropan , pojmenovaný po ruském chemikovi Nikolai Kischnerovi (in) , a může být aplikován pomocí hydrazinu a α, β-nenasycených karbonylových sloučenin . Mechanismus rozkladu byl předmětem mnoha studií, a pokud předmět zůstane kontroverzní, běžně se jedná o myšlenku, že k němu dochází prostřednictvím diradikálních druhů. Z hlediska zelené chemie je tato metoda považována za lepší než u jiných cyklopropanací na bázi karbenu, protože nezahrnuje použití kovů nebo halogenů a jejím jediným vedlejším produktem je dinitrogen . Tato reakce však může být nebezpečná, protože během tepelného přesmyku pyrazolinu mohou explodovat stopy nezreagovaných diazo sloučenin.
 Použití diazo sloučenin s kovovým katalyzátorem
Použití diazo sloučenin s kovovým katalyzátorem
Methyl phényldiazoacétate (en) a mnohé deriváty diazo blízkosti jsou prekurzory karbenového dárce akceptoru , které mohou být použity pro cyklopropanaci nebo vložit CH vazeb v organickém substrátu. Tyto reakce jsou katalyzovány dirhodium-tetraacetátem nebo některými jeho chirálními deriváty.
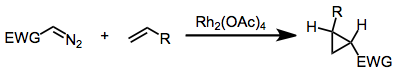 Použití volných karbenů
Použití volných karbenů
Z karbenů zdarma můžete využít k cyklopropanace reakce, ale jejich potenciál je omezen na to, protože jen málo může být vyroben pohodlně a téměř všichni jsou nestabilní, a to zejména vzhledem k jejich tendenci k dimerizaci (in) . Výjimkou jsou dihalogénocarbènes, jako dichlorokarben nebo difluorocarbene (v) , které jsou dostatečně stabilní a bude reagovat za vzniku dihalogen-cyklopropan geminální :

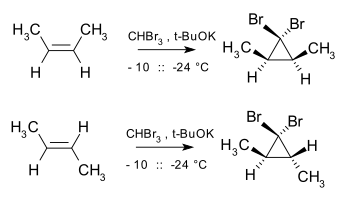
Tyto sloučeniny mohou být použity pro vytvoření allenů podle přesmyku Skattebøl (en) . Rozšíření kruhu Buchner (en) zahrnuje tvorbu stabilizované karbenem. Cyklopropanace je stereospecifická, protože přidání karbenu nebo karbenoidu k alkenu je formou chelotropní reakce , přičemž přidání je syn . Například dibromkarbonen (en) a cis -but-2-en produkují cis -2,3-dimethyl-1,1-dibromcyklopropan, zatímco trans izomer poskytuje pouze trans cyklopropan:
Z alkenů a ylidů
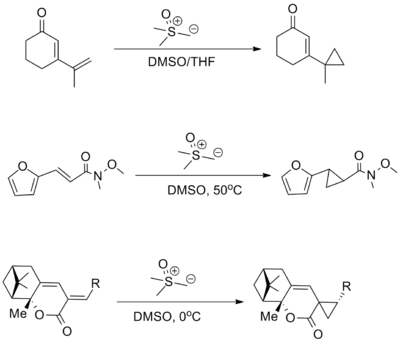
Cyklopropany se mohou vyrábět za použití ylidové síry reakcí Johnson-Corey-Chaykovského (en) , avšak tato metoda je do značné míry omezena na elektrony chudé alkeny, typicky karbonylové sloučeniny α, β-nenasycené.
Intramolekulární cyklizace
Cyklopropany lze získat různými intramolekulárními cyklizačními reakcemi . Jednoduchou metodou je použití primárních halogenalkanů nesoucích vhodně umístěné skupiny přitahující elektrony. Ošetření silnou bází vygeneruje karbanion, který bude cyklizovat způsobem 3-exo-trig (en) s vytěsněním halogenidu . Jako příklad lze uvést tvorbu cyklopropylkyanidu (en) a cyklopropylacetylenu (en) . Tento mechanismus také tvoří základ přeskupení Favorskii .
Příbuzným procesem je cyklizace 1,3-dibrompropanu (en) prostřednictvím Wurtzovy vazby . Ta byla použita pro první syntézu cyklopropanu od srpna Freund v roce 1881. Tato reakce se původně provádí za použití sodíku , ale výtěžek může být zlepšena použitím zinku místo .
BrCH 2 CH 2 CH 2 Br + 2 Na → (CH 2 ) 3 + 2 NaBrDalší přístupy
- Tyto Kulinkovich reakce tvoří cyclopropanols prostřednictvím reakcí mezi estery a Grignardovými činidly v přítomnosti alkoxidu titanu.
- Bingel reakce je speciální cyklopropanace reakce fullerenů .
- V přesmyku di-pi-methanu (en) , stimulace fotochemický způsobí přesmyk 1,4-dienů na formu vinylcyclopropanes. Ten pak může podstoupit přesmyk vinylcyklopropanu (en) .
- Mastné acyl-fosfolipid cyklopropan syntázy (en) katalyzuje cyklopropanací reakce v biologických systémech.
Biosyntéza
Zatímco cyklopropany jsou v biochemii relativně vzácné, v přírodě bylo identifikováno mnoho cyklopropanačních drah. Nejběžnější cesty zahrnují reakce uzavírání kruhů karbokationtů v terpenoidech . Mastné kyseliny cyklopropan (v) jsou odvozeny od napadení S -adénosylméthionine (SAM) na nenasycené mastné kyseliny .
Kyseliny 1-amino cyklopropan-1-karboxylové kyseliny , což je prekurzor na ethylen (což hraje roli hormonů v rostlinné říši) je přímo odvozen z S -méthylméthionine (SMM) intramolekulární nukleofilní skupiny malých a středních podniků 2 po kondenzaci s pyridoxal fosfátem .
Přímý přenos karbenem od diazoesters do alkenů bylo také dosaženo in vitro katalýza za použití varianty cytochromu P450 enzymu z Bacillus megaterium optimalizován řízené evoluce .
Poznámky a odkazy
- ( fr ) Tento článek je částečně nebo zcela převzat z článku Wikipedie v angličtině s názvem „ Cyclopropanation “ ( viz seznam autorů ) .
- Hélène Pellissier , „ Poslední vývoj v asymetrické cyklopropanaci “, Tetrahedron , sv. 64, č . 30–31,července 2008, str. 7041–7095 ( DOI 10.1016 / j.tet.2008.04.079 )
- (in) " carbenoids " Kompendium chemického názvosloví [ " Gold Book "], IUPAC 1997, opravené verze on-line (2006), 2 th ed.
- Bodo Fabisch a Mitchell, Terence N., „ Levná modifikace Simmons-Smithovy reakce: Tvorba brommethylzincbromidu podle studie NMR spektroskopie “, Journal of Organometallic Chemistry , sv. 269, n o 3,1984, str. 219-221 ( DOI 10.1016 / 0022-328X (84) 80305-8 )
- Georg Wittig a Wingler, Frank, „ Über methylenierte Metallhalogenide, IV. Cyclopropan-Bildung aus Olefinen mit Bis-halogenmethyl-zink “, Chemische Berichte , sv. 97, n o 8,1 st 08. 1964, str. 2146–2164 ( DOI 10.1002 / cber.19640970808 )
- J. Furukawa , Kawabata, N. a Nishimura, J., „ Syntéza cyklopropanů reakcí olefinů s dialkylzinkem a methylenjodidem “, Tetrahedron , sv. 24, n o 1,1968, str. 53–58 ( DOI 10.1016 / 0040-4020 (68) 89007-6 )
- AB Charette a A. Beauchemin , Simmons-Smith Cyclopropanation Reaction , sv. 58,2001( ISBN 978-0471264187 , DOI 10.1002 / 0471264180.or058.01 ) , s. 1
- David E. Lewis , „ Postižení, despotismus, odkysličení - od exilu po člena Akademie: Nikolai Matveevich Kizhner “, Angewandte Chemie International Edition , sv. 52, n o 45,4. listopadu 2013, str. 11704–11712 ( PMID 24123691 , DOI 10.1002 / anie.201303165 )
- NM Kishner, A. Zavadovskii, J. Russ. Phys. Chem. Soc. 43, 1132 (1911).
- R. J. Petersen a P. PS Skell , „ Fenylcyklopropan “, Org. Synth. , sv. 47,1967, str. 98 ( DOI 10.15227 / orgsyn.047.0098 )
- Robert J. Crawford a Anupama Mishra , „ Mechanismus tepelného rozkladu 1-pyrazolinů a jeho vztah k cyklopropanovým izomerizacím “, Journal of the American Chemical Society , sv. 88, n o 17,Září 1966, str. 3963–3969 ( DOI 10.1021 / ja00969a014 )
- Elena Muray , Ona Illa , José A. Castillo , Ángel Álvarez-Larena , José L. Bourdelande , Vicenç Branchadell a Rosa M. Ortuño , „ Fotolýza chirálních 1-pyrazolinů na cyklopropany: mechanismus a stereospecifičnost “, The Journal of Organic Chemistry , sv. 68, N O 12Červen 2003, str. 4906–4911 ( PMID 12790598 , DOI 10.1021 / jo0342471 )
- Davies, HML a Morton, D., „ Hlavní zásady pro selektivní a stereoselektivní intermolekulární C-H funkcionalizaci pomocí donoru / akceptoru Rhodium Carbenes “, Chemical Society Reviews , sv. 40, n O 4,2011, str. 1857–1869 ( DOI 10.1039 / C0CS00217H )
- Huw ML Davies a Wen-hao Hu, Dong Xing, „ methylfenyldiazoacetát “, EEROS ,2015, str. 1–10 ( ISBN 9780470842898 , DOI 10.1002 / 047084289X.rn00444.pub2 )
- Hélène Lebel , Marcoux, Jean-François, Molinaro, Carmela a Charette, André B., „ Stereoselective Cyclopropanation Reactions “, Chemical Reviews , sv. 103, n O 4,1 st 04. 2003, str. 977–1050 ( PMID 12683775 , DOI 10.1021 / cr010007e )
- Michał Fedoryński , „ Syntézy dihalocyklopropanů a jejich použití v organické syntéze “, Chemical Reviews , sv. 103, n O 4,1 st 04. 2003, str. 1099–1132 ( PMID 12683778 , DOI 10.1021 / cr0100087 )
- Skell, PS a Garner, AY, „ Stereochemistry of Carbene-Olefin Reactions. Reakce dibromokarbenu s cis- a trans-2-buteny “, Journal of the American Chemical Society , sv. 78, n o 14,1956, str. 3409–3411 ( DOI 10.1021 / ja01595a040 )
- Li, A.-H., Dai, L.-X. a Aggarwal, VK, „ Asymetric Ylide Reactions: Epoxidation, Cyclopropanation, Aziridination, Olefination, and Rearrangement “, Chemical Reviews , sv. 97, n O 6,1997, str. 2341 ( DOI 10.1021 / cr960411r )
- MJ Schlatter , Cyclopropyl Kyanide , Org. Synth. 23 , sb. „let. 3 ",1943, 20 str. , str. 223.
- Cyklopropylacetylen , Org. Synth. 77 , sb. „let. ",2000, 231 s.
- (de) August Freund , „ Über Trimethylen “ [„On Trimethylene“], Journal für praktische Chemie , sv. 26, n o 1,1881, str. 625–635 ( DOI 10.1002 / prac.18820260125 , číst online )
- (De) G. Gustavson , „ Ueber eine neue Darstellungsmethode des Trimethylens “ [„O nové metodě reprezentace trimethylenu“], J. Prakt. Chem. , sv. 36,1887, str. 300–305 ( DOI 10.1002 / prac.18870360127 , číst online )
- (in) " di-π methan přesmyku ," Kompendium chemického názvosloví [ " Gold Book "], IUPAC 1997, opravené verze on-line (2006), 2 th ed.
- Ludger A. Wessjohann Wolfgang Brandt a Thies Thiemann , „ Biosyntéza a metabolismus cyklopropanových kruhů v přírodních sloučeninách “ Chemical Reviews , sv. 103, n O 4,Dubna 2003, str. 1625–1648 ( PMID 12683792 , DOI 10.1021 / cr0100188 )
- PS Coelho , EM Brustad , A. Kannan a FH Arnold , „ Cyklopropanace olefinů pomocí přenosu karbenu katalyzovaná enzymy Engineered Cytochrome P450 Enzymes “, Science , sv. 339, n O 6117,20. prosince 2012, str. 307–310 ( PMID 23258409 , DOI 10.1126 / science.1231434 , Bibcode 2013Sci ... 339..307C , číst online )