Prolin
| Prolin | |
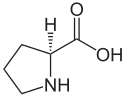 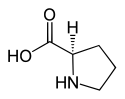 L nebo S (-) - prolin a D nebo R (+) - prolin |
|
| Identifikace | |
|---|---|
| Název IUPAC | kyselina pyrrolidin -2- karboxylové |
| Synonyma |
P, Pro |
| N O CAS |
(racemický) (L) neboS(-) (D) neboR(+) |
| Ne o ECHA | 100 009 264 |
| Ne o EC | 205-702-2 (L) |
| FEMA | 3319 |
| ÚSMĚVY |
[H] N1CCCC1C (O) = O , |
| InChI |
InChI: InChI = 1 / C5H9NO2 / c7-5 (8) 4-2-1-3-6-4 / h4,6H, 1-3H2, (H, 7,8) |
| Chemické vlastnosti | |
| Hrubý vzorec |
C 5 H 9 N O 2 [izomery] |
| Molární hmotnost | 115,1305 ± 0,0054 g / mol C 52,16%, H 7,88%, N 12,17%, O 27,79%, |
| pKa | 1,95 - 10,64 |
| Biochemické vlastnosti | |
| Kodony | CCA , CCU , CCG , CCC |
| izoelektrické pH | 6.30 |
| Esenciální aminokyselina | Ne |
| Výskyt u obratlovců | 5,0% |
| Opatření | |
| WHMIS | |
|
Nekontrolovaný produktTento produkt není kontrolován podle klasifikačních kritérií WHMIS. |
|
| Jednotky SI a STP, pokud není uvedeno jinak. | |
Prolin (Zkratky IUPAC - IUBMB : Pro a P ) je kyselý α-aminokyseliny , jehož enantiomer L je jedním z 22 proteinogenních aminokyselin , kódované na RNA od kodonů CCU, CCC, CCA a CCG. Je to jediný proteinogenní aminokyseliny, která má sekundární a non- primárního aminu , což mu dává zvláštní geometrii, která má tendenci přerušit sekundární struktury z proteinů, jako jsou například alfa helixy a beta listy .
Prolin tvoří nepolární zbytky, které při polymeraci mohou tvořit různé typy proteinů v rodině zvané polyproliny .
Zdrojem prolinové spirály může být přítomnost mnoha prolinových zbytků; to je zejména případ kolagenu . Prolinový cyklus je téměř plochý. To lze ukázat zvážením úhlů vazby v tomto kruhu.
Ve zvířecím světě
Prolin se podílí zejména na syntéze kolagenu, který má sekvenci ( Gly – Pro– Hyp ) n a jizvení.
Ve světě rostlin
Prolin se podílí na správném klíčení semen, kvetení a dalších fázích vývoje rostlin.
Akumulace prolinů byla pozorována u mnoha druhů rostlin, když byly vystaveny různým typům environmentálních stresů.
Rostoucí množství důkazů podporuje pozitivní korelaci mezi těmito akumulacemi a metabolickým řízením těchto stresů rostlinami. Má roli osmolytu, ale je také chelátorem kovů a má antioxidační vlastnosti. "Aplikuje se exogenně a v nízkých dávkách, zlepšuje toleranci stresu u rostlin," ale několik propojek také zaznamenalo nežádoucí účinky při vyšších dávkách.
Data
- Van der Waalsova síla : 90
- pK1 (a-COOH): 1,95
- pK2 (aN-H): 10,64
Prolin obsahuje ve své molekule cyklickou funkci sekundárního aminu.
Další aminokyselina, hydroxyprolin , je odvozena od prolin 4- hydroxylací .
Poznámky a odkazy
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (in) Francis A. Carey, " Tabulka pK a hodnoty pH " , v Ústavu chemie na University of Calgary , 2014(zpřístupněno 26. července 2015 )
- (in) Mr. Beals, L. Gross, S. Harrell, „ Amino Acid Frequency “ na Institutu pro environmentální modelování (ITSH) na University of Tennessee (přístup 26. července 2015 )
- „ Prolin (l-) “ v databázi chemických látek Reptox z CSST (quebecká organizace odpovědná za bezpečnost a ochranu zdraví při práci), přístup k 25. dubnu 2009
- J. Behre, R. Voigt, I. Althöfer, S. Schuster: K evolučnímu významu velikosti a rovinnosti prolinového kruhu . Naturwissenschaften 99 (2012) 789-799.
- (en) Mudasir Irfan Dar , Mohd Irfan Naikoo , Farha Rehman , Fauzia Naushin a Fareed Ahmad Khan , „Prolinová akumulace v rostlinách: role v toleranci stresu a rozvoji rostlin“ , v Noushina Iqbal, Rahat Nazar a Nafees A Khan, osmolyty a aklimatizace rostlin na měnící se prostředí: Emerging Omics Technologies , New Delhi, Springer,2016( ISBN 978-81-322-2615-4 a 978-81-322-2616-1 , DOI 10.1007 / 978-81-322-2616-1_9 ) , s. 155-166.
Podívejte se také
Bibliografie
- Ali Q, Ashraf M, Athar HUR (2007) Exogenně aplikovaný prolin v různých stadiích růstu zvyšuje růst dvou kultivarů kukuřice pěstovaných za podmínek nedostatku vody. Pak J Bot 39: 1133-1144
- (en) Patrick Armengaud , Laurent Thiery , Nathalie Buhot a Ghislaine Grenier-de March , „ Transkripční regulace biosyntézy prolinů v Medicago truncatula odhaluje vývojové a environmentální specifické rysy “ , Physiologia Plantarum , sv. 120, n o 3,Březen 2004, str. 442–450 ( ISSN 0031-9317 a 1399-3054 , DOI 10.1111 / j.0031-9317.2004.00251.x , číst online , přístup k 21. říjnu 2020 )
- (en) M. Ashraf a MR Foolad , „ Role glycin betainu a prolin při zlepšování odolnosti rostlin proti abiotickému stresu “ , Environmental and Experimental Botany , sv. 59, n O 2Březen 2007, str. 206–216 ( DOI 10.1016 / j.envexpbot.2005.12.006 , číst online , přístup k 21. říjnu 2020 )