Agregace proteinů
Agregace proteinů (nebo agregace / aglomerace protein ) je biologický jev, při kterém proteiny špatně složené agregát (to znamená, že se hromadí a jsou seskupeny), aby uvnitř jako extracelulární. Tyto proteinové agregáty často korelují s onemocněním . Ve skutečnosti se proteinové agregáty podílejí na celé řadě nemocí, které se nazývají amyloidóza , včetně ALS , Alzheimerovy a Parkinsonovy choroby a prionových onemocnění .
Po jejich syntéze mají proteiny ve zvyku skládat se do konkrétní trojrozměrné konformace, která je pro ně termodynamicky nejpříznivější: jejich nativní stav . Tento skládací proces je řízen hydrofobním účinkem , což je tendence hydrofobních částí proteinu, aby se snaží chránit z hydrofilního prostředí z buňky od vrtání otvorů pod uvnitř proteinu. Exteriér proteinu je tedy typicky hydrofilní, zatímco jeho vnitřek je typicky hydrofobní.
Proteinové struktury jsou stabilizovány nekovalentními vazbami a disulfidovými vazbami spojujícími dva cysteinové zbytky . Nekovalentní interakce zahrnují iontové vazby a slabé van der Waalsovy interakce . Iontové interakce se tvoří mezi aniontem a kationtem a tvoří solné můstky, které pomáhají stabilizovat protein. Van der Waalsovy interakce zahrnují nepolární interakce ( Londýnské síly ) a polární interakce ( vodíkové vazby , mezimolekulární síly ). Ty hrají důležitou roli v sekundární struktuře proteinů, jako je tvorba alfa šroubovice nebo beta listu , stejně jako v jejich terciární struktuře . Interakce mezi aminokyselinovými zbytky v daném proteinu jsou velmi důležité pro konečnou strukturu tohoto proteinu.
Pokud dojde ke změnám v nekovalentních interakcích, jak může dojít ze změny v aminokyselinové sekvenci, je pravděpodobné, že se protein špatně nebo vůbec nesloží. V tomto typu situace, pokud buňka nepomůže proteinům napravit tento defekt skládání nebo je zničit, mohou se shlukovat dohromady a v tomto procesu mohou exponované hydrofobní části proteinů interagovat s exponovanými hydrofobními částmi. bílkoviny. Mohou se tvořit tři hlavní typy proteinových agregátů: amorfní agregáty, oligomery a amyloidní fibrily .
Příčiny
Agregace proteinů může probíhat z několika příčin. Existují čtyři třídy, do kterých lze tyto příčiny kategorizovat, které jsou podrobně popsány níže.
Mutace
Tyto mutace se vyskytují v pořadí z DNA, může, ale nemusí mít vliv na aminokyselinová sekvence proteinu. Pokud je ovlivněna sekvence, může odlišná aminokyselina měnit interakce mezi postranními řetězci , což ovlivňuje skládání proteinu. To může vést k expozici hydrofobních oblastí proteinu, které agregují se stejným nesprávně složeným nebo rozloženým proteinem nebo s jiným proteinem.
Kromě mutací ovlivňujících samotné proteiny může být agregace proteinů způsobena také nepřímo mutacemi vyskytujícími se v proteinech během regulačních drah, jako je skládací dráha ( chaperony ) nebo dráha ubikvitin-proteazom ( ubikvitinové ligázy ). Chaperony pomáhají skládat proteiny tím, že jim poskytují bezpečné prostředí pro skládání. Ubikvitinové ligázy cílí na proteiny, které mají být degradovány modifikací ubikvitinu .
Poruchy během syntézy bílkovin
Agregace proteinů může být způsobena problémy, které se vyskytnou během transkripce nebo translace . Během transkripce je DNA kopírována do mRNA , čímž se vytvoří pre-mRNA vlákno, které prochází post-transkripčními modifikacemi za vzniku mRNA. Během translace pomáhají ribozomy a RNA překládat sekvenci mRNA na sekvenci aminokyselin. Pokud během některého z těchto dvou kroků dojde k defektům, které produkují nesprávný řetězec mRNA nebo sekvenci aminokyselin, způsobí to nesprávné poskládání proteinu, což vede k agregaci proteinu.
Stres prostředí
Stresy prostředí, jako jsou extrémní teploty nebo pH nebo oxidační stres, mohou také vést k agregaci proteinů. Příkladem onemocnění způsobeného tímto typem stresu je kryoglobulinémie .
Extrémní teploty mohou oslabit a destabilizovat nekovalentní vazby mezi aminokyselinovými zbytky. PH mimo rozsah pH daného proteinu mohou změnit protonační stav aminokyselin, což může zvýšit nebo snížit nekovalentní interakce. Může také vést k méně stabilní vazbě, a tedy k neskládání proteinu.
Oxidační stres může být způsoben radikály, jako je ROS . Tyto nestabilní radikály mohou napadat aminokyselinové zbytky, což vede k oxidaci postranních řetězců (jako jsou aromatické postranní řetězce nebo methioninové postranní řetězce ) a / nebo štěpení polypeptidových vazeb. To může ovlivnit nekovalentní vazby, které drží protein ve správném tvaru, což může způsobit destabilizaci proteinu, a tím zabránit skládání proteinu.
Stárnutí
Buňky mají mechanismy, které mohou znovu skládat nebo rozkládat proteinové agregáty. Jak však buňky stárnou, tyto kontrolní mechanismy jsou méně účinné a buňka je méně schopná převzít zodpovědnost za tyto agregáty.
Hypotéza, podle níž je agregace proteinů následným procesem stárnutí, je nyní testovatelná, protože se vyvíjejí určité modely opožděného stárnutí. Pokud by vývoj proteinových agregátů byl proces nezávislý na stárnutí, zpomalení tohoto stárnutí by nemělo žádný vliv na rychlost proteotoxicity v průběhu času. Pokud by však stárnutí bylo spojeno s poklesem aktivity ochranných mechanismů proti proteotoxicitě, modely zpomaleného stárnutí by ukázaly snížení agregace a proteotoxicity. Za účelem vyřešení tohoto problému bylo provedeno několik testů toxicity na hlístici C. elegans . Tyto studie ukázaly, že snížení signální aktivity inzulínu / IGF, dobře známé regulační dráhy stárnutí, chrání před agregací toxických proteinů spojenou s neurodegenerací. Platnost tohoto přístupu byla testována a potvrzena u savců , protože snížení aktivity signální dráhy IGF-1 chránilo studované myši s Alzheimerovou chorobou před projevy chování a poruch souvisejících s tímto onemocněním.
Umístění agregátů
Několik studií ukázalo, že buněčné reakce na agregaci proteinů jsou dobře regulovány a organizovány. Agregáty proteinů jsou lokalizovány ve specifických oblastech buňky a výzkum se zaměřil na tyto oblasti v prokaryotech ( E. coli ) a eukaryotech ( kvasinky , buňky savců).
V bakteriích
Agregáty bakterií se nacházejí asymetricky na jednom z pólů buňky, „ starším pólu “. Po buněčném dělení získává dceřiná buňka obsahující přední pól agregát bílkovin a roste pomaleji než dceřiná buňka bez agregátu. To představuje mechanismus přirozeného výběru ke snížení agregátů proteinů v bakteriální populaci.
V droždí
Většina proteinových agregátů v kvasinkových buňkách má svou skládací vadu korigovanou chaperony. U některých agregátů však nemusí být opravena jejich skládací vada, například proteiny poškozené oxidačním stresem nebo proteiny určené k degradaci. Místo toho je lze přesměrovat do jednoho ze dvou oddílů: oddělení JUxtaNuclear Quality-Control ( JUNQ ) poblíž jaderné membrány a Insolubile Protein Deposit nebo IPOD v angličtině) poblíž vakuoly v kvasinkových buňkách. Agregáty proteinů přecházejí na JUNQ, když jsou ubikvitizované a jsou určeny k degradaci, zatímco shlukové a nerozpustné proteiny přecházejí na IPOD pro delší skladování. Výsledky ukázaly, že proteiny v tomto místě lze odstranit autofagií . Tyto dvě možnosti spolupracují takovým způsobem, že proteiny mají tendenci přejít na IPOD, když je proteazomová dráha přetížena.
V savčích buňkách
V savčích buňkách se tyto proteinové agregáty nazývají „agresomy“ a vytvářejí se, když je buňka nemocná. K tomu dochází, protože agregáty mají tendenci se tvořit, když jsou v buňce přítomny heterologní proteiny, což může nastat, když je buňka mutována. Ubikvitin ligáza E3 je schopna rozpoznat špatně složené proteiny a ubikvitinovat je. HDAC6 pak může vázat ubikvitin a motorový protein dynein k transportu „označených“ agregátů do centrozomu . Jakmile se tam nacházejí, shlukují se do koule, která obklopuje centrosom. Poskytují chaperony a proteazomy a aktivují autofagii.
Odstranění kameniva
V buňce jsou dva hlavní systémy „kontroly kvality“ odpovědné za odstraňování proteinových agregátů. Špatně složené proteiny mohou být znovu složeny bi-chaperonovým systémem nebo degradovány ubikvitin-proteazomovým systémem nebo autofagií.
Skládací
Bi-chaperonový systém používá chaperony Hsp70 (DnaK-DnaJ-GrpE v E. coli a Ssa1-Ydj1 / Sis1-Sse1 / Fe1 v kvasinkách) a Hsp100 (ClpB v E. coli a Hsp104 v kvasinkách) k dezagregaci a neo složit proteiny.
Hsp70 interaguje s agregáty proteinů a rekrutuje Hsp100. Hsp70 stabilizuje aktivovaný Hsp100. Hsp100 mají aromatické pórů smyčky použity pro řezání závitů aktivity rozmotat jednotlivých polypeptidů. Tato vláknová aktivita může být zahájena na N-konci , C-konci nebo jinde ve středu polypeptidu . Polypeptid podléhá translokaci Hsp100 v řadě kroků, z nichž každý spotřebovává ATP . Polypeptid se neskládá a poté neo-skládá ani sám, ani pomocí proteinů tepelného šoku ( proteiny tepelného šoku ).
Degradace
Špatně poskládané proteiny lze odstranit systémem ubikvitin-proteazom. Skládá se z dráhy E1-E2-E3, která ubikvitinuje proteiny, aby je určila k degradaci. V eukaryotech jsou proteiny degradovány proteasomem 26S. V savčích buňkách cílí na Hsp70 vázané proteiny E3 ligáza a Hsp70 interagující karboxyterminální protein. V kvasinkách mají E3 Doa10 a Hrd1 ligázy podobné funkce na proteinech endoplazmatického retikula :

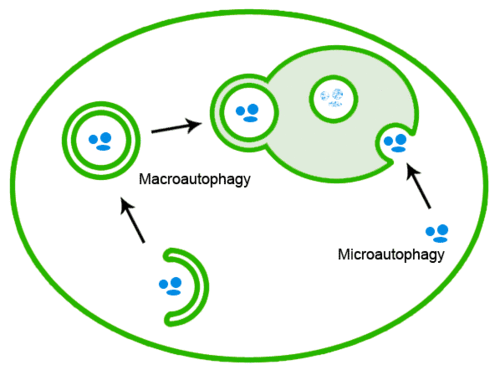
Špatně poskládané proteiny lze odstranit také autofagií, při které jsou agregáty proteinů transportovány do lysozomu :
Toxicita
Ačkoli se dospělo k názoru, že agregáty zralých proteinů jsou samy o sobě toxické, nedávné výsledky naznačují, že ve skutečnosti jsou nejvíce toxické nezralé agregáty proteinů. Hydrofobní skupiny v těchto agregátech mohou interagovat s jinými složkami buňky a poškodit je. Předpokládá se, že toxicita proteinových agregátů souvisí s mechanismy sekvestrace buněčných složek, s tvorbou ROS, s vazbou na specifické receptory v membráně nebo s narušením membrán. Genetický test určil, že druhy s vyšší molekulovou hmotností jsou odpovědné za permeabilizaci membrány. Je známo, že proteinové agregáty mohou in vitro destabilizovat umělé lipidové dvojvrstvy, což vede k permeabilizaci membrány.
Podívejte se také
Poznámky
- (fr) Tento článek je částečně nebo zcela převzat z článku anglické Wikipedie s názvem „ Agregace proteinů “ ( viz seznam autorů ) .
Reference
- Adriano Aguzzi a Tracy O'Connor , „ Nemoci agregace proteinů: patogenita a terapeutické perspektivy “, Nature Reviews. Drug Discovery , sv. 9, n o 3,března 2010, str. 237–248 ( ISSN 1474-1784 , PMID 20190788 , DOI 10.1038 / nrd3050 , číst online , přístup ke dni 30. října 2017 )
- Fernanda G. De Felice , Marcelo NN Vieira , M. Nazareth L. Meirelles a Ludmilla A. Morozova-Roche , „ Tvorba agregátů amyloidů z lidského lysozymu a jeho variant souvisejících s onemocněním pomocí hydrostatického tlaku “, časopis FASEB: oficiální publikace Federace amerických společností pro experimentální biologii , sv. 18, n o 10,Červenec 2004, str. 1099–1101 ( ISSN 1530-6860 , PMID 15155566 , DOI 10.1096 / fj.03-1072fje , číst online , přístup ke dni 30. října 2017 )
- Rudolph E. Tanzi a Lars Bertram , „ Dvacet let hypotézy amyloidů Alzheimerovy choroby: genetická perspektiva “, Cell , sv. 120, n O 4,25. února 2005, str. 545–555 ( ISSN 0092-8674 , PMID 15734686 , DOI 10.1016 / j.cell.2005.02.008 , číst online , přístup ke dni 30. října 2017 )
- MJ Gething a J. Sambrook , „ Protein skládající se v buňce “, Nature , sv. 355, n o 63552. ledna 1992, str. 33–45 ( ISSN 0028-0836 , PMID 1731198 , DOI 10.1038 / 355033a0 , číst online , přístup ke dni 30. října 2017 )
- (in) David L. Cox a Michael Nelson , Lehninger Principles of Biochemistry , New York, WH Freeman,2013( ISBN 978-1-4292-3414-6 ) , str. 143
- Sarah J Shoesmith Berke a Henry L. Paulson , „ Agregace proteinů a dráha ubikvitinového proteazomu: získání UPPer ruky na neurodegeneraci “, Current Opinion in Genetics & Development , sv. 13, n o 3,1 st 06. 2003, str. 253–261 ( DOI 10.1016 / S0959-437X (03) 00053-4 , číst online , přístup ke dni 30. října 2017 )
- (in) Robert F. Weaver, Molekulární biologie , New York, McGraw-Hill,2012( ISBN 978-0-07-352532-7 ) , str. 122-156; 523-600
- Jens Tyedmers , Axel Mogk a Bernd Bukau , „ Buněčné strategie pro řízení agregace proteinů “, Nature Reviews. Molecular Cell Biology , sv. 11, n o 11,listopadu 2010, str. 777–788 ( ISSN 1471-0080 , PMID 20944667 , DOI 10.1038 / nrm2993 , číst online , přístup ke dni 30. října 2017 )
- (in) ER Stadtman a RL Levine , „ Oxidace volných aminokyselin a zbytků aminokyselin v proteinech zprostředkovaná volnými radikály “ , Amino Acids , sv. 25 Žádné kosti 3-4,1 st 12. 2003, str. 207-218 ( ISSN 0939 do 4451 a 1438 až 2199 , DOI 10,1007 / s00726-003-0011-2 , číst on-line , přístupný 30.října 2017 )
- James F. Morley , Heather R. Brignull , Jill J. Weyers a Richard I. Morimoto , „ Prahová hodnota pro agregaci proteinů s polyglutaminovou expanzí a buněčnou toxicitu je dynamická a ovlivněna stárnutím Caenorhabditis elegans “, Proceedings of the National Academy of Sciences of the United States of America , sv. 99, n o 16,6. srpna 2002, str. 10417–10422 ( ISSN 0027-8424 , PMID 12122205 , DOI 10.1073 / pnas.152161099 , číst online , přístup k 30. říjnu 2017 )
- Natalia G. Bednarska , Joost Schymkowitz , Frederic Rousseau a Johan Van Eldere , „ Agregace proteinů v bakteriích: tenká hranice mezi funkčností a toxicitou “, Microbiology (Reading, England) , sv. 159, n o Pt 9,září 2013, str. 1795–1806 ( ISSN 1465-2080 , PMID 23894132 , DOI 10,1099 / mic.0.069575-0 , číst online , přístup k 30. říjnu 2017 )
- Mari Takalo , Antero Salminen , Hilkka Soininen a Mikko Hiltunen , „ Mechanismy agregace a degradace proteinů u neurodegenerativních onemocnění “, American Journal of Neurodegenerative Disease , sv. 2, n O 1,2013, str. 1–14 ( ISSN 2165-591X , PMID 23516262 , PMCID PMC3601466 , číst online , přístup k 30. říjnu 2017 )
- (in) Rafael Garcia-Mata , Ya-Sheng Gao a Elizabeth Sztul , „ Hassles with Takeing Out the Garbage: Aggravating Aggresomes “ , Traffic , sv. 3, n o 6,1 st 06. 2002, str. 388–396 ( ISSN 1600-0854 , DOI 10.1034 / j.1600-0854.2002.30602.x , číst online , přístup k 30. říjnu 2017 )
- (in) Niels Gregersen Lars Bolund a Peter Bross , „ Špatné skládání, agregace a zhoršení nemoci “ , Molecular Biotechnology , sv. 31, n O 21 st 10. 2005, str. 141–150 ( ISSN 1073-6085 a 1559-0305 , DOI 10,1385 / MB: 31: 2: 141 , číst online , přístup ke dni 30. října 2017 )
- Axel Mogk , Eva Kummer a Bernd Bukau , „ Spolupráce chaperonových strojů Hsp70 a Hsp100 při disagregaci proteinů “, Frontiers in Molecular Biosciences , sv. 2,2015, str. 22 ( ISSN 2296-889X , PMID 26042222 , PMCID PMC4436881 , DOI 10.3389 / fmolb.2015.00022 , číst online , přístup k 30. říjnu 2017 )
- Krzysztof Liberek , Agnieszka Lewandowska a Szymon Zietkiewicz , „ Chaperony pro kontrolu disagregace proteinů “, The EMBO journal , sv. 27, n O 223. ledna 2008, str. 328–335 ( ISSN 1460-2075 , PMID 18216875 , PMCID PMC2234349 , DOI 10.1038 / sj.emboj.7601970 , číst online , přístup ke dni 30. října 2017 )
- Bryan Chen , Marco Retzlaff , Thomas Roos a Judith Frydman , „ Buněčné strategie kontroly kvality bílkovin “, Cold Spring Harbor Perspectives in Biology , sv. 3, n o 8,1 st 08. 2011, a004374 ( ISSN 1943-0264 , PMID 21746797 , PMCID PMC3140689 , DOI 10.1101 / cshperspect.a004374 , číst online , přístup ke dni 30. října 2017 )
- YJ Zhu , H. Lin a R. Lal , „ Čerstvý a nefibrilární amyloidový beta protein (1–40) indukuje rychlou buněčnou degeneraci ve starých lidských fibroblastech: důkazy o buněčné toxicitě zprostředkované AbetaP kanálem “, časopis FASEB: oficiální publikace Federace amerických společností pro experimentální biologii , sv. 14, n o 9,Červen 2000, str. 1244-1254 ( ISSN 0892 - 6638 , PMID 10834946 , číst on-line , přístupný 30.října 2017 )
- C. Nilsberth , A. Westlind-Danielsson , CB Eckman a MM Condron , „ „ Arktická “mutace APP (E693G) způsobuje Alzheimerovu chorobu zvýšenou tvorbou protofibril Abeta “, Nature Neuroscience , sv. 4, n o 9,Září 2001, str. 887–893 ( ISSN 1097-6256 , PMID 11528419 , DOI 10.1038 / nn0901-887 , číst online , přístup ke dni 30. října 2017 )
- (in) Claudio Soto , „ Rozvíjení úlohy nesprávného skládání bílkovin u neurodegenerativních onemocnění “ , Nature Reviews Neuroscience , sv. 4, n o 1,ledna 2003, str. 49–60 ( ISSN 1471-003X , DOI 10.1038 / nrn1007 , číst online , přístup ke dni 30. října 2017 )
- Patrick Flagmeier , Suman De , David C. Wirthensohn a Steven F. Lee , „ Ultrasensitivní měření přítoku Ca (2+) do lipidových váčků indukovaných agregáty proteinů “, Angewandte Chemie (mezinárodní vydání v angličtině) , sv. 56, n o 27,26. června 2017, str. 7750–7754 ( ISSN 1521-3773 , PMID 28474754 , PMCID PMC5615231 , DOI 10.1002 / anie.201700966 , číst online , přístup k 30. říjnu 2017 )
externí odkazy
- (en) Folding @ Home Nápověda k dekódování skládání proteinů.
- (en) Rosetta @ Home Pomáhá při predikci proteinových struktur a komplexů.