Myasthenia gravis
Myasthenia gravis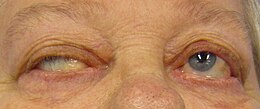 Ptóza u osoby s myasthenia gravis, která se snaží otevřít oči.
Ptóza u osoby s myasthenia gravis, která se snaží otevřít oči.
| Specialita | Neurologie |
|---|
| ICD - 10 | G70.0 |
|---|---|
| CIM - 9 | 358,0 |
| OMIM | 254200 |
| Nemoci DB | 8460 |
| MedlinePlus | 000712 |
| eMedicína | 1171206, 793136, 261815 a 1216417 |
| eMedicína |
neuro / 232 vznik / 325 (pohotovost), med / 3260 (těhotenství), oph / 263 (oko) |
| Pletivo | D009157 |
| Lék | Pyridostigmin , neostigmin , cyklosporin , cyklofosfamid , prednison , azathioprin , rituximab , ekulizumab , mykofenolát mofetil ( d ) , prednisolon , takrolimus , distigmin ( d ) a pyridostigmin |
| UK pacient | Myasthenia-gravis-pro |
Tyto gravis (řecký μύς „svalů“ a ἀσθένεια „slabost“), v latina gravis je neuromuskulární onemocnění autoimunitní chronické , které se projevují v různé míře podle slabost a únava nadměrné z příčně pruhovaného kosterního svalu , C, který se, ty, které jsou aktivovány dobrovolně. Za své jméno vděčí německému neurologovi Friedrichovi Jollymu (1844-1904) a má také stejnojmenné jméno : Erb - Goldflamova choroba , na počest dvou lékařů, kteří poskytli nejúplnější popis. To je způsobeno tím, protilátky cirkulující, že ve více než tři ze čtyř případů, cílové receptory na acetylcholinu v neuromuskulárních spojeních , čímž inhibují excitační účinek tohoto neurotransmiteru .
Historický
Pravděpodobně to byl Thomas Willis, kdo jako první popsal pacienta s myasthenia gravis. Jolly pojmenuje onemocnění zavedením termínu „ myasthenia gravis pseudoparalytica “ a zdůrazňuje elektrofyziologické zhoršení. Mary Walker navrhla v roce 1934 léčbu fyzostigminem . Abnormality v brzlíku ve vztahu k MG jsou známé, a tymektomie praktikována od začátku XX th století , před porozumění patofyziologie a identifikace autoimunitní geneze.
Epidemiologie
Jeho prevalence se pohybuje od 5 do 10 na 100 000 obyvatel a jeho výskyt mezi 2 a 20 za rok a na milion obyvatel v závislosti na sérii. Může se vyskytnout v jakémkoli věku, jeho nejvyšší výskyt se týká věkové skupiny 20 až 30 let. Poměr pohlaví pacientů, 3 ženy ke 2 mužům, se liší podle věkové skupiny (2 ženy k 1 muži u osob mladších 50 let, 1 žena k 1 muži u osob starších 50 let). V zásadě sporadické onemocnění jsou rodinné formy výjimečné.
Patofyziologie
Domnělý patofyziologie myasthenia gravis se skládá z poškození membránových proteinů postsynaptické v neuromuskulárním spojení podle cirkulující autoprotilátky . Primární protilátka cíl uzavřeno acetylcholinových receptorů (a neurotransmiter ), působí jako kompetitivní inhibitor z acetylcholinu a urychlit degradaci receptoru antigenní modulace. To má za následek zvýšení počtu acetylcholinových kvant, potřebných k produkci depolarizace postsynaptické membrány, což vede k rychlejšímu a hlubšímu vyčerpání presynaptických zásob acetylcholinu a klinicky vede ke svalové únavě.
Ve střednědobém horizontu může přítomnost těchto protilátek vyvolat prostřednictvím aktivace systému komplementu anatomické změny postsynaptické membrány, což dále snižuje její excitabilitu. V této fázi, v nejtěžších formách, může dojít k trvalému deficitu.
S výjimkou D-penicilaminu a alogenní transplantace kostní dřeně nebylo identifikováno žádné exogenní činidlo podporující nástup myasthenia gravis. Existuje mírná genetická predispozice, zejména skupiny HLA B8 (en) a DR3 (en) s DR1 (en) specifičtějšími pro oční myasthenia gravis. Mnoho dalších autoprotilátek bylo nedávno identifikováno jako patogeny, všechny zaměřené na složku postsynaptické membrány: protilátky anti-MuSK ( svalová specifická kináza ), protilátky anti-agrin, protilátky proti LRP4. Je prokázána role brzlíku v patogenezi. Je sídlem dozrávání T lymfocytů . Při jejich stimulaci se B lymfocyty transformují na plazmatické buňky vylučující protilátky.
Klinické projevy
Klinické příznaky lze popsat následovně:
kardinálním příznakem a nezbytným pro diagnózu je únava při námaze. Příznaky jsou proto kolísavé, zesilují se námahou a zlepšují se v klidu. Často jsou výraznější na konci dne a mohou se zhoršovat ve stresových situacích: infekce, chirurgický zákrok, teplo… Nakonec tedy může být klinické vyšetření striktně normální nebo málo narušené, zátěžové testy pak umožňují odhalení anomálií.
Lokalizace svalu a výsledné příznaky jsou různé:
- v 50% případů je počáteční stížností ptóza , diplopie nebo obojí. Tyto příznaky jsou často kolísavé, obvykle se objevují nebo zhoršují na konci dne nebo při čtení nebo řízení vozidla. Toto je stížnost, která nejvíce evokuje diagnózu a umožňuje jediný konkrétní klinický diagnostický test. Je skutečně charakteristický výskyt ptózy s oftalmoparézou (poklesnutím víček s obtížemi konvergence) při excentrické fixaci pohledu na několik minut u předem asymptomatického pacienta. U symptomatického pacienta je test kostky ledu (zlepšení ptózy po umístění ledu na několik minut na symptomatické víčko) méně specifický, ale velmi evokující;
- ve 20% případů se původní stížnost týká únavy končetin, nejčastěji v jejích proximálních částech, což může vést k diagnóze myopatie. Opakované zátěžové testy mohou odhalit segmentovou únavu, ale nejsou příliš konkrétní;
- v 10% případů se počáteční stížnost skládá z izolované asténie (generalizovaná únava, často zaměňovaná se skutečnou svalovou slabostí), která by neměla naznačovat diagnózu jako léčbu první linie, pokud lékař neprokáže skutečnou svalovou slabost a nedovolí únavu být v popředí. Toto je nejvíce nespecifická stížnost a klinické testy jsou málo užitečné;
- poměrně zřídka budou počáteční stížnosti spočívat v kolísavých poruchách žvýkání, polykání nebo slabosti extenzorů krku;
- pozorování globálního okulo-cefalického postižení produkujícího „myastenickou facii“ je vzácné, ale velmi evokativní (asymetrická palpebrální ptóza, klesající spodní ret, vymazání vrásek na čele, možné vnější poruchy oka a slabost extenzorů krku). Kolísající povaha této facie umožňuje odlišit ji od mnoha dalších příčin diflegie obličeje a potvrdit diagnózu.
Podle definice jsou příznaky pouze motorické a smyslové stížnosti chybí. V důsledku nadměrného kompenzačního úsilí však může pacient upozornit na citlivé, bolestivé potíže (myalgie, artralgie, parestézie) vedoucí k diagnóze revmatické patologie, myopatie, metabolické poruchy, polyneuropatie nebo myelopatie.
Při vyšetření jsou myotatické reflexy normální a atrofie je pozorována pouze u těžkých pokročilých forem.
Rozlišují se zobecněné formy, bulbární formy a čisté oční formy. Lze vytvořit různé kombinace (okulo-bulbární formy). Čisté oční formy jsou omezeny na zhoršení vnější okulomotricity a ptózy. Deset až dvacet procent (10 až 20%) očních forem zůstane v této fázi, což znemožňuje, ale mírnou formu onemocnění, ostatní progredují do generalizované myasthenia gravis.
Počáteční bulbární formy (15%) zahrnují nosní hlas s obtížemi artikulace, žvýkací slabost s tendencí k pádu čelisti, potíže s polykáním (dysfagie) s falešným jídlem nebo slinami.
Průběh nemoci obvykle nastává po řadě zhoršení a remise, které mohou být pro generalizované formy střídány skutečnými „myastenickými krizi“. Tyto krize, skutečné lékařské pohotovosti, jsou definovány náhlým zhoršením s akutním respiračním selháním, dušností s přetížením, poruchami polykání s rizikem aspirace nebo silnou generalizovanou slabostí s impotencí, která nedává odpočinek.
Stádia maximální závažnosti je dosažena během tří let u více než tří čtvrtin pacientů.
V 1 až 5% případů je onemocnění deklarováno inaugurační myastenickou krizí. Diagnóza je pak nesmírně obtížná a musí být vyvolána v případě disproporce mezi předpokládanou kauzální patologií a klinickou závažností nebo v případě nevysvětlitelných opakovaných neúspěchů při pokusech o odstavení mechanické ventilace, což je v takových situacích nutné vyvolat. jako akutní polyradikuloneuritida.
Osserman Clinical Classification nebo MGFA (Myasthenia Gravis Foundation of America)
Tato klasifikace popisuje několik fází:
- stupeň I : slabost očního svalu, možná ptóza. Žádná jiná svalová slabost
- stupeň II : slabost očních svalů jakékoli závažnosti, mírná slabost ostatních svalů
- stupeň IIa : převážně slabé svaly končetin nebo trupu
- stupeň II b: převládající slabost dýchacích svalů nebo poruchy polykání
- stupeň III : slabost očních svalů jakékoli závažnosti, mírná slabost ostatních svalů
- stupeň IIIa : převážně slabé svaly končetin nebo trupu
- stupeň III b: Převážně slabé dýchací svaly nebo poruchy polykání
- stupeň IV : slabost očních svalů jakékoli závažnosti, silná slabost ostatních svalů
- stupeň IV a: převážně slabost svalů končetin nebo svalů trupu
- stupeň IV b: převládající slabost dýchacích svalů nebo poruchy polykání. Může také zahrnovat potřebu nasogastrické sondy bez intubace
- stupeň V : intubace nezbytná k udržení dýchání
Speciální tvary
Různé formy myasthenia gravis si zaslouží být individualizovány jejich prezentací a konkrétním řízením.
Autoimunitní fetální a neonatální myasthenia gravis
Placenta je propustná pro protilátky. U deseti až dvaceti procent (10 až 20%) dětí matek s myasthenia gravis se novorozenecká myasthenia gravis objevuje během prvních 3 dnů a obvykle odezní během několika týdnů (maximálně 3 měsíců). Mezi příznaky, které se u jednotlivých dětí liší, patří: hypotonie, slabý pláč, poruchy sání nebo polykání, ptóza, diplegie obličeje a potíže s dýcháním. Léčba je založena na symptomatickém managementu na novorozenecké jednotce intenzivní péče až do vymizení a podání anticholinesteráz. Vývoj je obecně příznivý. V nejtěžších formách lze provést exsangvinotransfuzi.
Fetální formy jsou vzácnější a mohou mít za následek zpomalení intrauterinního růstu. Výjimečně se vyskytují závažné klinické projevy (hydramnion, artrogrypóza, smrt v děloze).
Infantilní a juvenilní autoimunitní myasthenia gravis
Myasthenia gravis začínající před 15. rokem věku, si tuto formu zaslouží individualizovat kvůli obtížnému rozlišení s vrozenou neautomunitní myasthenia gravis a vzhledem k věku je nutné co nejvíce omezit užívání kortikosteroidů a imunosupresiv.
Autoimunitní iatrogenní myasthenia gravis
Výjimečně je jejich diagnóza obecně patrná na základě klinické anamnézy. Zahrnují stejné autoprotilátky a reagují na stejnou léčbu jako klasická myasthenia gravis. Je však pravděpodobné, že budou reagovat na konkrétní léčbu. Zatím byly prokázány pouze:
- Myasthenia gravis vyvolaná D-penicilaminem. Týká se 1% pacientů léčených D-penicilaminem. Pravidlem je zotavení po vysazení D-penicilaminu do 6 měsíců;
- myasthenia gravis vyvolaná alogenní transplantací dřeně s onemocněním štěp versus hostitel.
Přidružené patologie
Určité patologické stavy by měly být systematicky vyšetřovány kvůli četnosti jejich spojení s myasthenia gravis nebo závažnosti jejich inherentní spontánní prognózy.
Nádory brzlíku
U 10 až 15% případů myasthenia gravis s protilátkami proti acetylcholinovému receptoru byl nalezen thymom . Thymomy jsou nádory předního mediastina, často benigní, variabilně spojené s myasthenia gravis.
Markerem existence těchto thymomů u pacientů mladších 60 let je anti-titin. Chirurgická indikace je nezbytná. Umožňuje určit, zda je thymom benigní (2/3 případů) nebo maligní podle jeho invazivního charakteru či nikoli.
U 50-70% mladé formy myasthenia gravis s protilátkou proti acetylcholinovému receptoru byla nalezena thymická hyperplazie. Tuto anomálii je vždy třeba považovat za benigní (což nevylučuje ablaci brzlíku).
Mezi 15 a 20% pacientů s thymomem se také projevují klinické příznaky myasthenia gravis a 25% pacientů má protilátky proti acetylcholinovému receptoru (protilátky anti-ACh-R), aniž by vykazovaly příznaky. Každý pacient s thymomem se známkami myasthenia gravis má pozitivní protilátky a jakákoli asymptomatická mediastinální masa spojená s anti-ACh-R protilátkami je thymom. Zatímco statistická asociace naznačuje korelaci mezi těmito dvěma patologiemi, přesný mechanismus příčiny a následku zůstává diskutován a zvažuje se několik hypotéz:
- výběr defektních T lymfocytů v thymomu, odpovědných za hypersekreci autoprotilátek;
- vadná prezentace autoantigenů na buňkách thymic, vedoucí k ne-eliminaci T lymfocytů, které je rozpoznávají;
- přítomnost specifických zárodečných center v thymickém parenchymu snadněji produkujících autoprotilátky;
- u starších osob přítomnost nespecifické autoimunity.
Ne všechny histologické typy thymomu jsou spojeny stejným způsobem s myasthenia gravis, některé s ním nikdy nejsou spojeny:
- typ A: 0%
- typ AB: 6,8%
- typ B1: 40%
- typ B2: 55,6%
- typ B3: 10%
- karcinom brzlíku: 0%
Autoimunitní onemocnění
V 5 až 15% případů, v závislosti na sérii, je u myasteniky identifikováno alespoň jedno další autoimunitní onemocnění. Toto jsou zprávy o významných asociacích, kromě hypotézy „dysimunní země“ nebyla prokázána žádná patofyziologická souvislost. Těmito patologiemi jsou autoimunitní dysthyroidismus, revmatoidní artritida, systémový lupus erythematodes, Sjögrenův syndrom, polymyositida, chronické zánětlivé onemocnění střev, Biermerova anémie, autoimunitní hemolytická anémie, adrenální nedostatečnost.
Další testy
Doplňková vyšetření, kromě vyšetření zaměřených na vyloučení alternativních diagnóz, mají za cíl potvrdit nebo vyloučit diagnózu a v případě diagnostického potvrzení vyhledat související patologie. Jedná se o tyto zkoušky:
Pro diagnostické účely
BiologieV klinické praxi jsou hledány pouze protilátky anti-acetylcholinového receptoru a, pokud chybí, protilátky anti-MuSK. Jejich specificita je 99%. Jejich celková citlivost je více než 90%, méně než 10% myasthenia gravis je proto definováno jako „seronegativní“. Přesněji řečeno, citlivost anti-receptorových protilátek na acetylcholin je 90% pro generalizovanou myasthenia gravis a 50% pro oční myasthenia gravis. Za předpokladu, že test na protilátky proti acetylcholinovému receptoru je negativní, je citlivost anti-MuSK protilátek 40% pro generalizovanou myasthenia gravis a marginální pro oční myasthenia gravis.
Jejich vynikající specificita z nich činí nejlepší test pro potvrzení diagnózy v případě silného klinického podezření (pozitivní prediktivní hodnota pouze 1% pro běžnou populaci).
V poslední době je také možné testovat protilátky LRP4 v případě dvojitě negativní myasthenia gravis.
Elektrofyziologická vyšetřeníJsou nutná dvě elektrofyziologická vyšetření:
- elektromyografická studie, která zahrnuje:
- běžný elektromyogram, který je obvykle normální. V závažných pokročilých případech však lze pozorovat činnosti inervace,
- elektromyografická studie s opakovanou supra-maximální stimulací motorického nervu. Test je považován za pozitivní, když je pokles amplitudy potenciálu pohonné jednotky (PUM) větší než 10%. Tento test je nespecifický a má citlivost 79% pro generalizovanou myasthenia gravis a 50% pro oční myasthenia gravis,
- „jednovláknová“ elektromyografická studie s měřením Jitteru (variace latence mezi stimulací a potenciálem motorické jednotky pro dané vlákno během opakované stimulace motorického nervu) znamená studium mnoha vláken vyžadujících zkušeného zkoušejícího a specializovaného zařízení. Test je považován za pozitivní, pokud je pozorováno zvýšení tohoto chvění nad laboratorní standardy pro studovaný sval. Tento test je nespecifický a má citlivost 98% pro generalizovanou myasthenia gravis a 80% pro oční myasthenia gravis,
- studie rychlostí nervového vedení. Toto vyšetření musí být normální, aby byly abnormality elektromyogramu považovány za relevantní.
Díky vynikající citlivosti elektromyografie je nejlepším testem pro vyloučení diagnózy v případě slabého klinického podezření (neurčitá negativní prediktivní hodnota, pokud je podíl pacientů ve studované skupině větší než 1%).
Farmakologický testProstigmin se používá buď jako terapeutický test per os, nebo při IM nebo zvláště IV před klinickým příznakem, který nemluvil na elektrofyziologické úrovni nebo v naléhavých případech (ptóza, diplopie, poruchy řeči nebo dýchání). považováno za pozitivní, pokud vede ke zlepšení příznaků nebo elektrofyziologických příznaků. Někdy se srovnává s placebovým testem.
Při hledání souvisejících patologií
BiologieSystematicky budou měřeny markery autoimunitních patologií potenciálně spojených s myasthenia gravis. To zahrnuje markery zánětu, hormony štítné žlázy a protilátky proti pyroperoxidáze, anti-nukleární faktory, anti-nukleární protilátky, hematogram, ionogram, funkce jater a ledvin, vitamin B12 a folát.
Hrudní CT skenerProvádí se systematicky k hledání thymomu (citlivost 99%, specificita 95%) a hyperplazie brzlíku (senzitivita 50%, specificita 95%).
Diferenciální diagnostika
Diferenciální diagnóza je široká a závisí na klinickém projevu. Můžeme zmínit zejména:
- další myastenické syndromy: vrozená myasthenia gravis , Lambert-Eatonův myastenický syndrom , botulismus , některé hadí jedy , otrava organofosforem nebo hořčíkem;
- myopatie;
- periferní neuropatie;
- revmatické patologie;
- poruchy tekutin a elektrolytů;
- endokrinopatie;
- anémie;
- získaná, vrozená a traumatická ptóza;
- dekompenzovaný strabismus;
- funkční poruchy, psychiatrické poruchy a syndrom chronické únavy.
Prognóza
Prognóza je u každého pacienta specifická. Můžeme však popsat některé obecnosti:
Závažnost myasthenia gravis souvisí s výskytem myastenických krizí s dýchacími potížemi a život ohrožujících. Toto riziko je nejvyšší na počátku onemocnění, přičemž 75% záchvatů se vyskytuje v prvních dvou letech vývoje.
Léčba generalizované myasthenia gravis může být neléčená fatální. Zásadní prognóza forem, které zůstávají oční, není zahrnuta.
Ve velmi vzácných případech dochází ke spontánní remisi onemocnění, jejíž trvání je proměnlivé.
10 až 20% bude na léčbu reagovat jen málo nebo ne a vyvine se u ní variabilní motorická impotence. Faktory špatné prognózy a špatné terapeutické odpovědi jsou: přítomnost thymomu, přítomnost anti-MuSK protilátek a séro-negativní formy.
Terapeutická péče
Léčba myasthenia gravis může být schematicky rozdělena na symptomatickou léčbu, udržovací léčbu a krizovou léčbu onemocnění, léčbu souvisejících patologií a obecná opatření. Obecné zásady jsou:
Symptomatická léčba myasthenia gravis
Anticholinesterázové lékyInhibitory acetylcholinesterázy, což je enzym degradující acetylcholin , představují symptomatickou léčbu první linie. Nejčastěji se používají pyridostigmin (Mestinon) a ambenoniumchlorid (Mytelasa). Užívání jiných anticholinesterázových léků (jako je neostigmin ) se stalo na rozdíl od myastenické krize okrajové. Jejich účinnost u seronegativní myasthenia gravis nebo s anti-MuSK protilátkami nebyla prokázána.
DMARD (DMARD)
Kortikosteroidy a imunosupresivaKortikosteroidy - jako je progresivní režim prednison (Cortancyl) nebo prednisolon (Solupred) - imunosupresiva - azathioprin (Imurel), který se nejvíce ukázal jako účinný - a mykofenolát mofetil (Cellcept) jsou druhým nejdůležitějším léčebným záměrem. Kortikosteroidy lze zahájit ve velmi nízkých dávkách a s pečlivým klinickým přehodnocením, přičemž časté je přechodné klinické zhoršení.
Nyní bylo prokázáno, že přidání kombinované léčby kortikosteroidy a imunosupresivy pro generalizovanou myasthenia gravis nedostatečně kontrolovanou anticholinesterázovými léky zlepšuje klinický stav po dvou letech ve srovnání s přidáním kortikosteroidů nebo imunosupresiv samostatně. Někteří odborníci doporučují jejich použití jako léčby první linie pro seronegativní formy nebo s anti-MuSK protilátkami.
Imunosupresiva nejsou pro oční formy příliš účinná.
Okrajově byla s určitým úspěchem v těžkých formách použita biologická léčba, jako je rituximab (Mabthera), chimérická monoklonální protilátka cílená na molekulu CD20 specificky exprimovanou B lymfocyty .
Intravenózní plazmaferéza a imunoglobulinTyto léčby mají kromě myastenických krizí jen malé místo ( viz níže ). Výjimečně se však používají u nejzávažnějších forem rezistentních na jiné způsoby léčby nebo v případě rychlé klinické degradace.
Léčba souvisejících patologií
Thymektomie a adjuvantní léčbaObjev thymomu je absolutní indikací pro thymektomii a vyžaduje dlouhodobé radiologické sledování při hledání neoplastických recidiv. V případě neúplné resekce, infiltrace sousedních tkání nebo objevu metastáz by měla být nabídnuta adjuvantní léčba spočívající v radioterapii a / nebo případně chemoterapii.
Klinický přínos thymektomie v nepřítomnosti thymomu je stále diskutován. Doporučuje se však v případě objevení hyperplazie brzlíku s přítomností protilátek proti acetylcholinovému receptoru u pacientů mladších 40 let. Randomizovaná studie z roku 2016 také zjistila klinické zlepšení symptomů myasthenia gravis po thymektomii, a to i při absenci hyperplazie brzlíku.
Je možné přechodné pooperační symptomatické zhoršení. V prvních měsících po thymektomii lze zahájit pokus o vysazení léku, pokud se objeví symptomatické zlepšení nebo dokonce remise.
Další ošetřeníV případě objevení se související autoimunitní patologie je nutná specifická léčba.
Řízení myastenických krizí
Podpůrná péčeJakýkoli rychlý nástup respiračního selhání, dušnost s bronchiálními kongescemi, poruchami polykání nebo generalizovanou slabostí objektivizovanou lékařem ospravedlňují lékařský přesun do nemocniční instituce s jednotkou intenzivní péče. Po přijetí bude provedeno posouzení dýchacích cest, dýchání, oběhu a neurologie a také měření vitální kapacity (CV). Porucha vědomí, vitální kapacita menší než 25% teoretické hodnoty nebo klinické respirační vyčerpání ospravedlňují intubaci a přenos na jednotku intenzivní péče pro mechanickou ventilaci a možnou hemodynamickou stabilizaci. V ostatních případech postačuje běžná péče s pravidelným hodnocením vitální kapacity.
Oprava reverzibilních spouštěcích a propagačních faktorůTyto faktory musí být prozkoumány a opraveny, jakmile jsou provedeny zásadní manévry. Jedná se hlavně o iatrogenní příčiny (viz Kontraindikace léků), infekce, dekompenzace dalších chronických patologických stavů pacienta a teplota, endogenní nebo exogenní.
Případ záchvatů vyskytujících se během těhotenství je zvláštní a možnost jejich výskytu musí být předem projednána s pacientkou. Těžké záchvaty, které nereagují na symptomatickou léčbu, vyžadují odpovídající léčbu.
Vylučte předávkování anticholinesterázamiHlavní diferenciální diagnózou myastenické krize je předávkování anticholinesterázou. Je třeba jej systematicky podezřívat v případě denního příjmu více než 480 mg pyridostigminu nebo muskarinových příznaků: bradykardie, bilaterální mióza, hypersekrece, rozpad stolice atd. V případě pochybností potvrdí diagnózu předávkování klinické zhoršení po podání neostigminu. Vedení je pak čistě podpůrné, kromě podávání atropinu pro jeho anti-muskarinové účinky.
Symptomatická léčbaPodávání neostigminu je symptomatickou léčbou první linie. Pokud se objeví muskarinové příznaky, měl by se přidat atropin.
V případě klinického zhoršení během léčby je třeba zvážit předávkování anticholinesterázovými léky.
V případě špatné terapeutické odpovědi (selhání detubace) je léčba druhé linie založena na opakování plazmaferézy a / nebo intravenózních imunoglobulinových léčení.
Pokud se to nepodaří, jsou léčbou třetí linie kortikosteroidy a imunosupresiva. Jejich indikace však musí být pečlivě kladeny, přechodné klinické zhoršení je běžné.
Obecná opatření a zdravotnická péče
Kontraindikace léků Myastenická kartaFrancouzské ministerstvo zdravotnictví vydalo kartu pro péči a pohotovost pro lidi s myasthenia gravis. Důrazně se doporučuje nosit kartu s uvedením jeho nemoci, jeho léčby, jeho posledních očkování a seznamu léků kontraindikovaných u myasthenia gravis. Mohou ji získat z referenčních konzultací nebo kontaktováním AFM-téléthon].
Životní stylStejně jako u jakékoli chronické patologie vyžaduje myasthenia gravis, aby byl pacient poučen o své nemoci, zejména o faktorech upřednostňujících myastenické krize. Účast na mírném fyzickém cvičení, přizpůsobená aktuálnímu stavu, by měla být podporována častým odpočinkem.
Zdravotnická péčeU těžkých forem nebo u pacientů rezistentních na důkladnou léčbu se může ukázat jako nezbytná sociální podpora a odborníky na fyzioterapii, logopedii, pracovní terapii, rehabilitaci nebo psychologii, stejně jako doporučení pacienta ke kombinaci léčby.
Připravte se na těhotenství a operaceCelkově je těhotenství a chirurgický zákrok hlavní příčinou myastenických záchvatů, ke kterým dochází ve 30% případů. Aby se minimalizovala rizika, někteří autoři doporučují předporodní a předoperační výkon plazmaferézních sezení nebo imunoglobulinových léčení a také vyhodnocení včetně funkčních respiračních testů. Porod musí vždy probíhat v nemocničním zařízení s jednotkou intenzivní péče a novorozeneckou resuscitační jednotkou. Detubace by nikdy neměla být prováděna, dokud není potvrzena schopnost pacienta účastnit se.
Během těhotenství musí být kortikosteroidy a imunosupresiva používány po konzultaci s gynekologem.
Poznámky a odkazy
- (in) MB Walker , „ Léčba myasthenia gravis pomocí fyzostigminu “ , Lancet , sv. 1,1934, str. 1200-1201 ( DOI 10.1016 / S0140-6736 (00) 94294-6 )
- (in) Phillips LH, „Epidemiologie myasthenia gravis “ Ann NY Acad Sci. 2003; 998: 407-12
- Vysoká škola učitelů neurologie. Myasthenia gravis
- (in) Carr AS, Cardwell CR, PO McCarron, J McConville, „Systematický přehled populačních epidemiologických studií u myasthenia gravis“ BMC Neurol. 2010; 10:46.
- (en) Bradley et al. Neurologie v klinické praxi , 5 th ed., Butterworth-Heinemann, 2007
- Goulon-Goeau a kol. „Myasthenia gravis and myasthenic syndromy“ EMC-Neurologie , 17-172-B-10, 2002, Elsevier, online shrnutí
- B. Eymardem „Protilátky myasteniích“ neurologická přezkoumání 2009; 165 (2): 125-205 DOI : 10,1016 / j.neurol.2008.11.020
- (v) Zhang B, C, Shen Bealmear B, Ragheb S, Xiong WC, Lewis RA, Lisák RP, Mei L. " Autoprotilátky k agrinu v myasthenia gravis pacientů " PLoS One , 2014; 3: e91816 DOI : 10,1371 /journal.pone.0091816
- (in) W. Allan. „Patogeneze myastenie“ Aktuální , 2012
- (in) Howard et al. "Klinické korelace protilátek, které vážou, blokují nebo modulují receptory lidské acetylcholinu v myasthenia gravis " Ann NY Acas Sci. 1987
- (en) SJ Bird „Klinické projevy myasthenia gravis “ Aktuální, 2013
- (en) Bershad et al. „ Krize Myasthenia gravis “ South Med J. 2008; 101 (1): 63-9. DOI : 10.1097 / SMJ.0b013e31815d4398
- Gaumond „Oční poruchy myasthenia gravis“ EMC-Neurologie , 2005 DOI : 10.1016 / j.emcn.2005.08.002
- (in) Pelak and When „Ocular myasthenia“ Up-to-Date , 2013
- (en) Spillane J, E Higham, Kullmann DM. „ Myasthenia gravis “ BMJ 2012; 345: e8497
- (en) Jaretzki A, Barohn RJ, Ernstoff RM a kol. , „ Myasthenia gravis: doporučení pro klinické výzkumné standardy. Pracovní skupina lékařské vědecké poradní rady nadace Myasthenia Gravis Foundation of America “ , Neurology , sv. 55, n o 1,2000, str. 16–23 ( PMID 10891897 , číst online )
- (in) Finnis MF Jayawant S, „ Juvenile myasthenia gravis: a pediatric perspective “ , Autoimmune Dis , sv. 2011,2011, str. 404101. ( PMID 22110902 , PMCID PMC3206364 , DOI 10.4061 / 2011/404101 , číst online [html] )
- Antititinová protilátka u myasthenia gravis s časným a pozdním nástupem. Szczudlik P, Szyluk B, Lipowska M, Ryniewicz B, Kubiszewska J, Dutkiewicz M, Gilhus NE, Kostera-Pruszczyk A. Acta Neurol Scand. 2014 (červen). Doi: 10.1111 / ane.12271. [EPUB před tiskem]
- Thymus, thymoma a myasthenia gravis Fujii Y, Surg Today 2013 květen; 43 (5): 461-6. doi: 10,1007 / s00595-012-0318-2
- Klinický a funkční význam klasifikace WHO pro neoplasmy lidského thymického epitelu: studie 146 po sobě jdoucích nádorů. Okumura M, Miyoshi S, Fujii Y, Takeuchi Y, Shiono H, Inoue M, Fukuhara K, Kadota Y, Tateyama H, Eimoto T, Matsuda H, Am J Surg Pathol 2001 Jan; 25 (1): 103-10.
- (en) Mercelis et al. „Diagnostická užitečnost stimulované jednovláknové elektromyografie svalu orbicularis oculi u pacientů s podezřením na oční myasthenie“ Muscle Nerve 2011; 43 (2): 168-70.
- (en) Preston a kol. Elektromyografie a neuromuskulární poruchy. Klinicko-elektrofyziologické korelace , 2 th vyd., Elsevier, 2005
- (en) Taraldsen Heldan. "Séropozitivní myastenie Gravis." Celonárodní epidemiologická studie » Neurologie 2009
- (en) Trakas et al. „Vývoj vysoce citlivého diagnostického testu pro autoprotilátky proti specifické tyrosinkinázové svalové tkáni (MuSK) v myasthenia gravis“, J. Neuroimmunol . 2011; 240-241: 79-86.
- (en) Vincent a kol. „Protilátka proti acetylcholinovému receptoru jako diagnostický test na myasthenia gravis : výsledky v 153 ověřených případech a 2967 diagnostických esejích“ J Neurolo Neurosurg Psych. 1985; 48 (12): 1246-52.
- (en) Witoonpanich et al. „Elektrofyziologická a imunologická studie u myasthenia gravis : diagnostická citlivost a korelace“ Clin Neurophysiol. 2011; 122 (9): 1873-7.
- (en) Zambelis et al. „Opakovaná nervová stimulace obličejových a hypotenárních svalů: relativní citlivost v různých podskupinách myasthenia gravis“ Eur Neurol. 2011; 65 (4): 203-7.
- (en) Lindstrom a kol. „Protilátka proti acetylcholinovému receptoru v myasthenia gravis. Prevalence, klinické koreláty a diagnostická hodnota » Neurologie 1976.
- (in) Bird „Diagnosis in myasthenia gravis “ Aktuální , 2013
- Autoprotilátky proti proteinu 4 souvisejícímu s lipoproteiny u pacientů s dvojitě seronegativní myasthenia gravis. Zhang B1, Tzartos JS, Belimezi M, Ragheb S, Bealmear B, Lewis RA, Xiong WC, Lisak RP, Tzartos SJ, Mei L. Arch Neurol. Duben 2012; 69 (4): 445-51. doi: 10,1001 / archneurol.2011.2393. EPUB 2011 12. prosince
- (in) Bird „Diferenciální diognoza myasthenia gravis“ Aktuální , 2012
- (in) Bird „Léčba myastenie“ Aktuální , 2013
- (in) Howard et al. Myasthenia Gravis. Příručka pro poskytovatele zdravotní péče , Myasthenia Gravis Foundation of America, 2008
- (en) Gold R, Schneider-Gold C, „ Současné a budoucí standardy v léčbě myasthenia gravis “ , Neurotherapeutics , sv. 5, n O 4,2008, str. 535-41. ( PMID 19019304 , PMCID PMC4514693 , DOI 10.1016 / j.nurt.2008.08.011 , číst online [html] )
- (en) Mandawat et al. "Srovnávací analýza terapeutické možnosti použité pro myasthenia gravis " Ann Neurol. 2010; 68 (6): 797-805.
- " ambenonium chlorid " na www.vidal.fr (k dispozici na 1. st srpna 2015 )
- (en) Collongues N, O Casez, Lacour A. a kol. „Rituximab v refrakterní a non-refrakterní myastenii: retrospektivní multicentrická studie “ Muscle Nerve 2012; 46: 687-91
- (in) Gil I. Wolfe, Henry J. Kaminski, Inmaculada B. Aban a kol., „ Randomizovaná studie Myasthenia Gravis in Thymectomy “ , New England Journal of Medicine (NEJM \ / MMS), sv. 375, n O 6,11. srpna 2016, str. 511-522 ( ISSN 0028-4793 , DOI 10.1056 / nejmoa1602489 , číst online ).
- (in) Goldenberg, WD and Shah, AK , „ Myasthenia Gravis “ , eMedicine (přístup k 5. května 2012 )
- (fr) Tento článek je částečně nebo zcela převzat z článku Wikipedie v angličtině s názvem „ Myasthenia gravis “ ( viz seznam autorů ) .