Vzduch
| Vzduch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC kód | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární hmotnost | 28,965 g / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T. fúze | -216,2 ° C ( 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° vroucí | -194,3 ° C ( 1 atm , 874,0 kg / m 3 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpustnost | 0,0292 objem / objem (voda, 0 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
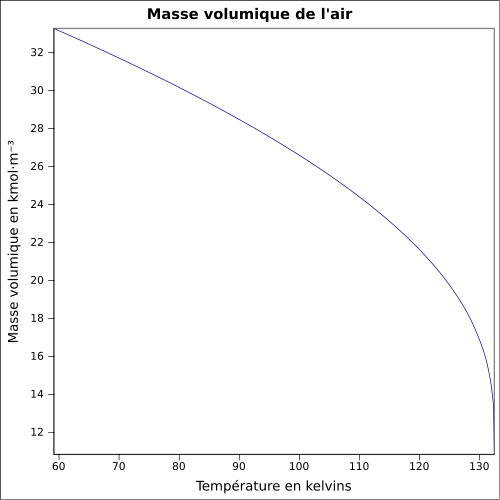
| Objemová hmotnost |
1,2 kg / m 3 ( 21,1 ° C , 1 atm )
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
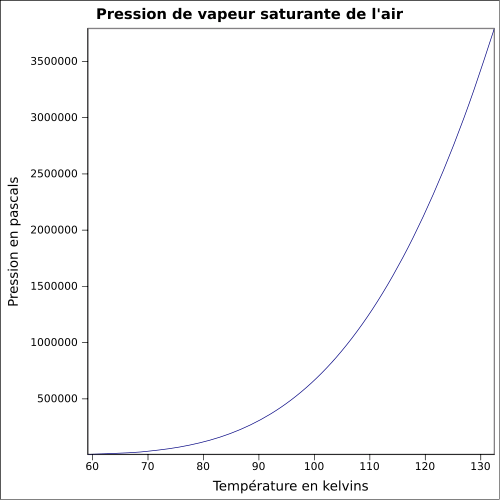
| Tlak nasycených par |
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritický bod | -140,6 ° C , 3 771 kPa , 351 kg / m 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 0,023 4 W m −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
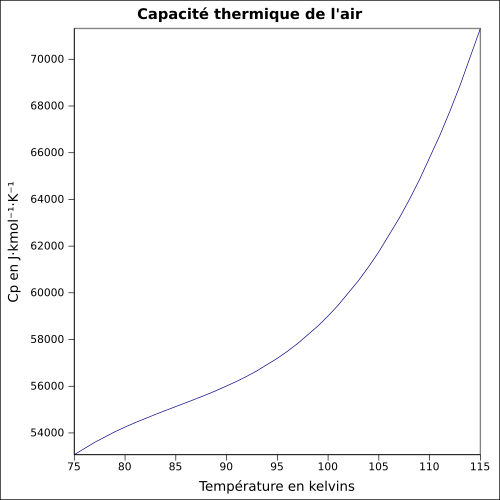
| C str |
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Index lomu | 1 000 26825 ( 100 kPa , suchý vzduch s 450 ppm CO 2) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Vzduch je směs plynů , které tvoří atmosféru Země . Obvykle je bezbarvý, neviditelný a bez zápachu.
Složení
Suchý vzduch blízko země je homogenní směs plynů. Skládá se přibližně z molárního zlomku nebo z objemu:
To také obsahuje stopy z 0.000072% dihydrogen (0,72 ppmv ), ale také ozonu , jakož i minimální přítomnost radonu . Může také obsahovat oxid siřičitý , oxidy dusíku , jemné suspendované látky ve formě aerosolu , prach a mikroorganismy.
Vzduch v zemském prostředí je většinou vlhký, protože obsahuje vodní páru . V blízkosti země je množství vodní páry velmi proměnlivé. Závisí to na klimatických podmínkách, zejména na teplotě. Parciální tlak vodní páry ve vzduchu je omezena jeho tlak nasycených par , který výrazně mění s teplotou:
| Teplota vzduchu | -10 ° C | 0 ° C | 10 ° C | 20 ° C | 30 ° C | 40 ° C |
| % vodní páry
pro tlak vzduchu 1013 hPa |
0 až 0,2% | 0 až 0,6% | 0 až 1,2% | 0 až 2,4% | 0 až 4,2% | 0 až 7,6% |
Procento vodní páry přítomné ve vzduchu se měří podle míry vlhkosti , což je důležitý prvek pro předpovědi počasí. Existuje několik množství k popisu hydrometrie: absolutní vlhkost , která odpovídá hmotnosti vodní páry na objem vzduchu; a relativní vlhkost , což je procento parciálního tlaku vodní páry ve srovnání s tlakem nasycených par .
Úroveň oxidu uhličitého se časem mění. Na jedné straně, to podstoupí roční změnu asi 6,5 ppm objemově ( p dd í l p ar m Milión v v olume) amplitudy. Na druhé straně se průměrná roční sazba zvyšuje o 1,2 až 1,4 ppmv ročně. V polovině roku 2008 to bylo řádově 384 ppmv (0,0384%), před průmyslovou revolucí to bylo 278 ppmv , v roce 1958 315 ppmv , v roce 1974 330 ppmv a v roce 1990 353 ppmv . Tento skleníkový skleníkový plyn hraje důležitou roli při globálním oteplování planety.
Metan je jiný plyn hlavní skleníkový jehož rychlost se zvyšuje s časem: 800 mm 3 / m 3 (0,8 ppmv ) v pre-průmyslové éry, 1585 mm 3 / m 3 1985, 1663 mm 3 / m 3 v roce 1992 a 1676 mm 3 / m 3 v roce 1996.
Do výšky asi 80 km je složení suchého vzduchu velmi homogenní, jedinou významnou změnou ve složení vzduchu je složení vodních par.
Složení vzduchu
|
|
||||||||||||||||||||||||||||||||||||||||||||
Hmotnostní podíly lze vyhodnotit vynásobením objemových podílů poměrem molární hmotnosti uvažovaného plynu děleno molární hmotností vzduchu, tj. 28 976 g mol −1 , například v případě CO 2. Tento poměr není zanedbatelný, protože se rovná 44 / 28,976 = 1,5185, tedy hmotnostní obsah CO 2ve vzduchu rovné 415 × 1,5185 = 630 ppmm .
Objemová hmotnost
Protože vzduch je stlačitelný plyn, jeho hustota (v kg / m 3 ) je funkcí tlaku, teploty a vlhkosti.
Pro suchý vzduch za normálního atmosférického tlaku ( 1013,25 hPa ):
Obecně se 1,293 kg / m 3 , aby 0 ° C a 1,204 kg / m 3 až 20 ° C .
Toto je zobecněno ( vzorec ideálního plynu ) v: (s T v kelvinech a P v pascalech podle konvencí SI). Pro teplotu θ ve stupních Celsia se teplota T v kelvinech získá přidáním 273,15 k θ : T (K) = θ (° C) + 273,15 .
Potenciál globálního oteplování
Potenciál globálního oteplování (GWP v angličtině : GWP: Potenciál globálního oteplování ) nebo ekvivalent CO 2umožňuje měřit „škodlivost“ každého skleníkového plynu .
Následující tabulka uvádí hodnotu GWP pro hlavní skleníkové plyny přítomné ve vzduchu:
| PRG | 1 (reference) | 8 | 23 | 310 | od 1300 do 1400 | od 6 200 do 7 100 | 6500 | 22 800 |
| plyn | oxid uhličitý | vodní pára | metan | oxid dusný (N 2 O) | chlorodifluormethan (HCFC) | dichlorodifluormethan (CFC) | tetrafluorid uhličitý (CF 4 ) | fluorid sírový (SF 6 ). |
Index lomu
Výraz pro index lomu vzduchu „za standardních podmínek“ je:
s , kde je vlnová délka vyjádřená v nanometrech (nm), kde je převrácená hodnota vlnové délky v mikrometrů.Toto je pro suchý vzduch s 0,03% oxidu uhličitého , při tlaku 101 325 Pa (760 milimetrů rtuti) a teplotě 288,15 Kelvina ( 15 ° C ).
Můžeme získat n pro jinou teplotu nebo tlak pomocí jednoho z následujících dvou výrazů:
s:
- T , teplota vyjádřená v kelvinech ;
- p , tlak v pascalech;
- T s , 288,15 K ;
- p s , 101 325 Pa ;
- n s , index lomu vzduchu uvedený výše,
nebo:
s:
- T , teplota ve stupních Celsia ;
- T s , 15 ° C ;
- p , tlak v mmHg ;
- p s , 760 mmHg ;
- , 0,00366 K -1 ;
- , (1,049 - 0,015 T ) × 10-6 mmHg -1 ;
- , 8,13 × 10-7 mmHg -1 ;
- n s , index lomu vzduchu uvedený výše.
Termofyzikální vlastnosti
Z tabulek publikovaných Frankem M. Whiteem, Heat and Mass transfer , Addison-Wesley, 1988.
s:
- T , teplota v Kelvinech ;
- ρ , hustota ;
- μ , dynamická viskozita ;
- ν , kinematická viskozita ;
- C p , specifické teplo při konstantním tlaku ;
- λ , tepelná vodivost ;
- a , tepelná difuzivita ;
- Pr , Prandtl číslo .
| T | ρ | μ | ν | C str | λ | na | Pr |
|---|---|---|---|---|---|---|---|
| K. | kg m −3 | kg m −1 s −1 | m 2 s -1 | J kg -1 K -1 | W m −1 K −1 | m 2 s -1 | - |
| 250 | 1.413 | 1,60 × 10 −5 | 0,949 × 10 −5 | 1005 | 0,0223 | 1,32 × 10 −5 | 0,722 |
| 300 | 1.177 | 1,85 × 10 −5 | 1,57 × 10 −5 | 1006 | 0,0262 | 2,22 × 10 −5 | 0,708 |
| 350 | 0,998 | 2,08 × 10 −5 | 2,08 × 10 −5 | 1009 | 0,0300 | 2,98 × 10 −5 | 0,697 |
| 400 | 0,883 | 2,29 × 10 −5 | 2,59 × 10 −5 | 1014 | 0,0337 | 3,76 × 10 −5 | 0,689 |
| 450 | 0,783 | 2,48 × 10 −5 | 2,89 × 10 −5 | 1021 | 0,0371 | 4,22 × 10 −5 | 0,683 |
| 500 | 0,705 | 2,67 × 10 −5 | 3,69 × 10 −5 | 1030 | 0,0404 | 5,57 × 10 −5 | 0,680 |
| 550 | 0,642 | 2,85 × 10 −5 | 4,43 × 10 −5 | 1039 | 0,0436 | 6,53 × 10 −5 | 0,680 |
| 600 | 0,588 | 3,02 × 10 −5 | 5,13 × 10 −5 | 1055 | 0,0466 | 7,51 × 10 −5 | 0,680 |
| 650 | 0,543 | 3,18 × 10 −5 | 5,85 × 10 −5 | 1063 | 0,0495 | 8,58 × 10 −5 | 0,682 |
| 700 | 0,503 | 3,33 × 10 −5 | 6,63 × 10 −5 | 1075 | 0,0523 | 9,67 × 10 −5 | 0,684 |
| 750 | 0,471 | 3,48 × 10 −5 | 7,39 × 10 −5 | 1086 | 0,0551 | 10,8 × 10 −5 | 0,686 |
| 800 | 0,441 | 3,63 × 10 −5 | 8,23 × 10 −5 | 1098 | 0,0578 | 12,0 × 10 −5 | 0,689 |
| 850 | 0,415 | 3,77 × 10 −5 | 9,07 × 10 −5 | 1110 | 0,0603 | 13,1 × 10 −5 | 0,692 |
| 900 | 0,392 | 3,90 × 10 −5 | 9,93 × 10 −5 | 1121 | 0,0628 | 14,3 × 10 −5 | 0,696 |
| 950 | 0,372 | 4,02 × 10 −5 | 10,8 × 10 −5 | 1132 | 0,0653 | 15,5 × 10 −5 | 0,699 |
| 1000 | 0,352 | 4,15 × 10 −5 | 11,8 × 10 −5 | 1142 | 0,0675 | 16,8 × 10 −5 | 0,702 |
| 1100 | 0,320 | 4,40 × 10 −5 | 13,7 × 10 −5 | 1161 | 0,0723 | 19,5 × 10 −5 | 0,706 |
| 1200 | 0,295 | 4,63 × 10 −5 | 15,7 × 10 −5 | 1179 | 0,0763 | 22,0 × 10 −5 | 0,714 |
| 1300 | 0,271 | 4,85 × 10 −5 | 17,9 × 10 −5 | 1197 | 0,0803 | 24,8 × 10 −5 | 0,722 |
Vztah mezi teplotou a tepelnou vodivostí vzduchu platný pro teplotu mezi 100 K a 1600 K je následující:
nebo:
- : teplota vyjádřená v K
- : tepelná vodivost ve W m −1 K −1
Vztah mezi dynamickou viskozitou vzduchu a teplotou je:
nebo:
- : teplota v K
- : dynamická viskozita v kg m −1 s −1
Vztah mezi kinematickou viskozitou vzduchu a teplotou je:
nebo:
- : teplota v K
- : kinematická viskozita vm 2 / s
Podle informací WPI (en) je vztah mezi měrným teplem vzduchu a teplotou:
nebo:
- : teplota v K
- : měrné teplo v J kg -1 K −1
Tlak
Kvůli poklesu tlaku vzduchu s nadmořskou výškou je nutné natlakovat kabiny letadel a jiných letadel . V praxi je tlak vyvíjený v kabinách větší než vnější tlak, i když menší než tlak na úrovni země.
Stlačený vzduch se používá také v potápění .
Zkapalnění
Vzduch je tvořen různými plyny, které se při dostatečném ochlazení nakonec změní na kapalné a poté na pevné . Například kyslík ztuhne při teplotě -218 ° C , se dusík se tekutým při -195 ° C . Při teplotě -270 ° C (asi 3 K ) jsou potom všechny plyny kromě hélia pevné a získáváme „zmrzlý vzduch“.
Vzduch nemohl být zkapalněn dříve, než budou známy kritické tlaky a teploty, které označují teoretické limity, za kterými může sloučenina existovat pouze v plynném stavu. Protože vzduch je směs, tyto hodnoty nemají striktní význam, ale ve skutečnosti již při teplotě nad -140 ° C není vzduch zkapalnitelný.
Teplota varu součástí vzduchu
| Příjmení | Vzorec | Teplota |
|---|---|---|
| Dinitrogen | Č. 2 | -195,79 ° C , kapalný dusík |
| Dioxygen | O 2 | -183 ° C , kapalný kyslík |
| Argon | Ar | -185,85 ° C |
| Oxid uhličitý | CO 2 | -56,6 ° C při 5,12 atm |
| Neon | narozený | -246,053 ° C |
| Hélium | Ahoj | -268,93 ° C , kapalné hélium |
| Oxid dusnatý | NE | -151,8 ° C |
| Krypton | Kr | -154,34 ° C |
| Metan | CH 4 | -161,52 ° C |
| Dihydrogen | H 2 | -252,76 ° C , kapalný vodík |
| Oxid dusičitý | N 2 O | -88,5 ° C |
| Xenon | Xe | -108,09 ° C |
| Oxid dusičitý | Č. 2 | 21,2 ° C |
| Ozón | O 3 | -111,9 ° C |
| Radon | Rn | -61,7 ° C |
První kapky kapalného vzduchu získali téměř současně Louis Paul Cailletet a Raoul-Pierre Pictet v roce 1877 náhlou expanzí mezi 300 a 1 atmosférou.
V roce 1894 vyvinul nizozemský fyzik Heike Kamerlingh Onnes první zařízení na kapalný vzduch. Během příštích 40 let provedli vědci ve Francii, Velké Británii, Německu a Rusku mnoho vylepšení procesu.
Sir James Dewar poprvé zkapalnil vodík v roce 1898 a Heike Kamerlingh Onnes helium, nejtěžší plyn ke zkapalnění, v roce 1908 .
Nezávisle na Carl von Linde , Georges Claude vyvinuta v roce 1902 je průmyslový proces pro zkapalňování vzduchu.
Symbolický
- V nevědeckém poli je vzduch jedním ze čtyř prvků (spolu s ohněm , vodou a zemí ), které byly kdysi považovány (a v některých kulturách stále považovány) za látky, na nichž bude založen celý život. Je symbolem Ducha.
- Vzduch je také často spojován s různými jinými pojmy, jako je rodina mečů v tarotových balíčcích .
Poznámky a odkazy
Poznámky
- Toto je molární hmotnost suchého vzduchu.
Reference
- „ Air “ , na olivier.fournet.free.fr (přístup 4. března 2010 )
- (en) Compressed Gas Association, Příručka pro stlačené plyny , Springer,1999, 4 th ed. , 702 s. ( ISBN 0-412-78230-8 , číst online ) , s. 234
- (en) Robert H. Perry a Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- (in) Philip E. Ciddor, „ Index lomu vzduchu: nové rovnice pro viditelné a blízké infračervené záření “ , Applied Optics , sv. 35, n o 9,1996, str. 1566-1573 ( DOI 10.1364 / AO.35.001566 )
- (in) Nedávný globální CO2 na noaa.gov, přístup k 21. dubnu 2021.
- (in) Keeling Curve , web keelingcurve.ucsd.edu, přístup 23. dubna 2015
- Koncentrace CO 2 v zemské atmosféře
- Koncentrace CO 2 měřená na Mauna Loa (Havaj), NOAA.
- Koncentrace metanu měřená na Mauna Loa (Havaj), NOAA.
- V praxi silně vysušený vzduch stále obsahuje stopy vodní páry.
- Zdroj dat: Oxid uhličitý: (en) NASA - Earth Fact Sheet , leden 2007. Metan: IPCC TAR; tabulka 6.1, 1998 (en) Třetí hodnotící zpráva IPCC „Climate Change 2001“, kterou předložila skupina GRID-Arendal v roce 2003. Celkem NASA činila 17 ppmv ze 100% a CO 2zde se zvýšil o 15 ppmv . K normalizaci by měl být N 2 snížen o 25 ppmv a O 2 o 7 ppmv .
- „ Index lomu vzduchu “ , na olivier.fournet.free.fr (přístup 4. března 2010 )
- Chemičtí profesionálové
- Chemical Professionals , nenalezeno 11. srpna 2013
- Tento dokument z webu WPI na webu wpi.edu
Podívejte se také
Související články
- Hustota vzduchu
- Vzduchová hmota
- Psychrometrie
- Vlhký vzduch
- Znečištění ovzduší a předměty z kategorie: Znečištění ovzduší
- Kvalita vzduchu