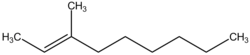
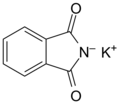
Organická sloučenina
Tyto organické sloučeniny jsou sloučeniny, z nichž jeden z chemických prvků složkou je uhlík , s několika výjimkami . Tyto sloučeniny mohou být přírodního původu nebo mohou být vyrobeny syntézou .
Je užitečné zaprvé rozlišit organické sloučeniny od anorganických sloučenin .
Rozlišení mezi organickými sloučeninami a anorganickými sloučeninami
Sloučenina se o chemické látky se skládají ze dvou nebo více různých chemických prvků .
Organické sloučeniny
Etymologie výrazu „organický“ je historická. Na začátku byla organická chemie chemií látek tvořených živými organismy (rostlinami, zvířaty a bakteriemi) pomocí tajemné „ životní síly “. Studium biochemických sloučenin vedlo chemiky k odstranění vody z organismů odpařováním a získání zbytkové suché hmotnosti, z nichž většina se skládá z molekul uhlíku. Když je objevili, věřili, že tyto uhlíkové molekuly existují pouze v živých organismech, a nazývali je organickými molekulami, aby se odlišily od anorganických molekul neživého světa.
Charakteristika uhlíku spočívá ve schopnosti jeho atomů navzájem se spojovat kovalentními vazbami téměř neurčitě a vytvářet uhlíkové řetězce velké rozmanitosti, které charakterizují molekuly zvané „Organické“. Tyto uhlíkové řetězce tvoří páteř organických sloučenin.
Nějaké příklady
-
3D struktura
- Tetrachlorethylen (stavební bloky: uhlík a chlor Cl)
-
Rovinný strukturní vzorec
-
3D struktura
-
3D struktura
-
Skeletální vzorec (uhlíková kostra)
- Struktura
-
Zastoupení společnosti Kékulé
-
Molekulární model
-
Zastoupení společnosti Kékulé
-
Reprezentace se šesti delokalizovanými elektrony
- Fenoplasty ( makromolekuly složené z prvků uhlík, vodík a kyslík O)
Anorganické sloučeniny
Anorganické sloučeniny jsou všechny ostatní sloučeniny.
Tyto sloučeniny původně představovaly látky nalezené v neživých bytostech „ minerální říše “ .
Zatímco organické sloučeniny se tvoří z kovalentních nebo převážně kovalentních vazeb, „ minerální “ sloučeniny se často tvoří z iontových nebo dominantních iontových vazeb .
Poznámky
- K allotropes uhlíku , jako je například diamant a grafitu , samotných konstrukcí na bázi uhlíkových řetězců nepatří do skupiny organických sloučenin. Ve skutečnosti jsou to jednoduchá tělesa , která se skládají z uhlíku s jedním prvkem, a ne ze sloučenin . Jsou zařazeny mezi anorganické minerální druhy
- Některé sloučeniny uhlíku lze klasifikovat jako anorganické sloučeniny. Některé příklady jsou uvedeny níže .
Organické sloučeniny
Existence organických sloučenin je založena na prvku uhlík .
Existuje velmi široká škála organických sloučenin, které lze nalézt v pevném, kapalném nebo plynném stavu. Organické molekuly obecně hrají důležitou roli v chemických reakcích probíhajících v živých organismech a jsou jádrem lidského průmyslu , zejména prostřednictvím ropných produktů . Odvětví chemie se zájmem o organické molekuly je organická chemie .
Organické molekuly obvykle obsahují alespoň jeden atom z uhlíku (C), vázanou na atom vodíku (H), ale ne vždy. Tam jsou organické sloučeniny, které neobsahují žádné CH vazbu: The kyseliny šťavelové se kyselina trifluoroctová se hexachlorethan a močovina jsou příklady.
Přírodní organické sloučeniny mají biologický původ .
Stavební kameny organických sloučenin
Kromě uhlíku obsahují organické sloučeniny jen malou škálu prvků:
- vodík (H), přičemž kyslík (O), přičemž dusík (N), nebo více zřídka síry (S) nebo fosforu (P), v případě přírodních organických látek;
- syntetické sloučeniny mohou obsahovat další prvky, například halogeny .
Přesnější popis rodiny organických sloučenin se trochu liší podle zdrojů. Někteří citují kovy jako stavební kameny syntetických organických sloučenin.
Sloučeniny uhlíku klasifikované jako anorganické
Několik jednoduchých sloučenin uhlíku je klasifikováno jako anorganické sloučeniny .
Uvedené sloučeniny jsou obecně:
Oxid uhelnatý (CO) a oxid uhličitý (CO 2 ), kyselina uhličitá, uhličitany a hydrogenuhličitany , že kyanidy jsou karbidy (kromě oleje ).
Poznámky
- Uhličitany, hydrogenuhličitany a kyanidy jsou obecně iontové sloučeniny , jejichž charakter je anorganický (viz část „ anorganické sloučeniny “).
Tyto sloučeniny jsou elektricky neutrální sestavy uhlíkatých kationtů a aniontů klasifikovaných v tomto případě mezi anorganické uhlíkaté chemické entity : - CO 3 2 - anionty pro uhličitany, HCO 3 - pro hydrogenuhličitany a CN - pro kyanidy - Existuje několik organické karbonáty (např, ethylenkarbonát , dimethylkarbonát ) a organické kyanidy (např vinyl kyanid , benzyl kyanid ), které jsou syntetické sloučeniny, uhlík kovalentní ve kterém skupiny CO 3 a CN nejsou ionty
Vyčerpávající definice
Podle evropské směrnice z 11. března 1999 označuje pojem „organická sloučenina“:
Jakákoliv sloučenina, která obsahuje alespoň prvek uhlík a jeden nebo více z následujících: vodík , halogen , kyslík , síra , fosfor , křemík nebo dusík , s výjimkou z oxidů uhlíku a uhličitany a hydrogenuhličitany anorganické .
„ Anorganická “ přesnost je důležitá, aby se vyloučily možné organické formy sloučenin uvedených ve výjimkách , jak bylo uvedeno výše v poznámkách .
Případ organokovových sloučenin
Sloučeniny, které mají kovalentní vazbu kov - uhlík mezi jedním nebo více atomy kovu a jedním nebo více atomy uhlíku "organyl" skupin, jsou součástí chemie zvané organokov .
Tyto sloučeniny ilustrují „ svévolný a v určitých případech zcela konvenční charakter “ rozdílu mezi organickými a anorganickými :
„Například nedávný vývoj chemie organokovových sloučenin (sloučenin s vazbou uhlík-kov), bioanorganické chemie (třicet prvků je nezbytných pro život, včetně sedmnácti kovů), ilustruje velmi relativní charakter hranic mezi chemickými minerály , organická chemie, dokonce i biochemie . "Organokovové sloučeniny ve skutečnosti kombinují aspekty organické chemie a anorganické chemie. Organokovová chemie „představuje jakýsi most mezi organickou chemií a anorganickou chemií “ .
Klasifikace
Zde je seznam funkcí organické chemie s příkladem vzorce, názvu a čísla CAS pro každou z nich .
Pro různé reprezentace níže viz „ reprezentace molekul “ a „ kosterní vzorec “.
Sloučeniny uhlíku (uhlovodíky nebo karbidy vodíku)
- Nasycené alifatické uhlovodíky
-
Alkany :
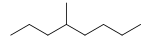 4-methyloktan (CAS )
4-methyloktan (CAS )
- Cykloalkany :
-
Alkany :
- Ethylenické uhlovodíky nebo olefiny nebo alkeny
- Monoalkeny:
-
Dienes :
- Alleny : 1,2-buta-dien nebo methyl allen (CAS )
- Polyeny
- Cykloalkeny nebo cykleny:
-
Dienes :
- Cyklodieni :
- Acetylenické uhlovodíky nebo alkyny :
Monovalentní organické funkce
V tomto případě je monovalentní funkce tam, kde je každý dotčený uhlík vázán k jedinému atomu, kterým není ani uhlík, ani vodík, nazývaný heteroatom .
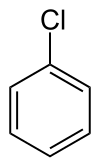
fenylchlorid nazývaný také chlorbenzen (CAS )
Monovalentní deriváty s kyslíkem
 n- butanol (CAS )
n- butanol (CAS )
 4-methylfenol nebo p-kresol
4-methylfenol nebo p-kresol
 methoxyethan (CAS )
methoxyethan (CAS )
- Etherové soli minerálních kyselin
Monovalentní deriváty s dusíkem
- Nitrosloučeniny
- Nitroso sloučeniny
 methylhydroxylamin (CAS )
methylhydroxylamin (CAS )
- Alifatické aminy
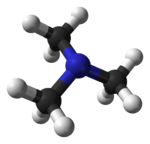 trimethylamin (CAS 75-50-3) ethylamin (CAS )
trimethylamin (CAS 75-50-3) ethylamin (CAS )
- Ketaly (a poloketaly, acetály , poloacetaly)
 1,1 (CAS )
1,1 (CAS )
 (CAS )
(CAS )
Bivalentní organické funkce
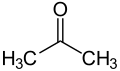 aceton nebo 2-propanon (CAS )
aceton nebo 2-propanon (CAS )
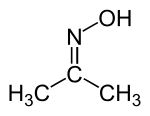 dimethylketoxime, isopropylideneazanol nebo 2-propanon, oxim (CAS )
dimethylketoxime, isopropylideneazanol nebo 2-propanon, oxim (CAS )
 3-penten-2-on (CAS )
3-penten-2-on (CAS )
Trojmocné organické funkce
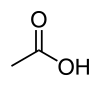 octová kyselina
octová kyselina
 anhydrid kyseliny propionové (CAS )
anhydrid kyseliny propionové (CAS )
 acetylchlorid (CAS )
acetylchlorid (CAS )
 ethylacetát (CAS )
ethylacetát (CAS )
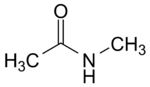 N-methylacetamid (CAS )
acetonitril (CAS )
N-methylacetamid (CAS )
acetonitril (CAS )
Tetravalentní organické funkce
 Methylchlorformiát (CAS )
Methylchlorformiát (CAS )
 2-buten-2-ol (CAS )
2-buten-2-ol (CAS )
Nenasycené deriváty
- Izokyanické ethery
Aromatické sloučeniny
Tyto aromatické sloučeniny obsahující kruh atomů uhlíku typu benzenu a podobně. Pokud kruh obsahuje jiný atom než uhlík, nazývá se to heterocyklus .
- Heterocykly
Jiné sloučeniny
Můžeme také citovat sloučeniny z jiných oborů souvisejících s organickou chemií:
- že polymery ;
- jsou organokovové sloučeniny .
Poznámky a odkazy
- Paul Arnaud, op. Cit. , str. 10
- Jean-Pierre Mercier, Philippe Godard, op. Cit. , str. 1 .
- Peter Atkins , Loretta Jones, op. Cit. , str. 15 .
- Jacques Angenault, op. cit. , str. 104
- Paul Arnaud, op. Cit. , str. 2
- Gerald Karp, Buněčná a molekulární biologie: koncepty a experimenty , De Boeck Supérieur,2010( číst online ) , s. 41.
- Peter Atkins , Loretta Jones, op. Cit. , str. 389 .
- Paul Arnaud, op. Cit. , str. 3
- V organické chemii je ionizace sloučenin vždy velmi omezená (Raymond Quelet, op. Cit. , P. 4 ).
- Existuje několik vzácných organických minerálů, zdroj: Claude GUILLEMIN , „ MINÉRALOGIE “, Encyclopædia Universalis [online], konzultováno 17. září 2014. URL: http://www.universalis.fr/encyclopedie/mineralogy/ .
- Raymond Quelet, op. cit. , str. 3
- Viz část „ definice úplnosti “
- Paul Arnaud, op. cit. , str. 1
- Text směrnice , článek 2, odstavec 16, na stránkách eur-lex.europa.eu .
- Oxid uhelnatý (CO), oxid uhličitý (CO 2 ). Další oxidy uhlíku, anorganické a organické, jsou uvedeny v tabulce v zápatí článku „ oxid uhelnatý “.
- Skupina organyl : "jakákoliv skupina, substituent organický, bez ohledu na jeho funkční skupiny , které mají valenční Free na atomu uhlíku" (Robert Panico et al. , Op cit.. , P. 59 , a (v) tohoto článku z Gold Book ).
- Robert Panico et al. , op. cit. , str. 52 , a (v) tohoto článku Gold Book .
- Maurice Bernard, op. cit. , str. 2 .
- Huheey, Keiter a kol. , op. cit , kapitola 15, s. 623 - Online prezentace - Číst online
Podívejte se také
Bibliografie
- Jacques Angenault (1995), La Chimie - encyklopedický slovník , 2 nd edition, Éditions Dunod ( ISBN 2100024973 )
- Paul Arnaud (1990), Organic Chemistry , 15 th edition, vysokoškolské studium , Editions Dunod ( ISBN 2040197168 )
- Jean-Pierre Mercier, Philippe Godard (1995), Organická chemie - zahájení , francouzský polytechnický a univerzitní tisk ( ISBN 2880742935 )
- Peter Atkins , Loretta Jones (1998), Chemie - molekuly, hmota, metamorfózy , 3 th vydání, Oxford University Press ( ISBN 2744500283 )
- Maurice Bernard (1994), hřiště v minerálním chemii , 2 nd edition, vysokoškolák úroveň , Éditions Dunod ( ISBN 2100020676 )
- Raymond Quelet (1964), Précis de chimie , sv. III - Organická chemie , kandidáti na vysvědčení o vyšších přípravných studiích , Presses Universitaires de France
- Robert Panico, Jean-Claude Richer, Jean Rigaudy (1996), Nomenklatura a terminologie v organické chemii , vydání technického inženýrství ( ISBN 2850590010 )
- Huheey, Keiter a kol. (1996), Anorganic Chemistry , De Boeck University ( ISBN 2804121127 )
- (en) Louis F. Fieser a Mary Fieser, Úvod do organické chemie , DC Heath and Company, Boston
- Donald J. Cram a George S. Hammond , Organic Chemistry , Gauthier-Villars , Paříž, 1965
- (pt) Geraldo Camargo de Carvalho, Química orgânica moderna (2 obj.), Livraria Nobel
- (pt) Arthur I. Vogel, Química orgánica qualitativa (3 obj.), Ao Livro Técnico, 1971
- (en) John H. Fletcher, Otis C. Dermer, Robert B. Fox, Nomenklatura organických sloučenin. Princip a praxe , Advances in Chemistry Series 126-1974
- A. Kurmann, Obecná organická chemie (3 obj.), Librairie Armand Colin, 1960