Argon
| Argon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Pevný a kapalný argon. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pozice v periodické tabulce | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | Ar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Příjmení | Argon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Protonové číslo | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doba | 3 e období | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | Blok p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rodina živlů | Vznešený plyn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronická konfigurace | [ Ne ] 3 s 2 3 p 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrony podle energetické hladiny | 2, 8, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti prvku | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomová hmotnost | 39,948 ± 0,001 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr (calc) | ( 71 hodin ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 106 ± 22 hodin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsův poloměr | 188 hod | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační stav | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kysličník | neznámý | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re : 15,759610 eV | 2 e : 27,62966 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 e : 40,74 eV | 4 e : 59,81 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 e : 75,02 eV | 6 th : 91.009 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 e : 124,323 eV | 8 e : 143 460 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 9 e : 422,45 eV | 10 e : 478,69 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 11 e : 538,96 eV | 12 e : 618,26 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 13 e : 686,10 eV | 14 e : 755,74 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 15 e : 854,77 eV | 16. th : 918,03 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 e : 4 120,8857 eV | 18 e : 4 426 2296 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nejstabilnější izotopy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednoduché tělesné fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Běžný stav | Plyn (nemagnetický) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
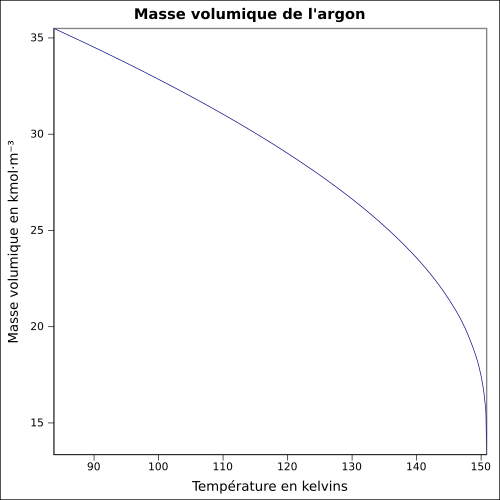
| Objemová hmotnost |
1,7837 g · L -1 ( 0 ° C , 1 atm ) rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalový systém | Tvář středověký | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Barva | bezbarvý | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fúzní bod | -189,36 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bod varu | -185,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fúzní energie | 1 188 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Odpařovací energie | 6,43 kJ · mol -1 ( 1 atm , -185,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritická teplota | -122,3 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trojitý bod | -189,3442 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární objem | 22,414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak páry |
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 319 m · s -1 až 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velké teplo |
520 J · kg -1 · K -1
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 0,01772 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozličný | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O Agentura | 100,028,315 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o EC | 231-147-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opatření | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Varování H280 a P403 H280 : Obsahuje plyn pod tlakem; při zahřátí může explodovat P403 : Uchovávejte na dobře větraném místě. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 NA, Odpověď : Kritická teplota stlačeného plynu = -122,4 ° C Zveřejnění na 1,0% podle klasifikačních kritérií |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doprava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : dusivý plyn nebo plyn, který nepředstavuje vedlejší riziko UN číslo : 1006 : KOMPRESOVANÝ ARGON Třída: 2.2 Klasifikační kód: 1A : Stlačený plyn, aspxiant; Štítek: 2.2 : nehořlavé, netoxické plyny (odpovídá skupinám označeným A nebo velkým O); 
22 : chlazený zkapalněný plyn, zadušený UN číslo : 1951 : CHLAZENÝ KAPALNÝ ARGON Třída: 2.2 Klasifikační kód: 3A : Chlazený zkapalněný plyn, zadušený; Štítek: 2.2 : nehořlavé, netoxické plyny (odpovídá skupinám označeným A nebo velkým O);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Argon je chemický prvek ze atomovým číslem 18 a symbolem Ar. Patří do skupiny 18 periodické tabulky a je součástí rodiny ze vzácných plynů , také nazýván „vzácné plyny“, který také zahrnuje hélium , tím neon , krypton , xenon a radon . Argon je 3 rd nejhojnější složkou zemské atmosféry , s hmotnostním zlomkem o 1.288%, což odpovídá objemové frakce o 0,934% (nebo 9340 ppm ), a je nejhojnější vzácných plynů na světě. " Zemská kůra , což odpovídá 1,5 ppm . Argon v zemské atmosféře se téměř úplně skládá z argonu 40 , je radiogenic nuklid vyplývající z rozpadu z draslíku 40 , zatímco argon pozorované v vesmíru je primárně skládá z argonu 36 , produkovaný hvězdné nucleosynthesis v supernov .
Jméno argon pochází ze starořeckého ἀργόν, což znamená „nečinný“, „líný“ [odvozeno z řeckého slova ἀεργός, vytvořeného z ἀ-εργός, což znamená „bez práce“, „nečinný“], s odkazem na skutečnost, že toto prvek je chemicky inertní. Jeho elektronická konfigurace představuje nasycenou valenční vrstvu na počátku její stability a virtuální nemožnosti vytvoření kovalentních vazeb . Teplota z 83.805 8 K jeho trojný bod je jedním z referenčních bodů Mezinárodní teplotní stupnice z roku 1990 (ITS-90).
Argon se vyrábí průmyslově pomocí frakční destilací ze zkapalněného vzduchu . Používá se především jako inertní atmosféra pro svařování a různé průmyslové procesy při vysoké teplotě zahrnující reaktivní látky. Argonová atmosféra se tedy používá v grafitových elektrických obloukových pecí, aby se zabránilo spalování ve druhé. Využívá také argon při osvětlení žárovkami , zářivkami a plynovými trubicemi . Používá se k výrobě modrozelených plynových laserů .
Hlavní vlastnosti
Argon je bezbarvý, bez zápachu, nehořlavý a netoxický v plynném, kapalném nebo pevném stavu. Jeho rozpustnost ve vodě je zhruba srovnatelná s rozpustností v kyslíku a je 2,5krát vyšší než v dusíku . Je chemicky inertní za téměř všech podmínek a při pokojové teplotě netvoří žádné potvrzené chemikálie .
Argon je však za určitých extrémních podmínek mimo rovnováhu schopen vytvářet chemické sloučeniny. Argon fluorohydrure Harf Takto se získá pomocí fotolýzy ultrafialovým z fluorovodíku HF v matrici kryogenní z jodid česný CSI a Ar atmosféře argonu; stabilní pod 27 K ( -246,15 ° C ), byl identifikován infračervenou spektroskopií . Fluorhydrid argonu je jediná známá sloučenina argonu, která je neutrální a stabilní v základním stavu .
Argon může také tvořit klatráty ve vodě, když jsou jeho atomy uvězněny v trojrozměrné mřížce tvořené ledem . Existují také polyatomické ionty obsahující argon, jako je argonhydridový kation ArH + , a exciplexy , jako například Ar 2* a ArF *. Různé sloučeniny s vazbami Ar C a Ar If stabilní byly předpovězeny numerickou simulací, ale nebyly syntetizovány v laboratoři.
Hlavní izotopy argonu přítomný v zemské kůře , jsou argonu 40 ( 40 Ar) na 99,6%, argon 36 ( 36 Ar) na 0,34% a v argon 38 ( 38 Ar) 0,06%. Draslíku-40 ( 40 K) rozpadá spontánně při rychlosti 11,2% v argonu 40 od elektronového záchytu nebo emisní tomografie a v množství 88,8% v vápníku 40 ( 40 Ca) o p rozpadu - s poločasem (polovina - život) 1,25 miliardy let. Tato doba trvání a poměr mezi vytvořenými vedlejšími produkty umožňuje určit stáří hornin metodou datování draslíkem a argonem .
V zemské atmosféře , argonu 39 je produkován především interakcí kosmického záření v atmosféře argonu 40 od záchytu neutronu následuje dvojité neutronové emise . V podloží může být také vyrobeno z draslíku 39 zachycením neutronů následovaným emisemi protonů .
Argonu 37 vzniká při podzemních testů z vápníku 40 od záchytu neutronu následným alfa rozpadu ; má poločas rozpadu 35 dní.
Argon je pozoruhodný v tom, že jeho izotopové složení se významně liší od jedné oblasti sluneční soustavy k druhé. Argon, jehož hlavním zdrojem je radioaktivní rozpad draslíku 40 ve skalách, sestává převážně z argonu 40 , jako na pozemských planetách udržujících atmosféru: Venuše , Země a Mars . Na druhou stranu, argon tvořený přímo hvězdnou nukleosyntézou je v podstatě tvořen argonem 36 produkovaným alfa reakcí , což je případ Slunce , jehož argon je podle měření slunečního větru 84,6% argonu 36 . Je to stejné na obřích planetách , kde je relativní počet izotopů 36 Ar: 38 Ar: 40 Ar 8400: 1600: 1.
Kromě pozemské atmosféry , která má objemový zlomek 0,934% argonu nebo 9 340 ppm , obsahuje atmosféra Merkuru 0,07 ppm , atmosféra Venuše 70 ppm a atmosféra Marsu 19 300 ppm , neboli 1,93%.
Převaha radiogenního argonu 40 v zemské atmosféře je zodpovědná za skutečnost, že atomová hmotnost argonu Země, v řádu 39,95 u , je o 0,85 u větší než u draslíku , což jej následuje v periodické tabulce prvků a jehož atomová hmotnost je řádově 39,10 u . To se zdálo paradoxní během objevu argonu v roce 1894, protože Dmitri Mendeleïev uspořádal svou periodickou tabulku podle rostoucí atomové hmotnosti, což vedlo k tomu, že musel být argon umístěn mezi draslík a vápník , s atomovou hmotností kolem 40, 08 u a zaměňován s to argonu do 0,13 u , zatímco mezi chlorem (35,45 u ) a draslíkem (39,10 u ) byl atomový hmotnostní rozdíl 3,65 u . Tento problém vyřešil Henry Moseley , který v roce 1913 prokázal, že periodická tabulka by měla být uspořádána podle rostoucího atomového čísla , a nikoli zvýšením atomové hmotnosti, což dalo prvky ve správném pořadí.
Atmosférický hojnosti vzhledem argonu ve srovnání s jinými vzácnými plyny - 9340 ppm z argonu, proti 5,24 ppm z helia , 18,18 ppm z neonu , 1,14 ppm z krypton a 0,087 ppm z xenonu - lze také připsat izotopů argonem 40 : argon 36 má skutečně hojnost pouze 31,5 ppm (0,337% z 9340 ppm ), stejného řádu jako u neonů (18,18 ppm ).
Sloučeniny
Argon atom má elektronový nasycený valenční skořepiny , s kompletní s a p podvrstvy . Díky tomu je tento prvek chemicky inertní a velmi stabilní, to znamená, že vytváří chemickou vazbu s jinými atomy jen velmi obtížně. Do roku 1962 byly vzácné plyny považovány za zcela inertní a nevhodné pro tvorbu chemických sloučenin ; k tomuto datu však syntéza xenon hexafluoroplatinátu XePtF 6 vydláždil cestu chemii vzácných plynů .
První sloučenina argonu s wolframovým pentakarbonylem chemického vzorce W (CO) 5 Ar, byla vydána v roce 1975, ale její skutečná existence zůstává sporná. V srpnu 1962 byl syntetizován na University of Helsinki argonu fluorohydride Harf pomocí fotolýzy ultrafialovým z fluorovodíku HF v matrici kryogenní z jodid česný CSI a Ar argonu stabilní sloučenině pod 27 K ( -246,15 ° C ), identifikovaného IČ spektroskopií . Tento objev vedl k myšlence, že argon může tvořit slabě vázané sloučeniny.
Dication metastable ARCf 22+ , izoelektronický s karbonylfluoridem COF 2a fosgen COCI 2z hlediska valenčních elektronů byla v roce 2009 pozorována implementace vazby uhlík -argon. Molekulární ion 36 ArH + , což odpovídá v argonu hydridu kationtu 36 (argonium), byl detekován v mezihvězdném na úrovni Krabí mlhoviny ; je to první sloučenina vzácného plynu detekovaná ve vesmíru .
Pevný hydrid argonu Ar (H 2 ) 2je van der Waalsovy sloučeniny mající stejnou krystalovou strukturu jako fáze Lavesovy (en) MGZN 2. Tvoří při tlaku mezi 4,3 a 220 GPa , i když výsledky získané Ramanovy spektroskopie ukazují, že H 2 molekulysloučeniny Ar (H 2 ) 2disociují nad 175 GPa .
Průmyslová výroba a aplikace
Argon se vyrábí průmyslově pomocí frakční destilací ze zkapalněného vzduchu v jednotkách kryogenních na destilaci vzduchu (v) , metoda pro oddělování kapalného dusíku , který vře při 77,3 K , argonu, jehož teplota varu je 87,3 K , a kapalného kyslíku , který vře při 90.2 K . Světová produkce argonu je řádově 700 000 tun ročně.
Argon má několik zajímavých vlastností, které ospravedlňují jeho průmyslové využití:
- je to chemicky inertní plyn;
- je to levná alternativa, když dusík není dostatečně inertní;
- má nízkou tepelnou vodivost (jedná se tedy o tepelný izolátor );
- jeho elektronické vlastnosti ( ionizace , emisní spektrum ) se používají v určitých osvětlovacích aplikacích.
Jiné vzácné plyny vykazují podobné vlastnosti a mohly by být také použity, ale argon je zdaleka nejlevnější ze všech, získává se jako vedlejší produkt extrakce kyslíku a dusíku ze vzduchu kryogenní frakční destilací.
Průmyslové aplikace
Argon se používá v určitých vysokoteplotních průmyslových procesech, ve kterých se chemicky inertní látky stávají reaktivními. Argonová atmosféra se tedy používá v elektrických pecích s grafitovými elektrodami za účelem, aby se zabránilo spalování tohoto materiálu.
U některých z těchto procesů by přítomnost dusíku nebo kyslíku způsobila vady materiálu. Argon se používá při určitých typech obloukového svařování, jako je plynové obloukové svařování a TIG svařování , stejně jako při ošetřování činidel titanu a dalších prvků . Krystaly křemíku a germania určené pro polovodičový průmysl se také pěstují v argonové atmosféře, aby byla zajištěna jejich krystalická kvalita.
Argon se používá v drůbežářském průmyslu jako metoda inertního zadušení plynu k udusit na drůbež , a to buď s hmotnostním porážku po nástupu onemocnění nebo jako prostředek k střídavého porážky na electronarcosis . Relativní hustota argonu vůči vzduchu způsobuje, že při plynování zůstává blízko země. Díky své nereaktivní povaze je kompatibilní s potravinářskými produkty a skutečnost, že částečně nahrazuje kyslík v tkáních, prodlužuje trvanlivost potravin.
Argon se někdy používá k hašení požárů konzervováním cenných zařízení, jako jsou počítačové servery , které by se poškodily použitím vody nebo pěny.
Lékařské aplikace
Procedury kryochirurgie (in), jako je kryoablace (in), používají kapalný argon ke zničení tkání, jako jsou rakovinné buňky . Bylo možné jej použít v postupu nazývaného argonu zvýšenou koagulaci , což je forma elektrochirurgických (v) od plazmového hořáku , který však představuje riziko plynové embolie materializované smrtí alespoň jednoho pacienta.
Argon modré lasery se používají v chirurgii pro šití na tepny , zničit nádory v oční chirurgii , nebo elektrokoagulace přes endoskopickou úředníků lézí gastrointestinálního krvácení.
Argon byl testován také nahradit dusíku v dýchacím plynu zvaného Argox za účelem urychlení odstranění rozpuštěného dusíku z krve .
Vědecký výzkum
Kapalný argon se používá jako cíl pro detekci neutrin a výzkum temné hmoty . Interakce mezi hypotetickým wimps a jader z argonu atomů by měla produkovat pozorovatelnou scintilační pomocí fotonásobiče . Dvoufázové detektory obsahující plyn argon se používají k detekci elektronů produkovaných ionizací během interakcí jádra WIMP-argon.
Stejně jako ostatní zkapalněné vzácné plyny má kapalný argon vysokou scintilační rychlost (přibližně 51 fotonů / keV ), je transparentní vůči své vlastní scintilaci a relativně snadno se čistí. Je levnější než xenon a má odlišný scintilační časový profil, což umožňuje odlišit elektronické interakce od jaderných. Bylo však silnější radioaktivity beta vzhledem k výskytu v atmosféře argonu 39 , až na použití argonu ze suterénu Země ochuzený o 39 Ar, jejíž poločas je pouze 269 rok a jejichž stock není rekonstituovány 40 Ar ( n , 2 n ) 39 Ar interakce z kosmického záření na atmosférický argonem .
V jiném registru byl argon 39 používán zejména k dnešnímu dni podzemních vod a ledových jader v Antarktidě . K-Ar datování a argon-argon datování se také používají pro radiometrického datování z sedimentární , metamorfované a magmatická .
Konzervativní
Argon, číslo E938 , se používá jako konzervant potravin k odstranění kyslíku a vlhkosti z atmosféry v obalech a ke zpoždění jeho doby použitelnosti . Oxidace vzduchem, k hydrolýze a další reakce , které degradují produkt, se tedy k oddálení nebo zcela zablokována. Chemická činidla a farmaceutické molekuly jsou někdy baleny v atmosféře argonu. Tento vzácný plyn se také používá jako konzervační prostředek pro laky , polyuretan nebo dokonce barvy .
Argon se také používá při výrobě vína k ochraně vína před kyslíkem a prevenci jeho oxidace a také proti nežádoucím bakteriálním interakcím (zejména bakteriím octovým , které produkují kyselinu octovou a mění víno na ocet ). Může být také použit jako hnací plyn pro spreje .
Laboratorní vybavení
Argon lze použít jako inertní plyn do vakuového potrubí a přihrádky na rukavice ; je upřednostňován před dusíkem , který je levnější, protože dusík je schopen reagovat s obzvláště reaktivními sloučeninami, stejně jako s určitým zařízením. Kromě toho má argon tu výhodu, že je na rozdíl od dusíku hustší než vzduch, což usnadňuje jeho použití v praxi.
Argon lze použít jako nosný plyn při plynové chromatografii a při elektrosprejové ionizaci . Je to plyn zvolený pro plazmu používanou v indukčně vázané plazmové spektrometrii . Argon se přednostně používá při nanášení rozprašováním (In) na vzorky, které mají být zkoumány skenovací elektronovou mikroskopií, a pro čištění destiček v mikrofabrikaci .
Osvětlení
Žárovka je obvykle naplněna argonem, aby byla zachována její vlákno z vysokoteplotního oxidaci . Argon se také používá pro své záření ionizací , jako v plazmových lampách a kalorimetrech ve fyzice částic . Výbojky plněné čistý argon produkují světlo světle fialový tažné lebleu levandule, který se stává modré přidáním malého rtuť .
Argon se také používá pro iontové lasery (v) modré a zelené.
Různé aplikace
Argon se používá jako tepelný izolátor pro dvojitá zasklení . Díky své chemické inertnosti a nízké tepelné vodivosti se také používá k plnění suchých obleků pro potápění .
Argon je jedním z plynů, které lze použít v astronautice jako hnací plyn pro VASIMR . V oblasti vzduchových zbraní se používá pod tlakem k ochlazení, uvolněním, hlav některých raket typu vzduch-vzduch , včetně raket AIM-9 Sidewinder .
Argon byl použit v atletice jako dopant simulující hypoxii . Byl proto spolu s xenonem zařazen na seznam metod a látek zakázaných Světovou antidopingovou agenturou v roce 2014, než byl v roce 2020 stažen.
Historie a etymologie
Slovo argon pochází ze starořeckého ἀργός / argós („nečinný“, „líný“, „sterilní“), tvořený soukromou řeckou předponou ἀ a slovem ἔργον / ergon („práce“), tato etymologie evokuje inertní charakter prvku.
Henry Cavendish předpokládal přítomnost chemicky inertního plynu ve vzduchu již v roce 1785, ale jeho objev lorda Rayleigha a sira Williama Ramsaye na University College London počkal až do roku 1894 . Udělali to tak, že ze vzorku čistého vzduchu odstranili kyslík , oxid uhličitý , vodní páru a dusík a zanechali inertní plyn, kterému říkali argon . Tito dva vědci oficiálně oznámili svůj objev Královské společnosti dne31. ledna 1895.
Na trať je postavila skutečnost, že chemicky vyrobený dusík byl o 0,5% lehčí než dusík extrahovaný ze vzduchu odstraněním dalších v té době známých atmosférických plynů. Frakční destilace zkapalněného vzduchu jim umožnilo produkovat významné množství argonu v roce 1898 a současně izolovat dvě další vzácné plyny neon a xenon .
Argon byl také pozorován v roce 1882 během nezávislé práce HF Newall a WN Hartley, kteří zaznamenali spektrální čáry v emisním spektru vzduchu neodpovídající žádnému známému chemickému prvku .
Chemická značka pro argonu byl až do roku 1957, kdy se stala Ar.
Nebezpečí
Stejně jako helium není argon při nízkých koncentracích nebezpečný. Je však o 38% hustší než vzduch a vdechnutí velkého množství argonu s sebou nese riziko udušení nedostatkem kyslíku ( anoxie ); k tomu může dojít například při svařování v omezeném prostoru.
Poznámky a odkazy
- (in) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia a Santiago Barragan Alvarez , „ Covalent radii revisited “ , Dalton Transactions ,2008, str. 2832 - 2838 ( DOI 10.1039 / b801115j )
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , TF-CRC,2006, 87 th ed. ( ISBN 0849304873 ) , s. 10-202
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Vázaná kniha ( ISBN 978-1-420-09084-0 )
- (en) Robert H. Perry a Donald W. Green , Perryho Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- Zápis z Mezinárodní výbor pro míry a váhy , 78 th zasedání, 1989, pp. T1-T21 (a str. T23-T42, anglická verze).
- Databáze Chemical Abstracts dotazovaná prostřednictvím SciFinder Web 15. prosince 2009 ( výsledky vyhledávání )
- Zápis čísla CAS „7440-37-1“ do chemické databáze GESTIS IFA (německý orgán odpovědný za bezpečnost a ochranu zdraví při práci) ( německy , anglicky ), přístup 30. ledna 2009 (vyžadován JavaScript)
- „ Argon “ v databázi chemických produktů Reptox z CSST (quebecká organizace odpovědná za bezpečnost a ochranu zdraví při práci), přístup k 25. dubnu 2009
- (in) Markku Räsänen , „ Argon out of air “ , Nature Chemistry , sv. 6, n o 1, Leden 2014Článek n o 82 ( PMID 24345939 , DOI 10,1038 / nchem.1825 , číst on-line )
- (cs) Leonid Khriachtchev, Mika Pettersson, Nino Runeberg, Jan Lundell a Markku Räsänen , „ Stabilní argonová sloučenina “ , Nature , sv. 406, n O 6798, 24. srpna 2000, str. 874-876 ( PMID 10972285 , DOI 10.1038 / 35022551 , Bibcode 2000Natur.406..874K , číst online )
- (in) VR Belosludov OS Subbotin DS Krupskii, Prokuda OV, RV a Y. Belosludov Kawazoe , „ Mikroskopický model klatrátových sloučenin “ , Journal of Physics: Conference Series , Vol. 29, n o 1, ledna 2006, str. 1-7 ( DOI 10.1088 / 1742-6596 / 29/1/001 , Bibcode 2006JPhCS..29 .... 1B , číst online )
- (in) Arik Cohen, Jan Lundell a R. Benny Gerber , „ První sloučeniny s chemickými vazbami argon-argon a uhlík-křemík “ , Journal of Chemical Physics , sv. 119, n o 13, Říjen 2003, str. 6415-6417 ( DOI 10.1063 / 1.1613631 , Bibcode 2003JChPh.119.6415C , číst online )
- (en) J. Emsley, Nature's Building Blocks , Oxford University Press, 2001, s. 1. 44–45 . ( ISBN 978-0-19-960563-7 )
- Etienne Roth ( r. ), Bernard Poty ( r. ), Robert Delmas et al. ( pref. Jean Coulomb ), Metody datování přírodními jadernými jevy , Paris, Éditions Masson , kol. " CEA Collection ",1985, 631 s. ( ISBN 978-2-225-80674-2 , upozornění BnF n o FRBNF34836710 ) , kap. 17 („Křemík 32 a argon 39“)
- (in) Věda pro 37 Ar jako monitor podzemních jaderných výbuchů , strana 1, 2010
- (in) Katharina Lodders , „ The Solar Abundance Argon “ , The Astrophysical Journal , sv. 674, n o 1, 10.02.2008, str. 607-611 ( DOI 10.1086 / 524725 , Bibcode 2008ApJ ... 674..607L , arXiv arXiv: 0710.4523 , číst online )
- (in) AGW Cameron , „ Elementární a izotopické nadbytky těkavých prvků na vnějších planetách “ , Space Science Reviews , sv. 14, n kost 3-4, Březen 1973, str. 392-400 ( DOI 10.1007 / BF00214750 , Bibcode 1973SSRv ... 14..392C , číst online )
- (in) Marco Fontani , Mariagrazia Costa a Mary Virginia Orna , The Lost Elements: The Periodic Table's Shadow Side , New York, Oxford University Press ,2015( 1 st ed. 2014), 531 str. ( ISBN 9780199383344 ) , s. 182.
- (in) Neil Bartlett , „ Xenon hexafluoroplatinate Xe + [PtF 6 ] - " , Proceedings of the Chemical Society , n O 6,Června 1962, str. 197-236 ( DOI 10.1039 / PS9620000197 , číst online )
- (in) Nigel A. Young , „ Hlavní skupina koordinační chemie při nízké teplotě: Přehled matricových komplexů skupiny 12 až skupiny 18 “ , Coordination Chemistry Reviews , sv. 257 n kostí 5-6, Březen 2013, str. 956-1010 ( DOI 10.1016 / j.ccr.2012.10.013 , číst online )
- (in) Neil Bartlett , „ Vznešené plyny “ , Chemical & Engineering News , sv. 81, n o 36, 08.09.2003, str. 32-34 ( DOI 10.1021 / cen-v081n036.p032 , číst online )
- (in) Jessica F. Lockyear Kevin Douglas, Stephen D. Price, Małgorzata Karwowska, Karol J. Fijalkowski Wojciech Grochala Marek Remeš Jana Roithová a Detlef Schroeder , „ Generace ARCf 2 2+ Dication “, The Journal of Physical Chemistry Letters ,sv. 1,n o 1,8. prosince 2009, str. 358-362 ( DOI 10.1021 / jz900274p , číst online )
- (en) J. Barlow, BM Swinyard, PJ Owen, J. Cernicharo, HL Gomez, RJ Ivison, O. Krause, TL Lim, M. Matsuura, S. Miller, G. Olofsson a AND Polehampton , „ Detection of a Molekulární ionty ušlechtilého plynu, 36 ArH + , v Krabí mlhovině “ , Science , sv. 342, n O 6164, 13. prosince 2013, str. 1343-1345 ( PMID 24337290 , DOI 10.1126 / science.1243582 , Bibcode 2013Sci ... 342.1343B , číst online )
- (in) Annette K. Kleppe, Mónica Amboage a Andrew P. Jephcoat , „ Nová vysokotlaká van der Waalsova směs Kr (H 2) 4 objeven v binárním systému krypton-vodík “ , Scientific Reports , sv. 4,16. května 2014, Článek n o 4989 ( DOI 10,1038 / srep04989 , bibcode 2014NatSR ... 4E4989K , číst on-line )
- „ Periodická tabulka prvků: Argon - Ar “ , Environmentalchemistry.com (přístup 12. září 2008 )
- (in) Sara J. Shields a ABM Raj , „ Kritický přehled elektrických omračovacích systémů ve vodních lázních pro porážku drůbeže a nedávný vývoj v alternativních technologiích “ , Journal of Applied Animal Welfare Science , sv. 13, n O 4, 2012, str. 281-299 ( PMID 20865613 , DOI 10.1080 / 10888705.2010.507119 , číst online )
- DL Fletcher , „ Slaughter Technology, “ Symposium: Nedávné pokroky v technologii zabití drůbeže ,1999( Přečtěte si on-line , přístupný 1 st 01. 2010 )
- (in) MJ Fraqueza a AS Barreto , „ Efektem je trvanlivost krůtího masa v obalech s upravenou atmosférou s argonovou směsí “ , Poultry Science , sv. 88, n o 9, Září 1999, str. 1991-1998 ( PMID 19687286 , DOI 10.3382 / ps.2008-00239 , číst online )
- (in) Joseph Z. Su, Andrew K. Kim, George P. Crampton a Zhigang Liu , „ Potlačení požáru s inertními plyny “ , Journal of Fire Protection Engineering , sv. 11, n O 2 2001, str. 72 - 87 ( DOI 10,1106 / X21V-YQKU-PMKP-XGTP , číst on-line )
- (in) „ Embolie fatálních plynů způsobená přetlakem během laparoskopického použití koagulace vylepšené argonem “ , Health Devices , sv. 23, n O 6, Červen 1994, str. 257-259 ( číst online )
- (in) Jerome Canady , Kimberly Wiley a Biagio Ravo , „ koagulace argonové plazmy a budoucí aplikace pro endoskopické sondy Dual-Mode “ , Recenze v Gastroenterologické poruchy , sv. 6, n o 1,2006, str. 1-12 ( ISSN 1533-001X , PMID 16520707 , čtení online , přístup 9. října 2017 ).
- (in) Andrew A Pilmanis Ulf I. Balldin, James T. Webb a Kevin M. Krause , „ Staged Decompression to 3.5 Psi Using Argon-Oxygen and Oxygen Breareat 100% Mixtures “ , Aviation, Space, and Environmental Medicine , flight. 74, N O 12 prosince 2003, str. 1243-1250 ( PMID 14692466 , číst online )
- (in) Dan Gastler Ed Kearns, Andrew Hime, Laura C. Stonehill Stan Seibert, Josh Klein, Hugh W. Lippincott, Daniel N. McKinsey a James A. Nikkel , „ Měření účinnosti scintilace pro jaderný zpětný ráz v kapalném argonu “ , Physical Review C , sv. 85, n O 6, 27. června 2012, Článek n o 065811 ( DOI 10,1103 / PhysRevC.85.065811 , bibcode 2012PhRvC..85f5811G , arXiv 1004,0373 , číst on-line )
- (in) J.Xu F. Calaprice, C. Galbiati, A. Goretti Guray G., T. Hohman, D. Holtz, An. Ianni, Mr. Laubenstein, Loer B., C. Lovec, CJ Martov, D Montanari, S. Mukhopadhyay, A. Nelson, SD Rountree, RB Vogelaar a A. Wright , „ Studie obsahu stopového 39 Ar v argonu z hlubin podzemních zdrojů “ , Astroparticle Physics , sv. 66, června 2015, str. 53-60 ( DOI 10.1016 / j.astropartphys.2015.01.002 , Bibcode 2015APh .... 66 ... 53X , arXiv 1204.6011 , číst online )
- Paul Depovere, Periodická tabulka prvků. Základní zázrak vesmíru , De Boeck Supérieur ,2002, str. 98.
- (cs) Henry Cavendish , „ XXIII. Experimenty na vzduchu. “ , Philosophical Transactions of the Royal Society of London , sv. 75, 1785, str. 372-384 ( DOI 10.1098 / rstl.1785.0023 , Bibcode 1785RSPT ... 75..372C , číst online )
- (in) Robert John Strutt a William Ramsay , „ I. Argon, nová forma atmosféry “ , Proceedings of the Royal Society of London , sv. 57, 1895, str. 265-287 ( DOI 10.1098 / rspl.1894.0149 , JSTOR 115394 , číst online )
- (in) John William Strutt a William Ramsay , „ VI. Argon, nová složka atmosféry ” , Philosophical Transactions of the Royal Society of London , 1895, str. 187-241 ( DOI 10.1098 / rsta.1895.0006 , JSTOR 90645 , Bibcode 1895RSPTA.186..187R , číst online )
- (in) Sir William Ramsay, „ Vzácné plyny atmosféry “ , https://www.nobelprize.org/ , Nobelova cena za chemii , 12. prosince 1904(přístup 14. června 2020 ) .
- (in) John H. Holloway, chemie ušlechtilých plynů , Methuen,1968, str. 6
- (in) John Emsley, Nature's Building Blocks: An AZ Guide to the Elements , Oxford University Press, 2003, s. 1. 36 . ( ISBN 0198503407 )
- (in) Norman E. Holden, „ Historie původu chemických prvků a jejich objevitelů “ , 41. Valné shromáždění IUPAC v Brisbane, Austrálie 29. června - 8. července 2001 , na adrese https: //www.nndc.bnl. gov / , Národní centrum pro jaderná data , 12. března 2004(přístup 14. června 2020 ) .
Podívejte se také
Související články
externí odkazy
- (en) „ Technické údaje pro Argon “ (přístup k 24. dubnu 2016 ) , se známými údaji pro každý izotop na podstránkách
- (In) Obrázky argonu v různých formách
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Ahoj | |||||||||||||||||||||||||||||||
| 2 | Li | Být | B | VS | NE | Ó | F | narozený | |||||||||||||||||||||||||
| 3 | N / A | Mg | Al | Ano | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K. | Že | Sc | Ti | PROTI | Cr | Mn | Fe | Spol | Nebo | Cu | Zn | Ga | Ge | Eso | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Pozn | Mo | Tc | Ru | Rh | Pd | Ag | CD | v | Sn | Sb | Vy | Já | Xe | |||||||||||||||
| 6 | Čs | Ba | The | Tento | Pr | Nd | Odpoledne | Sm | Měl | Gd | Tb | Dy | Ho | Er | Tm | Yb | Číst | Hf | Vaše | Ž | D | Kost | Ir | Pt | V | Hg | Tl | Pb | Bi | Po | V | Rn | |
| 7 | Fr. | Ra | Ac | Čt | Pa | U | Np | Mohl | Dopoledne | Cm | Bk | Srov | Je | Fm | Md | Ne | Lr | Rf | Db | Sg | Bh | Hs | Mt. | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Alkalické kovy |
Alkalická země |
Lanthanidy |
Přechodné kovy |
Špatné kovy |
kovově loids |
Nebankovní kovy |
halo geny |
Ušlechtilé plyny |
Položky nezařazené |
| Aktinidy | |||||||||
| Superaktinidy | |||||||||