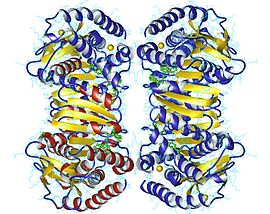
Malát dehydrogenáza
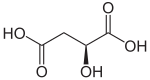
Malát dehydrogenáza ( MDH ) je oxidoreduktázy z Krebsova cyklu , který katalyzuje na reakci :
|
+ NAD + NADH + H + + |

|
| L- malát | Oxaloacetát |
Tento enzym se účastní několika hlavních metabolických cest , včetně Krebsova cyklu .
Malát dehydrogenáza| Č. ES | ES |
|---|---|
| Číslo CAS |
| IUBMB | Vstup IUBMB |
|---|---|
| IntEnz | IntEnz pohled |
| BRENDA | Vstup BRENDA |
| KEGG | Vstup KEGG |
| MetaCyc | Metabolická cesta |
| PRIAM | Profil |
| PDB | Struktury |
| JÍT | AmiGO / EGO |
Izoformy
Tyto prokaryotes mít jeden tvar, ale všechny eukaryotes mají alespoň dvě izoformy , jeden v cytosolu a další v mitochondriální matrix . Tyto houby a rostliny mají rovněž specifický tvar, aby glyoxisome , který je zapojen do glyoxylátu cyklu . Rostliny mají čtvrtou specifickou formu pro chloroplasty a na NADP + , malátdehydrogenázu NADP + ( EC ) , která se podílí na Calvinově cyklu , fixaci uhlíku v C4a metabolismus kyseliny crassulacean .
Nakonec archaea obsahuje malátdehydrogenázu úzce související s laktátdehydrogenázou .
Biochemie
Malátdehydrogenáza nastane nejprve v Krebsově cyklu , kde oxid je L -malátová v oxalacetátu . Ta může být dále kondenzován s acetyl-CoA o citrát syntázy zahájit nové kolo Krebsova cyklu.
Podílí se také na glukoneogenezi , v jejích mitochondriálních a cytosolických formách . Pyruvát může být skutečně převedeny na oxalacetát podle pyruvátkarboxyláza , který je snížení o L -malátová podle malátdehydrogenáza mitochondriální zatímco běží v opačném směru do Krebsova cyklu: -malátová může opustit mitochondrie dosáhnout cytosolu a je zde opět oxiduje na oxaloacetát cytosol-malátdehydrogenázou. Oxaloctan se potom převede na fosfoenolpyruvát podle fosfoenolpyruvát karboxykinázy (PEPCK).
Mitochondriální forma se také podílí na kyvadlové dopravě malát-aspartát , která je nezbytná pro buněčné dýchání .
Struktura a katalytický mechanismus
Malát dehydrogenáza se vyskytuje u většiny živých tvorů jako homodimerní protein úzce příbuzný strukturou s laktátdehydrogenázou . Je to velká molekula, jejíž podjednotky mají hmotnost 30 až 35 kDa . Peptidová sekvence z těchto enzymů vede k prokázání, že se rozcházely do dvou fylogenetických skupin : na mitochondriální izoenzymů na jedné straně, a cytosolické a chloroplastový izoenzymů na straně druhé. Tato pozorování podporují endosymbiotickou teorii, že mitochondrie a chloroplasty se vyvinuly uvnitř eukaryotických buněk z předků prokaryot . Kromě toho je peptidová sekvence malátdehydrogenázy archaea podobná sekvenci laktátdehydrogenázy jako sekvence malátdehydrogenázy z jiných organismů, což ilustruje vztah mezi laktátdehydrogenázou a malátdehydrogenázou.
Každá podjednotka dimerů malátdehydrogenázy má dvě odlišné domény, které se liší strukturou a funkčností. Každá doména přijímá paralelní strukturu β-listů se čtyřmi β-listy a α-šroubovicí obsahující centrální vazebné místo NAD + . Podjednotky jsou navzájem spojeny četnými vodíkovými vazbami a hydrofobními interakcemi.
Aktivní místo z malátdehydrogenáza je hydrofobní dutina zahrnuty v proteinu, ve kterém jsou specifická vazebná místa na podkladu a na jeho koenzym , NAD + . V aktivním stavu je enzym podléhá konformační změnu, která uzavírá substrát, aby se minimalizovalo jejich vystavení rozpouštědla a umístěnou v blízkosti substrátu na zbytky z aminokyselin katalytické klíčů. Tři zbytky, které zahrnují katalytickou triádu, jsou na jedné straně His195 a Asp168 , které oba fungují jako systém přenosu protonu, a zbytky Arg102 , Arg109 a Arg171 , které vážou substrát. Kinetické studie ukázaly, že enzymatická aktivita malátdehydrogenázy je sekvenována: NAD + / NADH se váže před substrátem.
Poznámky a odkazy
- Hodnoty hmotnosti a počtu zbytků zde uvedeno, jsou ty, které v prekurzorového proteinu vyplývající z překladu z genu , před posttranslačních modifikací , a mohou se výrazně liší od odpovídajících hodnot pro funkční protein .
- (in) P. Minárik N. Tomášková, M. a M. Kollárová Antalík , „ malátdehydrogenáza - struktura a funkce “ , General Physiology and Biophysics , Vol. 21, n o 3, Září 2002, str. 257-265 ( PMID 12537350 , číst online )
- (in) RA Musrati M. Kollárová, N. a D. Mernik Mikulášová , „ malate dehydrogenase: distribution, function and properties “ , General Physiology and Biophysics , Vol. 17, n o 3, Září 1998, str. 193-210 ( PMID 9834842 , číst online )
- (in) Lee McAlister-Henn , „ Evoluční vztahy mezi malátdehydrogenázou “ , Trends in Biochemical Sciences , sv. 13, n o 5, Květen 1988, str. 178-181 ( PMID 3076279 , DOI 10.1016 / 0968-0004 (88) 90146-6 , číst online )
- (in) Fabrice Ash Lad, Jadwiga Chroboczek Giuseppe Zaccai, Henryk Eisenberg a Moshe Mevarech , „ Klonování, sekvenování a exprese genu kódujícího malát dehydrogenázu extrémně halofilní archaebakterie Haloarcula marismortui v Escherichia coli “ , Biochemistry , sv. 32, n o 16, 27.dubna 1993, str. 4308-4313 ( PMID 8476859 , DOI 10.1021 / bi00067a020 , číst online )
- (in) Michael D. Hall, David G. Levitt a Leonard J. Banaszak , „ Krystalová struktura malátdehydrogenázy Escherichia coli : komplex apoenzymu a citrátu v rozlišení 1,87 Å “ , Journal of Molecular Biology , sv. 226, n o 3, 5. srpna 1992, str. 867-882 ( PMID 1507230 , DOI 10.1016 / 0022-2836 (92) 90637-Y , číst online )
- (in) Victor S. Lamzin Zbigniew Dauter a Keith S. Wilson , „ Dehydrogenace zrcadlem “ , Nature Structural Biology , sv. 1, n o 5, Květen 1994, str. 281-282 ( PMID 7664032 , DOI 10.1038 / nsb0594-281 , číst online )
- (in) Thomas B. Shows, Verne Chapman a Frank H. Ruddle , „ Mitochondriální malát dehydrogenáza a jablečný enzym: Mendelovy zděděné elektroforetické varianty u myší “ , Biochemical Genetics , sv. 4, n o 6, Prosinec 1970, str. 707-718 ( PMID 5496232 , DOI 10.1007 / BF00486384 , číst online )