Oxid dusnatý
| Oxid dusnatý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Molekula oxidu dusnatého |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Název IUPAC | Oxid dusnatý | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o ECHA | 100 030 233 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o EC | 233-271-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC kód | R07 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 145068 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ÚSMĚVY |
N = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / HNO / c1-2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | bezbarvý stlačený plyn. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hrubý vzorec |
N O [izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární hmotnost | 30,0061 ± 0,0005 g / mol N 46,68%, O 53,32%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolární moment | 0,15872 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T. fúze | -163,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° vroucí | -151,8 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpustnost | ve vodě při 0 ° C : 7,4 ml / 100 ml | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objemová hmotnost |
1,3 kg · l -1 (kapalina)
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak nasycených par |
rovnice:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritický bod | 65,8 bar , -93,35 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 325 m · s -1 ( 10 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 plyn, 1 bar | 211 J / Mol K. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 plyn | 90,29 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 kapalina | 87,7 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 13,83 kJ · mol -1 ( 1 atm , -151,74 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C str |
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionizační energie | 9,26438 ± 0,00005 eV (plyn) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opatření | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    A, C, D1A, E, : Stlačený plyn kritická teplota = -93 ° C, C : Oxidační materiál příčiny nebo podporuje spalování jiného materiálu uvolněním kyslíku D1a : velmi toxický materiál, který má vážné okamžité účinky pro přepravu nebezpečných věcí: třída 2,3 E : nerezavějícího materiálu pro přepravu nebezpečných věcí : třída 8 Zveřejnění na 1,0% podle seznamu zveřejnění přísad |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Směrnice 67/548 / EHS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 T +  VS  Ó Symboly : T + : Vysoce toxický C : Žíravý O : Oxidující R věty : R8 : Kontakt s hořlavým materiálem může způsobit požár . R26 : Vysoce toxický při vdechování. R34 : Způsobuje popáleniny. Světy : S9 : Uchovávejte obal na dobře větraném místě. S17 : Chraňte před hořlavým materiálem. S26 : V případě zasažení očí okamžitě důkladně vypláchněte vodou a vyhledejte odborníka. S28 : Po kontaktu s kůží okamžitě a hojně omyjte… (vhodné výrobky uvede výrobce). S45 : V případě nehody nebo pokud se necítíte dobře, okamžitě vyhledejte lékařskou pomoc (je-li to možné, ukažte štítek). S36 / 37/39 : Noste vhodný ochranný oděv, rukavice a ochranu očí / obličeje. R věty : 8, 26, 34, S-věty : 9, 17, 26, 28, 36/37/39, 45, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doprava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
265 : jedovatý a oxidační plyn (podporuje požár) UN číslo : 1660 : OXID DUSIČNÝ, STLAČENÝ; nebo OXID DUSIČNÝ, STLAČENÝ Třída: 2.3 Štítky: 2.3 : Toxické plyny (odpovídá skupinám označeným velkým T, tj. T, TF, TC, TO, TFC a TOC). 5.1 : Oxidační látky 8 : Žíravé látky    |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalace | Nebezpečný, může vést k smrti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kůže | Dráždivý | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oči | Může způsobit podráždění | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Požití | Používá se k terapeutickým účelům, ale má vedlejší účinky a je při předávkování nebezpečný | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoxikologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prahová hodnota zápachu | nízká: 0,29 ppm vysoká: 0,97 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Oxid dusnatý , oxid dusnatý , oxid dusnatý nebo NO je chemická sloučenina vytvořen z atomu z kyslíku a atomu dusíku . Je to plyn za normálních podmínek teploty a tlaku . Je to důležitý neurotransmiter u savců ; rozpuštěný, snadno prochází biologickými membránami a přechází z jedné buňky do druhé, což představuje „ideálního parakrinního posla“ .
Oxid dusnatý (NO) by neměl být zaměňován s jinými oxidy dusíku , jako je oxid dusný N 2 O, kterému se říká „smějící se plyn“ a který je celkovým anestetikem , nebo znovu, jako je oxid dusičitý NO 2 , extrémně dráždivý a škodlivý červenohnědý plyn, který vzniká rychlou oxidací NO kyslíkem ve vzduchu.
Jeho velká reaktivita (zejména v rozpustné fázi) vůči radikálovým sloučeninám, jako je molekulární kyslík - což je biradikál - nebo superoxidový anion, je způsobena skutečností, že je sama radikálovou sloučeninou - jeho spinová elektronika je 1/2. V biologickém prostředí se jeho poločas odhaduje na 1 až 5 sekund nebo dokonce 30 sekund. Získané peroxynitrity jsou silná oxidační a nitrační činidla. To vysvětluje všudypřítomné účinky, které dosud nejsou dobře pochopeny, od imunitní odpovědi přes mikrobiální záchvaty a zánětlivé procesy až po septický šok a neuronální smrt ve fázi ischemie . Podílí se také na buněčných mechanismech učení paměti nebo na fenoménu erekce .
Výroba a vlivy na životní prostředí
Tento plyn může být syntetizován v malém množství mnoha organismy, včetně lidského těla.
V přírodě při vysoké teplotě dusík a kyslík reagují za vzniku oxidu dusnatého, například působením blesku .
Lidská činnost zásadně změnila produkci oxidu dusnatého v biosféře , vzhledem k tvorbě velkého množství tohoto plynu ve spalovací komoře ze spalovacích motorů , v některých kotlů a průmyslových motorů a v některých procesů chemického průmyslu . Jedním z cílů katalytických konvertorů výfukových plynů je zvrátit tuto reakci a snížit emise tohoto plynu.
Vlastnosti
Chemické vlastnosti oxidu dusnatého jsou velmi četné. Následuje stručný přehled metod přípravy a odezvy.
Příprava
Oxid dusnatý se tvoří z prvků při vysoké teplotě, jak je uvedeno výše.
Může být syntetizován v laboratoři podle následujících oxidačně-redukčních reakcí, kdy se na dusíkatý derivát se stupněm oxidace vyšším než + II (kyselina dusičná: + V; kyselina dusitá: + III) působí příslušným redukčním činidlem. Všechny tyto reakce musí být prováděny v nepřítomnosti kyslíku, protože ten rychle oxiduje NO na oxid dusičitý. :
Tedy redukce kyseliny dusičné zředěné mědí
8 HNO 3 + 3 Cu → 3 Cu (NO 3 ) 2 + 4 H 2 O + 2 NOnebo kyseliny dusité (vytvořené in situ) jodidem nebo železnatými ionty
2 NaNO 2 + 2 NaI + 2 H 2 SO 4 → I 2 + 4 NaHSO 4 + 2 NO2 NaNO 2 + 2 FeSO 4 + 3 H 2 SO 4 → Fe 2 (SO 4 ) 3 + 2 NaHSO 4 + 2 H 2 O + 2 NOPředchozí reakce je jednoduchá metoda k získání NO v laboratoři.
Oxid dusnatý lze získat také v bezvodém prostředí díky redukci dusičnanů a dusitanů chromem (III):
3 KNO 2 (l) + KNO 3 (l) + Cr 2 O 3 (s) → 2 K 2 CrO 4 (s) + 4 NOPrůmyslové syntézy NO zahrnuje oxidaci amoniaku kyslíkem v přítomnosti platinové černi na 750 až 900 ° C .
Reaktivita
Oxidační redukce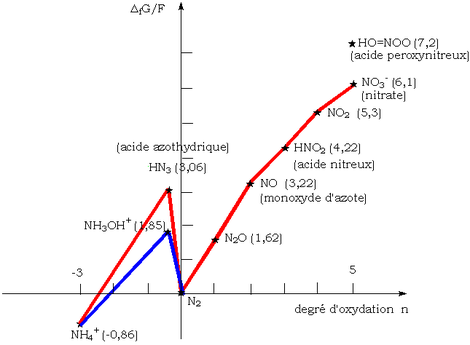
Frost diagram při pH = 0 z dusíku, jasně ukazuje, že oxid dusnatý je nestabilní a že by mělo nepřiměřené do dusík N 2.a kyselina dusičná HNO 3. Ve skutečnosti se velmi snadno oxiduje na oxid dusičitý NO 2, stabilnější, kyslíkem ve vzduchu. Proto jsou při oxidaci mědi koncentrovanou kyselinou dusičnou pozorovány načervenalé páry posledně jmenovaného plynu.
Možnou hypotézou je, že biradikální O 2 se váže na dva NO radikály za vzniku ON-OO-NO, který pak podléhá homolytickému narušení vedoucímu k NO 2 .
Při absenci kyslíku však disproporcionuje kolem 50 ° C na oxid dusný N 2 O(smějící se plyn) a oxid dusičitý NO 2(červené páry). Při 25 ° C je reakční rychlost prakticky nulová a NO je zde metastabilní.
Ve vodném roztoku se NO rozpouští za vzniku kyseliny dusičné HNO 2, podle následujícího možného reakčního schématu:
4 NO + O 2 + 2 H 2 O → 4 HNO 2NO reaguje s fluorem , chlorem a bromem za vzniku sloučenin typu X-NO, známých jako nitrosylhalogenidy. Jód příliš slabě oxiduje, aby vedl k tvorbě nitrosyljodidu.
Jodotrifluormethan reaguje s NO za vzniku jednoho z mála známých modrých plynů, nitrosotrifluormethanu:
NO + CF 3 I → I 2 + CF 3 NORychlost tvorby peroxynitritového iontu z oxidu dusnatého a superoxidového iontu je 1,9 × 10 10 mol − 1 s −1 , což znamená přítomnost peroxynitritu in vitro a in vivo při menším přebytku jeho dvou prekurzorů.
DimerizaceNa rozdíl od oxidu dusičitého nemá oxid uhelnatý tendenci dimerizovat. Toto chování je přičítáno distribuci jediného elektronu po celé molekule, stejně jako skutečnosti, že nejpravděpodobnější struktura O = NN = O by ponechala celkový počet vazeb beze změny (2 × 2,5).
V kapalné fázi dochází k částečné dimerizaci. Forma C 2v (cis) je stabilnější než její trans homolog a forma C 2h (obdélníková molekula s vazbou atomu dusíku jedné molekuly s atomem kyslíku druhé a naopak) není pozorována.
Výpočty ab inito SCF ukázaly, že cis forma dimeru (NO) 2 bude mít vzdálenosti d (NN) = 174 μm a d (OO) = 116 μm a úhel ONN = 107 °. Tyto hodnoty se významně liší od hodnot odvozených z neuspořádaných rentgenových difrakčních dat v pevné fázi (viz obrázek na opačné straně). Tento rozdíl v hodnotách potvrzuje obtížnost studia dimeru, jehož tvorba je prchavá.
Oxid dusnatý je také ligand
Oxidu dusnatého molekula se vztahuje k tomu oxidu uhelnatého CO, s tím rozdílem, že má další elektron, který se rozkládá na anti- lepení orbitální . Takto NO vytváří komplexy stejného typu jako komplexy vytvořené s CO, přičemž úhel vazby MN = O je prakticky roven 180 ° - ve skutečnosti se tento úhel pohybuje mezi 160 ° a 180 ° .
Tyto komplexy jsou proto považovány za lineární. V tomto případě dusík formálně zabírá svůj volný dublet v koordinační vazbě. Dusík je však oxidován, protože dává svůj jediný elektron kovu, který koordinuje, a který je proto redukován. Komplexy tetracarbonylonickel, nitrosylotricarbonylocobalt a dicarbonylodinitrosylofer jsou tedy izostrukturní (čtyřboká), protože izoelektronické .
N O může tvořit komplexy darováním pouze jednoho elektronu kovu. To vede ke skupině MNO, kde úhel vazby je mezi 120 ° a 140 ° .
Může také působit jako most mezi dvěma kovovými centry prostřednictvím dusíku.
Reakce nitrosyl komplexůChemie sloučenin koordinujících NO je rozsáhlá a bude diskutována pouze krátce. Například NO je vložen mezi niob a methyl ligand v následující reakci:
Charakterizace koordinovaného NOTerminály NO lze rozpoznat podle jejich intenzivní infračervené absorpce při 1610 cm- 1 . Počet IR absorpčních vln úhlových derivací je nižší.
Kvantitativní analýza
Nejklasičtější kvantitativní analýza oxidu dusnatého zahrnuje jednoduchou chemiluminiscenční reakci s ozonem.
Vzorek obsahující NO se smísí s nadměrným množstvím ozonu. Dusnatého reaguje oxid za vzniku kyslíku a di oxid z dusíku . Reakce také uvolňuje energii ve formě elektromagnetických vln ve viditelném: to je chemiluminiscence. Intenzita vyprodukovaného světla, měřená pomocí fotodetektoru, je úměrná množství oxidu dusnatého. Příkladem terapeutické aplikace NO je jeho měření ve vydechovaném vzduchu pacientů (většinou astmatiků). Princip spočívá ve vyfukování v chemiluninescenčním zařízení a tedy měření vydechovaného NO, a tedy měření zánětu dýchacích cest.
Je také možné stanovit různými elektrochemickými metodami ( potenciometrie s manganistanem draselným , polarografie )
Technické aplikace
Biologické funkce
NO je endogenní molekula uvolňovaná endotelovými buňkami , makrofágy , jaterními buňkami a neurony .
V těle plní oxid dusnatý několik funkcí.
Je přirozeně syntetizován tělem z L- argininu a kyslíku několika enzymy zvanými NO syntázy (NOS), což jsou hemoproteiny blízké cytochromu P450. Katalyzátor pro oxidaci kyslíkem z iminourea skupiny argininu je tedy železo v hemu , která projde z oxidačním stupni + II stupňů + III a IV + a naopak.
Vazba NO na thioly s nízkou molekulovou hmotností - jako je glutathion - vede k tvorbě S-nitrosothiolů, které by byly důležitým determinantem pro aktivitu a transport NO. Tyto sloučeniny mohou následně působit jako dárci NO a tím podstatně prodloužit svůj poločas.
Buněčná aktivita oxidu dusnatého prochází dvěma základními cestami, kterými jsou produkce intracelulárního cyklického guanosinmonofosfátu (cGMP) z guanosin trifosfátu (GTP) a tvorba cytotoxických peroxynitritů. Zvýšení koncentrace cyklického GMP zahrnuje aktivaci cytoplazmatické ( nemembránové ) guanylátcyklázy .
Vazodilatátor
Endotel z krevních cév používá ne pro spuštění uvolnění svého hladkého svalstva halenky , což způsobuje vazodilataci a zvýšení průtoku krve a snížení shlukování krevních destiček (trombocytů) . Je to nejdůležitější z „neadrenergních necholinergních“ neurotransmiterů ; pracuje v erekci (penis, klitoris, bradavky) a také se zdá, že hraje důležitou roli při uchování endotelu . U velké části lidí se tato syntéza NO považuje za nedostatečnou, což zvyšuje riziko vzniku kardiovaskulárních onemocnění . mechanismus Tento mechanismus vysvětluje použití dusičnanů, jako je trinitrin, při léčbě stejných srdečních onemocnění: Tyto léky se transformují na NO, a to způsobem, který dosud není zcela objasněn, což zase rozšiřuje koronární tepny , cévy zavlažující srdce, zvýšení jeho prokrvení.
EDRF (relaxační faktor odvozený od endotelu) je starý název pro NO. Bývalí lékaři si všimli jeho vazodilatační role, ale dosud ji chemicky neidentifikovali.
Mikrobicid
Tyto makrofágy , buňky imunitního systému , produkují NO za účelem odstranění bakteriálních patogenů, NO, které se mohou za určitých okolností, může způsobovat škodlivé vedlejší účinky, je v případě tzv fulminantní infekce septikémie , kde Nadměrná produkce NO makrofágy vede k masivní vazodilatace , hlavní příčina arteriální hypotenze vyskytující se v septickém šoku .
Neurotransmiter
NO působí jako neurotransmiter mezi nervovými buňkami . Na rozdíl od většiny jiných neurotransmiterů, jejichž působení v synaptické štěrbině je zaměřeno pouze na postsynaptický neuron, malá molekula NO široce difunduje a může dosáhnout několika okolních neuronů, včetně neuronů, které nejsou synapsemi propojeny. Předpokládá se, že tento proces zahrnuje zapamatování zajištěním dlouhodobého zapamatování . Tyto endokanabinoidy , lipidů neurotransmitery, mají podobné difúzní vlastnosti.
Uvolňující hladké svaly
NO je přítomen v mnoha orgánech trávicího traktu jako neurotransmiter neadrenergní, necholinergní. Je zodpovědný za relaxaci hladkého svalstva gastrointestinálního traktu. Zejména zvyšuje kapacitu žaludku k ukládání potravinových tekutin.
Regulátor apoptózy
Oxid dusnatý je základním regulátorem buněčné apoptózy . Může mít antiapoptotický účinek nebo naopak apoptotický účinek. Tento přepínač je úzce spojen s přítomností nebo nepřítomností buněčných redukčních látek, jako je glutathion .
Za přítomnosti vysoké hladiny superoxidu O 2 - iontu umožňuje oxid dusnatý tvorbu peroxynitritového iontu , pravděpodobně zodpovědného za modifikaci potenciálu mitochondriální membrány, stejně jako za mnoho jevů buněčné apoptózy , zejména buněčných buněk imunitní systém.
Exogenní ŽÁDNÍ dárci
Jedná se o látky s jednou nebo více vazbami dusík - kyslík, dusík - dusík nebo zabraňující destrukci NO ( viagra ). Existují dusičnany , dusitany , dusičnany, azidy ...
Terapeutické použití
Terapeutické použití:
- Léčivě se používá jako inhalovaný vazodilatátor . Použití inhalovaných vazodilatancií selektivně vazodilatuje kapiláry v dobře větraných oblastech plic. To umožňuje snížit plicní arteriální hypertenzi spojenou s hypoxickou vazokonstrikcí a zvýšit okysličení krve.
- Sloučenina zvaná asymetrický dimethyl arginin (ADMA) je známým inhibitorem syntézy NO, a je proto považována za biologický marker kardiovaskulární dysfunkce.
- Produkce NO také hraje důležitou roli při dosahování a udržování dlouhotrvající erekce. Zvýšené koncentrace cGMP vedou k lepší vazodilataci a erekci. Předpokládá se, že účinek „ druků “ se také získat prostřednictvím NO, což způsobuje uvolnění hladkých svalových vláken, které obklopují arteriol zásobujících kavernózních těles na penisu a zvyšuje průtok krve. Sildenafil (Viagra) a tadalafil (Cialis) jsou kompetitivní inhibitory tohoto enzymu fosfodiesterázy typu 5 (PDE5), odpovědné za inaktivaci cyklického GMP v GMP.
Objev biologických vlastností NO v 80. letech byl zcela neočekávaný a způsobil určitý rozruch. Vědecký časopis s názvem NO „Molekula roku“ v roce 1992 byl vytvořen NO Learned Society a objevil se vědecký časopis zcela věnovaný NO. Nobelova cena za medicínu a fyziologii získala v roce 1998 na Ferid Murad , Robert F. Furchgott a Louis J. Ignarra za jejich práci na neurotransmise funkcí NO. Tato práce je u zrodu založení francouzské farmaceutické společnosti Nicox . Odhaduje se, že 3 000 ročně publikace vědeckých článků o roli v biologii oxidu dusnatého.
bezpečnostní
Odkaz OSN pro přepravu nebezpečných věcí :
- Název (francouzsky): Oxid dusnatý, stlačený
- Třída: 2
- číslo: 1660
Bibliografie
- Nathan S Bryan, Janet Zand, Bill Gottlieb, Řešení: oxid dusnatý (NO) , Vědecký a technický institut pro životní prostředí a zdraví (ISTES), 2014, 188 stran.
Poznámky a odkazy
- Oxid dusičitý , bezpečnostní list (y) Mezinárodního programu pro chemickou bezpečnost , konzultován 9. května 2009
- (in) David R. Lide, Příručka chemie a fyziky , CRC,16. června 2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 a 1-4200-6679-X ) , s. 9-50
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (en) Robert H. Perry a Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- „ Vlastnosti různých plynů “ na adrese flexwareinc.com (přístup 12. dubna 2010 )
- (in) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40
- (in) Irvin Glassman, Richard A. Yetter, Combustion , Elsevier,2008, 4 th ed. , 773 s. ( ISBN 978-0-12-088573-2 ) , str. 6
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , Vázaná kniha ( ISBN 978-1-4200-9084-0 )
- (in) David R. Lide, Příručka chemie a fyziky , CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205
- „ Oxid dusnatý “ v databázi chemických produktů Reptox z CSST (Quebecská organizace odpovědná za bezpečnost a ochranu zdraví při práci), přístup k 25. dubnu 2009
- „ Oxid dusnatý “ , na hazmap.nlm.nih.gov (přístup 14. listopadu 2009 )
- Crépel, F., a Lemaire, G. (1995) Oxid dusnatý . ; Časopis MS (medicína / věda); 11: 1639-42 (PDF, 4 stránky)
- Gabbai, FB, Garcia, GE a kol. , Role oxidu dusnatého v glomerulární fyziologie a patofyziologie , Adv Nephrol Necker Hosp 24, 3-18 (1995)
- RA Schroeder a PC Kuo, Oxid dusnatý: fyziologie a farmakologie , Anesth Analg 81, 1052-9 (1995)
- Entalpie izomerizace peroxynitritového iontu na dusičnany
- Sennequier, N., a Vadon-Le Goff, S. (1998). Biosyntéza oxidu dusnatého (NO): mechanismus, regulace a kontrola. SLEČNA. Médecine sciences, 14 (11), 1185-1195 ( http://cat.inist.fr/?aModele=afficheN&cpsidt=1584829 resumé])
- De Soete, G. (1993). Oxid dusný ze spalování a průmyslu: Chemie, emise a regulace Oxid dusný ze spalování a průmyslu: Chemie, emise a redukční techniky ( shrnutí ).
- RB King; Anorganic Chemistry of Main Group Elements, VCH Publishers, New York, 1995.
- Química Nova - Chemie peroxynitritu, biologického toxinu
- Greenwood NN & Earnshaw A. (1997). Chemie prvků. 2. th Ed., Elsevier, str. 446 .
- Skanckea PN Boggsb JE (1973). Teoretické studium struktury (NO) 2. Chemická fyzika Dopisy (21) str. 316-317 .
- Lipscomb WN, Wang FE, květen WR a Lippert EL (1961). Komentáře ke strukturám 1,2-dichlorethanu a N202. Acta.Cryst. (14) s. 1100-01 .
- FA Cotton, G. Wilkinson, CA Murillo, M. Bochmann; Advanced Anorganic Chemistry, 6. vydání. Wiley-Interscience, New York, 1999.
- Fischer G & Becknell D; Anální. Chem., 44 , 863, 1972
- Kieselbach, Ind. Eng. Chem., Anal. Vyd., 16 , 766, 1944
- Farmakrama; Oxid dusnatý
- Syntáza oxidu dusnatého je cytochrom P-450 typu h ... [Biochemistry. 1992] - výsledek PubMed
- Andrews, KL, Triggle, CR a kol. NE a vaskulatura: odkud pochází a co dělá? Heart Fail Rev 7, 423-45 (2002)
- Metabolismus oxidu dusnatého
- Giuliano, F., Rampin, O., Benoit, G., & Jardin, A. (1997). Periferní farmakologie erekce . Advances in Urology, 7 (1), 24-33.
- Oxid dusnatý jako bifunkční regulátor apoptózy
- Chemie peroxynitritů
- Kontrastní účinky NO a peroxynitritů na expresi HSP70 a apoptózu v lidských monocytech; Adrie C & al. Am J Physiol Cell Physiol 279: 452-460, 2000.
- Funkční studie glutathionperoxidázy kódované HIV-1
- NE a NO-dárci
- Azid sodný jako nepřímý donor oxidu dusnatého: výzkumy izolovaných segmentů krysí aorty; Ukr Biokhim Zh. 2005 červenec-srpen; 77 (4): 120-3
- Klinické použití oxidu dusnatého; Olson G.
- 1998 Nobelova cena za medicínu za objev úlohy NO v kardiovaskulární regulaci
- Řešení: oxid dusnatý (NO) , poznámka ke čtení Louis-Marie Houdebine, pseudo-sciences.org, 31. prosince 2014
Podívejte se také
- Syndrom akutní dechové tísně
- Neurotransmiter
- EDRF: Název relaxačního faktoru odvozeného od endotelu, který byl této stejné molekule dán dříve, než známe jeho chemický vzorec
- Transdukce signálu
- Měření oxidů dusíku
Externí odkaz
- Oxid dusnatý: Biologie a chemie , vědecký časopis








