Dihydrogen
| Dihydrogen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Název IUPAC | vodík | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyma |
vodík |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O Agentura | 100 014 187 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o EC | 215-605-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E949 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ÚSMĚVY |
[HH] , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | bezbarvý stlačený plyn bez zápachu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzorec |
H 2 [izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární hmotnost | 2,01588 ± 0,00014 g / mol H 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T. fúze | -259,1 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° vroucí | -252,76 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpustnost |
21,4 ml v 1 l vody (tj. 1,92 mg / l ) ( 0 ° C ) 8,5 ml v 1 l vody ( tj. 0,76 mg / l ) ( 80 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametr rozpustnosti δ | 6,9 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objemová hmotnost |
0,089 88 g / l (plyn, CNTP ), 0,070 8 kg / l (kapalina, −253 ° C ), rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota samovznícení | 500 až 571 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bod vzplanutí | hořlavý plyn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Výbušné limity ve vzduchu | 4 - 76 % obj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak nasycených par |
rovnice:
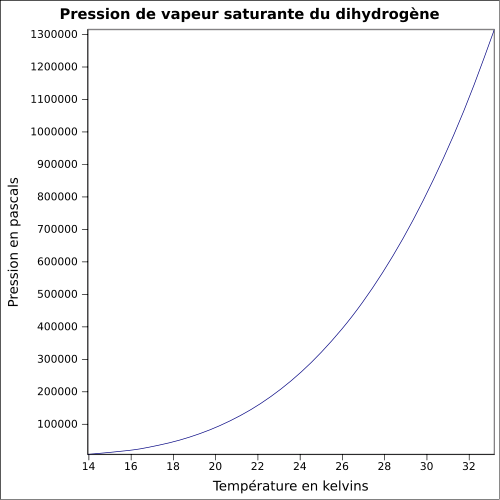
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritický bod | 13,0 bar, -239,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trojitý bod |
-259,3467 ° C ; 7 205 kPa abs |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 42,5 × 10 −5 kcal cm −1 s −1 K −1 až 16,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 1310 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 plyn, 1 bar | 130,68 J K −1 mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 0,058 68 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 0,90 kJ mol −1 ( 1 atm , -252,76 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C str | 14 266 J kg −1 K −1 až 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 285,8 kJ / mol ( 25 ° C , plyn) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 242,7 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opatření | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Nebezpečí H220 H220 : Extrémně hořlavý plyn |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Kritická teplota stlačeného plynu = -239,9 ° C B1 : Dolní mez hořlavosti hořlavého plynu = 4,0% Zveřejnění 1,0% podle klasifikačních kritérií |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| plyn:
4
0
0
chlazená kapalina: 4 3 0 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doprava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : hořlavý plyn UN číslo : 1049 : STLAČENÝ VODÍK Třída: 2.1 Klasifikační kód: 1F : Stlačený plyn, hořlavý; Štítek: 2.1 : Hořlavé plyny (odpovídá skupinám označeným velkým F); 
223 : chlazený zkapalněný plyn, hořlavý UN číslo : 1966 : HYDROGEN REFRIGERATED LIQUID Třída: 2.1 Klasifikační kód: 3F : Chlazený zkapalněný plyn, hořlavý; Štítek: 2.1 : Hořlavé plyny (odpovídá skupinám označeným velkým F);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalace | udušení | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dihydrogenfosfát je forma molekulární z prvku vodíku , který existuje jako plyn do standardních podmínek teploty a tlaku . Molekuly mají dva atomy vodíku; jeho chemický vzorec je H 2 . Říká se mu také „molekulární vodík“ nebo v plynném stavu „plynný vodík“. V běžném jazyce, kde neexistuje dvojznačnost se stejnojmenným chemickým prvkem, je velmi často označován jednoduše jako „vodík“ a někdy pro molekulu vodíku mluvíme jednoduše o „molekule vodíku“.
To bylo použito v zeppelin- typů vzducholodí , s použitím vlastností Archimedes tah předtím, než byla nahrazena heliem , což je méně nebezpečné, protože není hořlavý. Globální spotřeba vodíku se dnes pohybuje kolem 50 milionů tun ročně. Většina výroby vodíku se spotřebovává na místě, zejména v chemickém a petrochemickém průmyslu: syntéza amoniaku (50%), rafinace a odsíření uhlovodíků (37%), syntéza methanolu (12%). Vyrábí se 96% z uhlovodíků (metan, ropa, uhlí) a 4% elektrolýzou vody . Tato výroba je v roce 2020 doprovázena produkcí 830 milionů tun CO 2ročně, tedy asi 2% globálních emisí .
Je to lehký plyn, který zemská gravitace nedokáže zadržet. Hoří ve vzduchu a vytváří vodu , a proto se jeho název skládá z předpony „hydro“, z řeckého ὕδωρ (hudôr), což znamená „voda“, a z přípony „gen“, z řeckého γεννᾰν (gennen), „Beget“ . Používá se zejména ke konzervování masa . Dihydrogen má teplotu odpařovací o 20,27 K a teplotu tání v 14,02 K . Při velmi vysokých tlacích , jako jsou ty, které existují ve středu plynných gigantů , se tyto molekuly disociují a vodík se stává tekutým kovem . V prostoru, mraky H 2 jsou základem pro tvorbu hvězdy procesu .
Historický
Prvním známým vědcem, který popsal produkci dihydrogenu, byl švýcarský Paracelsus (1493-1541). Tento objev učinil tak, že nalil železný prášek vitriolem , ale nerozuměl přesné povaze plynu uvolňovaného během experimentu .
Anglický chemik Henry Cavendish (1731-1810), opakující pokusy Paracelse s několika různými kovy , zjistil, že takto vyrobený plyn se liší od vzduchu, je hořlavý a má nízkou hustotu. Nazval tento plyn „hořlavý vzduch“ (v angličtině: hořlavý vzduch ) a zjistil, že jeho produktem spalování je voda . Dioxygen se mu s názvem „vitální vzduch“.
Francouzský chemik Antoine Lavoisier, který potvrdil Cavendishovy experimenty, navrhuje nahradit slovo „hořlavý vzduch“ slovem „vodík“. Toto slovo je vytvořeno s předponou hydro (z řeckého ὕδωρ (hudôr), „voda“) a příponovým genem (z řeckého γεννᾰν (gennen), „generovat“). Slovo vodík tedy znamená, že vytváří vodu .
Následně bude ve vědecké oblasti pro pojmenování chemického prvku H použito slovo „vodík“ a pro molekulu H 2 slovo „vodík“ .
Chemické vlastnosti
Test uznání
Aby se otestovala přítomnost dihydrogenu, přiblíží se plamen plamene ke zkumavce obsahující dihydrogen. Chemická reakce spalování vodíku s kyslíkem ve vzduchu, iniciovaná zdrojem tepla, produkuje charakteristický hluk zvaný „štěkání“ nebo „štěkání“.
Spalování
Spalování vodíku v dioxygen , který produkuje vodu , je 2 H 2 (g) + O 2(g) → 2 H20(dále jen). Je obzvláště prudký (viz test rozpoznávání) a velmi exotermický : jeho výhřevnost je 141,86 MJ / kg [nebo 141,79 MJ / kg ] (při 25 ° C [nebo 15 ° C ] pod 1 atm ) nebo standardní entalpie spalování při 25 ° C , z -285.84 kJ / mol , při teplotě 100 ° C , z -283.45 kJ / mo l (H 2 plynu, o 2 plynu, ale H 2 o kapalina , jako vyšší hodnotu výhřevnosti nebo PCS), ale 120,1 MJ / kg [nebo 119,93 MJ / kg ], tj. hodnotu entalpie spalování, při teplotě 100 ° C , z -242,8 kJ / mol (H 2 plynu, plynného o 2 , H 2 o par , jako nižší výhřevností nebo NCV , počítání 40,660 kJ / mol pro odpařování vody při 100 ° C ), například proti pouze 49,51 MJ / kg pro butan . Tato vlastnost z něj činí palivo vhodné pro kosmické lodě, ale jeho skladování je nebezpečné.
Stejná pomalejší oxidace se používá k výrobě elektřiny v palivovém článku .
Orto a para formy
Plynný vodík je směs dvou typů isomerních molekul, které se liší od sebe v spinu jejich atomových jader . Tyto dvě formy se nazývají orto- a para-vodík a orto forma (paralelní spiny, tripletový stav) odpovídá excitovanému stavu, který v čistém stavu neexistuje. Za normálních teplotních a tlakových podmínek se tepelnou excitací vodík skládá ze 75% ortho formy a 25% para formy. Při 77 K je rovnovážná směs (dosáhla spontánně za několik dní, ale za několik hodin s katalyzátory) 50%. Ale při velmi nízké teplotě se orto forma v průběhu času zcela transformuje do para stavu (antiparalelní spiny, singletový stav). Tyto dvě formy mají mírně odlišné energetické úrovně, a proto mírně odlišné fyzikálně-chemické vlastnosti . Například teplota tání a teplota varu para-vodíku jsou asi o 0,1 K nižší než teplota tání a orto- .
Zdroje vodíku
Dihydrogen je velmi lehký plyn. Protože ji zemská gravitace nedokáže zadržet, přirozeně uniká ze zemské atmosféry. Proto je ve vzduchu přítomen pouze ve stopových množstvích (0,5 ppmv ) . Tento atmosférický nedostatek znamená, že veškerý použitý dihydrogen se vyrábí průmyslově různými procesy, z molekul, kde jsou atomy vodíku chemicky vázány.
Existuje však několik geologických kontextů, kde dihydrogen přirozeně pramení ze Země . Vodík vycházející z těchto zón se označuje pojmem přírodní vodík .
Umělý vodík
Výroba vodíku zahrnuje mnoho různých procesů je vodík atom tvořící řadu molekul ( voda , uhlovodíky , cukry , atd ).
Historický způsob výrobyHistoricky, v XIX th století, dihydrogen byla získána emisí vodní páry (H 2 O) v sudu naplněné železnými pilinami a čipy. Vodní pára oxidovala kov a na jedné straně vytvořila oxid železitý, na druhé straně uvolňovala vodík. Ten poté opustil hlaveň, kde byl přefiltrován do dalšího sudu naplněného vodou, poté uložen přímo do aerostatu . Toto zařízení umožnilo armádě nafouknout pozorovací balón kdekoli a během několika hodin .
Současné metodyV roce 2015 byl vodík průmyslově vyráběn různými procesy:
- pro 49% parní reformací z uhlovodíků (zejména z metanu , viz reforma metanu );
- pro 29% částečnou oxidací ropy
- pro 18% zplyňování z uhlí
- 4% elektrolýzou vody .
Studují se také další procesy, od krakování nebo částečné oxidace, která má tu výhodu, že je exotermická .
Reforma uhlovodíkových parParní reformování uhlovodíků je metoda, která na počátku XXI th století, je nejvíce používán v průmyslovém měřítku. Jeho princip je založen na reakci uhlovodíků (metan atd.) Za přítomnosti vodní páry a tepla. Globální reakce je napsána:
.Energetická účinnost se pohybuje kolem 40 až 45% v některých zařízeních . V průmyslové praxi je nutné reakci urychlit pomocí katalyzátorů nebo hořáků. Má tu nevýhodu, že produkuje oxid uhličitý , skleníkový plyn .
Katalytické technologie, nebo inovativnější technologie, jako jsou plazmové reformátory, jsou v současné době studovány.
Elektrolýza vodyElektrolýza vody je technologie, která spočívá v tom, průchodem elektrického proudu (přímé) ve vodě (na kterém elektrolyt , jako je hydroxid sodný byl již dříve přidané ), aby se dosáhlo disociaci molekul vody na vodík a kyslík .
Reakce na anodě :
2 H 2 O(l) → O 2(g) + 4 H + (aq) + 4 e -Reakce na katodě :
4 H 2 O(l) + 4 e - → 2 H 2 (g) + 4 OH - (aq)Reakce ve vodě:
4 H + (aq) + 4 OH - (aq) → 4 H 2 O (dále jen)Celková reakce:
2 H 2 O(l) → 2 H 2 (g) + O 2 (G)kde (l), (g) a (aq) znamenají „v kapalné fázi“, „v plynné fázi“ a „ve vodném roztoku“.
Tato technologie vyžaduje velké množství elektřiny. Podle Ademe v roce 2020 je účinnost vodíkového řetězce v Power-to-H2-to-Power 25%, zatímco účinnost elektrických baterií je 70%. Proto se používá relativně málo.
Částečná oxidace uhlovodíkůTato reakce je „bohatým“ spalováním v tom smyslu, že cílem je vytvořit plyn bohatý na H 2 a CO (syntézní plyn); místo „klasických“ produktů CO 2 a H 2 O.
Reakce je napsána:
.Jako oxidační činidlo se většinou používá vzduch. Pak máme:
.Reakce je exotermická: například entalpie reakce s metanem je −35,7 kJ mol −1 .
Stejně jako reakce reformování párou je nutné reakci katalyzovat.
Zájem o parciální oxidační reakci spočívá v její exotermické povaze (na rozdíl od parní reformovací reakce), která napomáhá katalýze (zvýšení teploty).
Hlavní nevýhoda spočívá v tom, že procentuální podíly H 2 jsou nižší než ty získané parním reformováním, z důvodu přítomnosti majoritní dusíku ve vzduchu. Kromě toho existuje riziko získání NO x .
Působení kyseliny na kovDihydrogen se vyrábí působením kyseliny na kov. Příklad:
.Dihydrogen lze také vyrobit reakcí hydroxidu sodného s hliníkem podle vzorce:
Produkce fotosyntézou (sinice)Některé sinice dokážou chemicky rozložit vodu na kyslík a vodík pomocí fotosyntetických reakcí. To by umožnilo vyrábět vodík pomocí sluneční energie . V této oblasti probíhá výzkum, zejména pokud jde o genetické inženýrství .
Přírodní vodík
Vodík produkovaný na Zemi přirozeně, na rozdíl od vodíku vyrobeného uměle reformováním metanu nebo uhlovodíků , se říká, že je to přírodní vodík nebo nativní vodík .
Distribuce, výrobní kapacita a fyzikálně-chemické mechanismy pramenů nebo vklady jsou stále předmětem průzkumných studií na počátku XXI -tého století. V dubnu 2019 byl tedy zahájen a spolufinancován výzkumný projekt sen4H2 Evropskou kosmickou agenturou , jehož cílem je detekovat přirozené emise vodíku pomocí satelitních snímků.
Zdroje přírodního vodíkuVýroba přírodního vodíku v páteři je známá již od 70. let minulého století a studovala se v poslední době. Jedná se o serpentinization reakce ( redox z olivínu ) mezi vodu a vyvřelých hornin v jedné rovině s zemském plášti , a to za tepla těchto exotermních reakcí : kyslíku z H 2 O molekul.atomy vodíku zachycené železem ve skále se mohou v H 2 volně sdružovat. Takto vyrobený vodík uniká hydrotermálními ventilačními otvory a může případně reagovat postupně za vzniku methanu , poté těžších uhlovodíků. Příliš hluboko nelze tyto vklady v roce 2018 využít
Emise vodíku byly také objeveny uprostřed kontinentálních kráterů ruským geologem Nicolayem Larinem po jeho práci na hypotéze hydratované Země. Společnost IFP Energies nouvelles tento objev potvrdila v roce 2013 a hlásila lokálně důležité problémy na většině kontinentů, v Rusku , Spojených státech , v Brazílii , v Ománu nebo v Mali .
Tento jev je stále špatně pochopen a diskuse o přesném mechanismu, který generuje tyto emise, ještě nebyla vyřešena. Mohlo by se jednat o hydrataci železa infiltrovanou vodou, která je přítomna v pásech greenstone , přítomných v kráterech. V Kansasu , poblíž Junction City , bylo tedy v 80. letech identifikováno ložisko, které bylo předmětem zájmu ve dvacátých letech minulého století; dihydrogen by se tam získával z takových reakcí oxidace železa. V Rusku odhadoval IFP v roce 2010 denní tok jedné deprese na několik desítek tisíc metrů krychlových , nebo ekvivalentní spotřebu 500 taxíků. Originál geologický či hydrogeologický také převládá pro vydání vodíku studovaných v Brazílii, v některých pohádkové kruzích nacházejících se v povodí z São Francisco .
V Yanartaně v Turecku by „tisícileté požáry“ Mount Chimera byly spalováním plynu složeného z metanu (87%), vodíku (7,5 až 11%) a dinitrogenu (2 až 4,9%), který má dvojí původ: serpentinizace na jedné straně, termogenní plyn na straně druhé. Byly by původním zdrojem olympijského ohně .
Mali je v roce 2015, jedinou zemí, kde je přírodní vodík použity, v obci Bourakébougou , 60 kilometrů severně od Bamako . Plyn by pocházel z „nadměrného zrání ropy“ pravděpodobně zakopaného poblíž a jeho zásoby se odhadují na zhruba 1,5 miliardy metrů krychlových . Tlak v jamkách neklesá, takže zásyp se neustále plní, což umožňuje udržitelnost této operace.
Tyto sopečné plyny často obsahují stopy vodíku. Na Havaji tedy spektroskopická studie provedená na ohni sopečného plynu ukázala, že se jednalo o spalování dihydrogenu.
Jakákoli magmatická hornina by obsahovala vodík až do asi 5 l / m 3 ; proto všechny vrty vykazují odplynění vodíkem. Během ruského experimentu s vrtáním sg3 bylo bahno vytěžené z díry popsáno jako probublávání tímto plynem .
VýzvyNa rozdíl od umělého vodíku, který vyžaduje výrobu energie, která ji redukuje na pouhý nosič energie , je přírodní vodík skutečným zdrojem energie , při jehož spalování se neprodukuje pouze voda. Kromě toho by mohly být možné koprodukce s geotermální energií nebo těžbou helia , což by mohlo odvětví pomoci být konkurenceschopným. V roce 2020 však nebude průmyslový potenciál přesně kvantifikován a zákon o těžbě v mnoha zemích vodík nezohledňuje. Detekce vodíku in situ je skutečně obtížná, ačkoli byly vyvinuty účinnější detektory.
Průmyslové použití
Globální spotřeba vodíku se dnes pohybuje kolem 50 milionů tun ročně. Většina produkce vodíku se spotřebovává na místě, zejména v chemickém a petrochemickém průmyslu: syntéza amoniaku (50%), rafinace a odsíření uhlovodíků (37%), syntéza methanolu (12%).
Hlavní průmyslové využití vodíku je:
- metoda Haber-Bosch (výroba amoniaku ) se hydrogenace z tuků a olejů a výroby methanolu ;
- výroba kyseliny chlorovodíkové , na svařování , na paliva pro rakety a snížení z rud z kovu;
- kapalina dihydrogen se používá pro výzkum při velmi nízkých teplotách, včetně studie supravodivosti ;
- vodík se používá jako stopovací plyn k provádění operací detekce úniků v různých oblastech (rafinace ropy, automobily, topná zařízení, vodní rozvodná síť, nádrže na letadla atd.);
- vodík je potravinářská přídatná látka povolená pod kódem E949 , v kategorii značkovačů;
- vodík se také používá jako teplonosná kapalina v některých strojích s vysokým výkonem (například synchronní alternátor elektrárny);
- v aerostatech byl použit vodík, protože je čtrnáctkrát méně hustý než vzduch, ale z bezpečnostních důvodů byl nahrazen heliem; stále se používá pro některé meteorologické balóny na vzdálených stanicích.
- Dihydrogen byl testován jako palivo pro letectví během letu 15. dubna 1988 s Tupolev Tu-155.
Některé izotopy vodíku mají také zvláštní průmyslové nebo technologické využití:
- deuterium ( 2 H), se používá v jaderné technice jako moderátor ( těžké vody nebo D 2 O) ke zpomalení neutronů . Sloučeniny deuteria se také používají v chemii a biologii ke studiu nebo využití izotopového účinku ;
- tritium ( 3 H), další izotop, je produkován v nukleárních reaktorech a je používán pro konstrukci atomové bomby . Používá se také jako izotopový marker v biologických vědách a jako zdroj záření v luminiscenčních barvách;
- deuterium a tritium jsou také fúzovány ve výzkumných reaktorech a zvažovány pro projekty řízené jaderné fúze na Zemi.
K dnešnímu dni jsou zvažovány tři hlavní způsoby skladování vodíku na palubě vozidla:
- skladování ve formě stlačeného plynu;
- skladování v kapalné formě při nízké teplotě;
- skladování v pevné formě, přičemž vodík se poté váže na další složky ( adsorpcí nebo ve formě chemické sloučeniny).
Stlačený plyn
Je to nejběžnější forma skladování vodíku.
Skladování plynu ve stlačené formě (v současné době 350 barů) umožňuje dosáhnout uspokojivé hustoty hmoty s kompozitními nádržemi. Hustota objemu úložiště zůstává nízká: tlak 700 barů je nevyhnutelný, aby byla technologie konkurenceschopná.
Tato technologie existuje a běžně se používá. Jeho nevýhoda spočívá v energii potřebné pro kompresi a v nízké účinnosti z hlediska velikosti ve srovnání s jinými metodami. Tato objemnost je jednou z obtíží při použití dihydrogenu ve formě stlačeného plynu v automobilových aplikacích.
Po stlačení je hustota vodíku při 20 MPa ( 200 bar) přibližně 16,8 kg / m 3 , při 35 MPa ( 350 bar) přibližně 23 kg / m 3 a při 70 MPa ( 700 bar)) přibližně 38 kg / m 3 . To odpovídá hustotě hustoty energie 767 kWh / m 3 (27 ° C, 35 MPa) a stále hustotě hustoty energie 33,3 kWh / kg.
Skladování kapaliny při 20 K ( −253 ° C ) pod 10 barů umožňuje dosáhnout zajímavých objemových a hmotnostních hustot, ale k minimalizaci odpařování vyžaduje nádrže s vysokou tepelnou izolací.
Technologie tam je. Má lepší objemovou účinnost než skladování stlačeného plynu ( 70 kg / m 3 proti 10 kg / m 3 při 115 barech a 0 ° C ). Tato výhoda je však zmírněna relativně velkým objemem nezbytných izolačních skříní.
Na druhou stranu je k přechodu do kapalné fáze zapotřebí značné množství energie: zkapalnění spotřebuje 30 až 40% energetického obsahu plynu a ztráta při skutečném použití je značná (v současné době 1,25 na tisíc za hodinu), silně penalizace úložiště za týden.
Tato technika se používá zejména v kosmickém sektoru, kde i přes krátkou dobu implementace je plnění kontinuální až do posledního okamžiku.
Kovové hydridy
Skladování na substrátech v adsorbované formě, zejména na hydridech kovů, má velmi zajímavou objemovou hustotu, ale nízkou hmotnostní hustotu. Kromě toho kinetika, teplota a cyklický tlak zůstávají těžkými body pro kontrolu.
Atomy vodíku jsou uloženy v některých sloučeninách kovů. Vodík se získává zahříváním nebo snížením tlaku. Tato technika je dnes špatně pochopena. Má tu nevýhodu, že vyžaduje extrémně čistý dihydrogen, aby nedošlo ke zničení absorpční kapacity hydridů. Handicapem je také vytápění za účelem získání plynu. Tento typ skladování, který je i nadále předmětem výzkumu, je ve fázi průmyslového vývoje a plánují se některé demonstrační projekty, například se start-upem McPhy, který vyvíjí technologii hydridu hořečnatého (technologie od CNRS, NEEL Institute) .
Skladovací kapacita určitých hydridů.
| Hydrid | Hmotnostní procenta H 2 obsahu |
|---|---|
| LaNi 5 H 6.5 | 1.4 |
| ZnMn 2 H 3.6 | 1.8 |
| TiFeH 2 | 1.9 |
| Mg 2 NiH 4 | 3.6 |
| VH 2 | 3.8 |
| MGH 2 | 7.6 |
Velmi studoval kovu je palladium , které prostřednictvím svého hydridu PDH 2, má schopnost absorbovat velké množství vodíku ve své krystalové mřížce. Při pokojové teplotě a atmosférickém tlaku může palladium absorbovat až 900násobek svého objemu plynného vodíku, přičemž tento proces je reverzibilní.
Adsorpce na uhlí umožňuje ukládat na povrchu určitých uhlíkových struktur , jako je aktivní uhlí nebo nanotrubiček , molekul vodíku. Umožňuje skladovat 0,05 až 2% hmotnostní dihydrogenu .
Tento typ úložiště je ve fázi výzkumu.
Výroba a použití
Ve zprávě publikované v června 2019si Mezinárodní energetická agentura všímá všestrannosti vodíku, který lze vyrábět ze všech fosilních paliv, obnovitelných zdrojů energie a jaderné energie, lze jej přepravovat v plynné nebo kapalné formě a přeměnit jej na elektřinu nebo metan pro širokou škálu použití.
Můžeme rozlišit tři kategorie vyráběného vodíku podle toho, jak se vyrábí (viz část Aktuální metody ):
- vodík šedá , produkoval konverzí fosilních paliv bez zachycování a ukládání uhlíku ;
- vodík modrý , produkoval konverzí fosilních paliv se zachycování a ukládání uhlíku;
- zelená vodík vyroben z z elektřiny z obnovitelných zdrojů a jaderných ( fialové pro některé, žlutá pro ostatní).
Vodík produkovaný v zemské kůře ( diagenezí a radiolýzou ), stejně jako prvotní vodík (přítomný od vzniku Země ) jsou dalšími možnými zdroji, které však dosud nebyly prozkoumány.
V roce 2020 se náklady na šedý vodík pohybují mezi 1 a 2 EUR / kg oproti 4 až 7 EUR / kg pro zelený vodík vyráběný průmyslovým způsobem. Podle Julien Chauvet, ředitele společnosti Engie Solutions pro Hydrogen France , „kilo vám umožní ujet 100 km, což je srovnatelné s benzínem a je podobné naftě pro lehká vozidla“ .
Průmyslová produkce
Vodík se v současné době vyrábí téměř výhradně ze zemního plynu , ropy a uhlí .
Pro vlastní potřebu průmysl vyrábí vodík ( např .: ve Francii více než 900 000 t / rok vodíku, zejména pro odsiřování ropných paliv a pro výrobu amoniaku v dusičnanových hnojivech ; vodík je pak chemický vstup a ne energie dopravce ). Nejlevnější průmyslový proces k výrobě tohoto vodíku, v roce 2018, je reformování z uhlovodíků , nejčastěji parním reformováním ze zemního plynu (který je složen převážně z methanu ). Při teplotě mezi 700 a 1100 ° C , vodní pára reaguje s methanem za vzniku oxidu uhelnatého a vodíku. Čištění vodíku je snazší za vysokého tlaku, reformování se provádí za tlaku dvaceti barů . Směs vodíku a oxidu uhelnatého se běžně označuje jako " syntézní plyn ". Pokud se reakce provádí v přítomnosti přebytečné vodní páry, oxid uhelnatý se oxiduje na vyšší oxidační úroveň, což vede k oxidu uhličitému , který zvyšuje produkci vodíku .
Společnost Air Liquide má v tomto procesu zvláštní mistrovství. V roce 2015 uvedla do provozu v Saúdské Arábii v závodě Yanbu jednotku s celkovou výrobní kapacitou vodíku 340 000 m 3 / h na CNTP .
V roce 2019 poskytne Australská agentura pro energii z obnovitelných zdrojů (ARENA) 9,41 milionu australských dolarů (8,5 mil. EUR ) na projekt skupiny Hazer (australská společnost pro obnovitelnou energii) zaměřenou na přeměnu bioplynu z methanizace čistírenského kalu na vodík a grafit . Hazer chce v Munsteru (Západní Austrálie) postavit demonstrační závod v hodnotě 15,8 milionu USD.
Vodíkový sektor a výzvy pro udržitelný rozvoj
„Tradiční“ průmyslová výroba vodíku z fosilních uhlovodíků má špatnou uhlíkovou stopu a vypouští mnoho skleníkových plynů a dosahuje 830 milionů tun CO 2.ročně v roce 2020, tj. přibližně 2% celosvětových emisí a téměř stejně jako odvětví letectví nebo námořní doprava. Ve Francii tyto emise dosahují téměř deseti milionů tun ekvivalentu CO 2 .ročně kolem 2015-2017, tj. 7,5% emisí skleníkových plynů z francouzského průmyslu, uvádí ADEME . Výroba vodíku z obnovitelné elektřiny, která je více ctnostná, by mohla do roku 2030 snížit své náklady o 30% díky rozmachu obnovitelných energií a souvisejícím úsporám z rozsahu .
Odvětví vodíku vyrábí, uchovává, propaguje a zdokonaluje výzkum vodíku a vodíku. V roce 2015 probíhají experimenty se zeleným (bezhlíkovým) vodíkem , ale tento plyn se stále „vyrábí hlavně ze zemního plynu ( fosilní ) a používá se jako chemická složka v průmyslových procesech“ , se špatnou uhlíkovou bilancí a významným příspěvkem k skleníkový efekt . Toto odvětví je nicméně prezentováno jako zajímavé pro udržitelný rozvoj , Protože:
- pokud je vyráběn elektrolýzou vody a bezuhlíkovým způsobem získáváním přerušovaných obnovitelných přebytků elektřiny (hlavně větrné a fotovoltaické), lze tento energetický vektor uložit, zejména v mezisezónních cyklech, pak použít při methanaci a / nebo vstřikováno do plynárenské sítě (6 až 20% objemu v závislosti na podmínkách), čímž se usnadní rovnováha a flexibilita elektrické sítě ;
- elektřina, která může být skladována díky své přeměně na plyn (vodík nebo metan), by umožnila ukládat „řádově jednu terrawatthodinu ročně“ a až několik desítek terawatthodin ročně elektřiny podle ADEME , kdy míra rozšíření obnovitelných energií ve skladbě elektřiny dosáhne 80%, a jako taková by mohla „významně přispět k přechodu na nízkouhlíkový energetický model, zejména v odvětví skladování energie“ ;
- vodík lze použít k místní výrobě elektřiny, ale se ztrátou účinnosti; že z elektrolýzy vody se blíží 70%, ale celková účinnost výroby elektřiny z H 2, by bylo kolem 25% v souladu s ADEME v roce 2020;
- vodík je kompatibilní s vlastní spotřebou v domácnosti, na ostrově nebo ve čtvrti, což umožňuje skladování na několik dní, týdnů nebo měsíců, navíc baterie jsou užitečnější pro krátkodobé skladování. Už by to bylo ekonomicky odůvodněné V oblastech, které nejsou propojeny s kontinentální elektrickou sítí ( např. Izolované ostrovy, francouzské zámořské komunity, kde výroba elektřiny stále závisí na palivu za vysoké náklady, v průměru 225 EUR / MWh v roce 2013 podle ADEME);
- vodík může pohánět určité flotily profesionálních vozidel , aniž by vyžadoval nákladnou síť několika stovek čerpacích stanic po celé zemi. Podle Ademe „ekonomický model stanice pro flotilu je dostupný pro denní spotřebu vyšší než 80 kg H 2 / den, pro uvádění vodíku na trh za méně než 10 EUR / kg “ . V tomto případě má výhody rychlé dobíjení a velká autonomie;
- vodík může být použit v ocelářském průmyslu jako náhrada uhlí nebo zemního plynu pro redukci železné rudy. Použití tohoto procesu ve Francii by spotřebovalo 700 000 tun vodíku, ale zabránilo by se emisím 22 MtCO 2/ rok, tedy téměř 5% emisí země, uvádí Francouzská asociace pro vodíkové a palivové články (Afhypac).
the 8. července 2020, Evropská komise představuje program pro rozvoj zeleného vodíku, který stanoví cíl, že vodík pokryje do roku 2050 12 až 14% energetických potřeb s cílem dekarbonizovat některá průmyslová a dopravní odvětví. Spoléhá se na vodík, aby přispěl k přechodu na energii a ke snížení emisí skleníkových plynů. Evropský komisař pro vnitřní obchod Thierry Breton zároveň oznamuje vytvoření vodíkové aliance.
Ve FranciiADEME zvažuje elektřiny směsi až 40% skládající se z „obnovitelných“ v roce 2035, a pak na 60% a 70% v roce 2050 (proti téměř o 18% v roce 2017, zatímco u většiny vodní zdroje).
Toto odvětví se snaží industrializovat své procesy, aby snížilo své náklady (zejména náklady na palivové články ). Rozvoju „vodíkové mobility“ brání také stále velmi nízký počet nabíjecích stanic (a jejich stále nízká kapacita: 10 až 80 kg H 2 / d při 350 barech). Vodík může ve srovnání s bateriemi zlepšit výkon vozidla, rozšířit jeho dojezd a zlepšit rychlost dobíjení.
Ademe se domnívá, že vodík bude hrát důležitou roli při přechodu na energii, jako vektor pro optimalizaci energetických sítí, pro ukládání energie při vlastní spotřebě solární nebo fotovoltaické energie a pro některá profesionální vozidla za podmínky, že svou energii dekarbonizuje. Výroba elektrolýzou za použití zelené elektřiny a transformaci biomasy ( parní reforming z bioplynu , pyrogasification pevné biomasy). Environmentální výkonnost tohoto odvětví bude záviset především na „primárním zdroji používaném k výrobě vodíku“. Agentura požaduje omezení přepravní vzdálenosti vodíku mezi výrobním místem a distribuční stanicí na méně než sto kilometrů. Pokud je to možné, měla by být upřednostňována vozidla na baterie (dojezd, dostupnost atd.), Vzhledem k lepšímu výkonu tohoto typu skladování a prioritou zůstávají úspory energie. Jednou z možností rozvoje (v současné době se testuje v letech 2018/2019) je injekce do plynové sítě ve Francii prostřednictvím dvou demonstrantů: GRHYD a Jupiter 1000 , aby se odstranily dosud existující technické překážky.
v června 2018, francouzská vláda pověřila Ademe zahájením „národního plánu zavádění vodíku“ (neboli „vodíkového plánu“) s cílem dát impuls tomuto odvětví, jehož „vysoký potenciál“ vnímají veřejní aktéři. Cílem vlády je „vytvořit francouzský průmyslový sektor bez uhlíku, otevřít nové perspektivy pro skladování obnovitelných energií a vyvinout řešení s nulovými emisemi pro dopravu“ . O rok později veřejná agentura uskutečnila několik výzev k předkládání projektů , včetně „Vodíkových mobilních ekosystémů“, které umožnily vybrat projekty „na všech územích“ a diverzifikované, například „dodávka na poslední míli v městských oblastech.“, Kolektivní osobní doprava autobusová nebo námořní kyvadlová doprava, půjčovna aut, sběr odpadu, obchodní a komunální flotily nebo dokonce použití těžkých nákladních vozidel jako stavebních vozidel “ .
CEA slibuje nové průmyslové elektrolýzy technologii zvanou rSOC s jedním drahých kovů: indium (kov, použitý v LCD obrazovky ), s nižšími teplotami (od 700 ° C do 800 ° C ) a nižší teplotě. Spotřebu energie. Je také reverzibilní, což umožňuje vyrábět vodík nebo obnovovat elektrickou energii, jako je palivový článek.
Na konci roku 2019 spojily společnosti Air Liquide a Engie své síly s Durance-Luberon-Verdon Agglomeration (DLVA) za účelem výroby, skladování a distribuce „zeleného vodíku“ (v rámci projektu „HyGreen Provence“ zahájeného v roce 2017 s cílem 1300 GWh solární elektřina a několik tisíc tun: rok vodíku vyrobeného elektrolýzou Dlouhodobě by mohlo být vyrobeno několik desítek tisíc tun obnovitelného vodíku, které lze skladovat v místní solné dutině .
Francouzská společnost McPhy , která již instalovala 17 MW výrobní kapacity vodíku tlakovou elektrolýzou, včetně 6 MW v Audi v Německu, oznamuje v lednu 2020 podpis inženýrské smlouvy na výrobní projekt 20 MW průmyslového zeleného vodíku , největšího dosud realizovaný projekt v Evropě, který se do roku 2022 nachází v nizozemském Delfzijlu. Závod bude vyrábět 3 000 tun vodíku ročně elektrolýzou vody pomocí větrné energie a bude využíván k výrobě bioethanolu. Projekt těží z 15 milionů eur v grantech Evropské unie a nizozemského fondu. Podle McPhyho bude správná stupnice 100 nebo 200 MW k dosažení konkurenceschopné ceny v tomto odvětví.
Zákon o energetickém klimatu z listopadu 2019 dává vládě jeden rok na zavedení podpůrného mechanismu pro „vodík vyrobený z obnovitelné energie nebo elektrolýzou vody pomocí nízkouhlíkové elektřiny“ . Před rokem 2023 je cílem víceletého energetického programu dekarbonizovat 10% vodíku spotřebovaného v průmyslu, což vyžaduje výrobu 90 000 tun zeleného vodíku. V lednu 2020 vláda vyhlašuje výzvu k vyjádření zájmu , jejímž cílem je otestovat chuť průmyslníků k tématu, které obdrželo více než 160 projektů. Například v lednu společnost H2V Industry eviduje žádosti o stavební povolení pro dva závody na výrobu vodíku v průmyslové oblasti Port-Jérôme v Normandii a na velkém námořním přístavu Dunkerque z obnovitelné energie; pokud se jim podaří těžit z podpůrného mechanismu, jejich uvedení do provozu by mohlo proběhnout v letech 2023–2024 a vyrobili by 56 000 tun vodíku. Postavili se také hlavní francouzští průmysloví hráči (Engie, EDF, Air Liquide, Vinci atd. ).
Vláda Castexu oznámila v září 2020 mnohem ambicióznější plán, než jaký představil Nicolas Hulot v roce 2018 a který má 100 milionů EUR: Plán 2020 plánuje do roku 2030 věnovat 7,2 miliardy EUR zelenému nebo nízkouhlíkovému vodíku, včetně 2 miliard EUR v letech 2021 a 2022 jako součást plánu obnovy. Vláda plánuje dotovat výrobu zeleného vodíku prostřednictvím výběrových řízení, vycházejících z obnovitelných zdrojů, a výstavby závodů na palivové články pro vodíková vozidla. Aby se předešlo duplicitě, uvažuje se o partnerství s Německem, které v červnu představilo plán vodíku ve výši 9 miliard EUR.
Tento vodíkový plán zahrnuje první součást ve výši 1,5 miliardy EUR věnovanou na výrobu elektrolyzérů s cílem snížit náklady jejím vylepšením a zvýšením objemů na kapacitu 6,5 GW . Druhá složka ve výši téměř jedné miliardy eur bude do roku 2023 použita na vývoj nabídky těžké vodíkové mobility snížením nákladů a zlepšením účinnosti palivových článků pro vlaky, nákladní automobily, autobusy a letadla prostřednictvím několika výzev k předkládání projektů (350 milionů eur pro demonstranti, 275 milionů na regionální experimenty atd.). Nakonec bude stimulována pomoc na výzkum a inovace, přičemž obálka se do roku 2023 zvýší na 650 milionů. Bruno Le Maire doufá, že tento plán vytvoří 50 000 až 150 000 přímých a nepřímých pracovních míst. Vláda zvažuje spolupráci s Německem označovanou jako „Airbus pro elektrolýzu“ jako „Airbus pro baterie“. Francie si stanovila za cíl vyrábět 600 000 tun ročně zeleného vodíku z bezuhlíkové elektřiny, obnovitelného nebo jaderného původu. Na rozdíl od Německa však Paříž nebude dotovat zachycování uhlíku ze „šedého“ vodíku. Bruno Le Maire doufá, že se dočká „vzniku francouzského odvětví elektrolýzy“: vedle gigantů, jako je Air Liquide, je také mnoho start-upů, jako je Lhyfe se sídlem v Nantes, která pro výrobce a místní úřady vyvíjí zelené závody na výrobu vodíku nebo dokonce McPhy , výrobce elektrolyzérů Drôme, jehož akcionářem je EDF.
V BelgiiTým KUL navrhuje prototyp 1,6 m 2 fotoelektrochemického článku produkujícího v průměru 250 litrů vodíku denně z atmosférických vodních par. Zařízení přeměňuje 15% sluneční energie na vodík a kyslík. A tato technologie nepoužívá drahé kovy ani jiné drahé materiály. S dvaceti panely by dobře izolovaný dům byl rok soběstačný v elektřině a topení.
Společnost Colruyt Group (významný belgický maloobchod) chce co nejvíce dekarbonizovat své aktivity. V roce 2018 bylo jedno z jeho logistických center vybaveno 75 výtahy poháněnými „bezuhlíkovým“ vodíkem a flotila nákladních vozidel musí být přestavěna do roku 2030. U plynového přehrávače se připravuje instalační projekt o výkonu 12 až 25 MW . (Rozšiřitelný) převádět elektřinu z větrných turbín na moři na vodík v průmyslovém měřítku.
V JaponskuNa konci roku 2017 Japonsko, hlavní dovozce energie, potvrdilo, že se chce stát lídrem jako „ vodíková společnost “ s cílem „nákladové parity“ s benzínem a LNG pro výrobu elektřiny. Stejně jako v minulosti v oblasti jaderné energie je vodík prezentován jako hlavní prostředek k dekarbonizaci energie, ale pilotní projekty vydají své závěry kolem roku 2020. V roce 2018 je v čele vodíkové mobility Japonsko, kde je téměř 2 500 automobilů s vodíkovými palivovými články. cirkulace a více než sto vodíkových stanic (ve srovnání s 45 v Německu, 42 ve Spojených státech a přibližně 20 ve Francii současně). Cílem země je rozdělit výrobní náklady do roku 2030 o více než tři, do roku 2050 pak o 80%. V letech 2013 až 2017 již japonský stát investoval 1,5 miliardy USD do výzkumu a vývoje a vývoje vodíku.
V Kaliforniiv října 2019, Kalifornie má 7 570 registrovaných vodíkových vozů a 42 amerických veřejných stanic.
V NěmeckuNěmecká vláda přijala ambiciózní plán pro rozvoj „zelených“ vodíku, obdařenou 9 miliard eur.
Vodíkový motor
Jaderná fúze: H bomba a fúzní reaktory
Nebezpečí, rizika a bezpečnostní opatření
Dihydrogen je plyn klasifikovaný jako „extrémně hořlavý “. Je charakterizován velmi širokým rozsahem hořlavosti (od 4 do 75% objemu ve vzduchu), což způsobuje deflagraci z velmi nízkého aktivačního energetického příkonu (jiskra stačí, pokud poskytuje a. Energii 0,02 milijoulů (mJ), zatímco trvá 0,29 mJ spouštět explozi v methanu ). Dihydrogen smíchaný s kyslíkem ve stechiometrických poměrech je silná výbušnina . Dihydrogen ve vzduchu je výbušná směs , když je H 2 / vzduch objemový poměr je mezi 13 a 65%
Historie jeho použití ve vzducholodi je plná vážných nehod, z nichž nejznámější je katastrofa v Hindenburgu . K LS 129 Zeppelin , nafouknutý 200.000 krychlových metrů vodíku (protože USA vyhlásila embargo proti Německu pro helium ) spálil06.05.1937po příletu na letiště Lakehurst poblíž New Yorku ). Z celkového počtu 97 naloděných zemřelo 36 lidí. Přítomná média široce zveřejňovala obrazy katastrofy, která vedla k veřejné nespokojenosti s balónky. Vyšetřování původu nehody, usnadněné množstvím fotografických dokumentů, však neosvědčilo výbuch vodíku, ale souvislé zapálení z požáru v obálce (pravděpodobně způsobeného výbojem statické elektřiny). Složení vodotěsného povlaku obalu (butyráty a hliník) by napomohlo prudké aluminotermické reakci . Nehoda by však byla mnohem méně násilná, kdyby byl balón nafouknutý heliem.
Nahrazení vodíku heliem (mnohem dražším a hustším) nevedlo k očekávanému oživení laskavosti. Strach z vodíku zůstal; „Hindenburg syndrom“ pravděpodobně nespravedlivě penalizován průmyslu.
Dihydrogen reaguje ještě prudčeji s chlorem za vzniku kyseliny chlorovodíkové (HCl), a to i bez aktivace, a s difluoridem za vzniku nebezpečné kyseliny fluorovodíkové (HF), a to i při teplotách, kdy je vodík kapalný a fluorovaný, přičemž druhá reakce je nejexotermnější chemickou látkou reakce existuje .
Standardní bezpečnostní byly posíleny s cílem řešit rizika vyvolaná průchodem v tunelech a parkování v garážích, nebo v podzemních parkovištích.
Globální předpisy o vozidlech se vyvíjejí pod záštitou OSN na základě návrhů výrobců, ale pokud jde o dihydrogen, japonští, američtí a evropští výrobci nesouhlasí. Evropská komise by mohla rozhodnout o prozatímních předpisech Společenství.
Ve Francii spolupracují INERIS a CEA s Mezinárodní organizací pro normalizaci ( ISO ) v technické komisi TC 197 pro riziko vodíku. Otázkou se zabývá i evropský projekt Hysafe , kde INERIS kritizoval návrh nařízení tím, že navrhl globálnější a systémový přístup, a nikoli podle komponent pro homologaci hybridních vozidel . V roce 2015 připravila společnost MEDDE aktualizaci předpisů pro čerpací stanice a flotily vozidel poháněných vodíkem.
Nebezpečí pro ozonovou vrstvu
Masivní uvolňování plynného vodíku zvýšilo hypotézu o riziku pro ozónovou vrstvu .
Bezpečnostní opatření
Následující body jsou pozoruhodné:
- vodík není ve své podstatě toxický;
- je osmkrát lehčí než metan. Jeho velmi malá molekula mu dává velmi dobrý difúzní koeficient ve vzduchu (čtyřikrát vyšší než metan); v neuzavřeném prostředí má tedy vodík tendenci stoupat a rychle se ředit ve vzduchu (je to bezpečnostní faktor na čerstvém vzduchu a nebezpečný faktor v omezených místech);
- jedná se o nejenergetičtější chemickou látku na jednotku hmotnosti (120 kJ / g ); ale na jednotku objemu plynu je teoretická výbušná energie 3,5krát nižší u vodíku než u zemního plynu;
- jeho spodní mez zapálení je 4% obj., srovnatelné se zemním plynem (5% obj.); ale jeho horní hranice zánětu je výrazně vyšší (75% proti 15%); to znamená, že v případě úniku se vodík vznítí mnohem snadněji než zemní plyn nebo kapalná paliva;
- energie potřebná k jeho zapálení při stechiometrii je také podstatně nižší (asi 10krát) než zemní plyn nebo propan;
- vodíkový plamen, bledě modrý, je během dne téměř neviditelný (riziko pro pohotovostní služby);
- vodíkový plamen se šíří asi sedmkrát rychleji než u zemního plynu a riziko detonace (exploze s velmi silným výbuchovým efektem) se zvyšuje díky vysokému koeficientu difuzivity.
Hořlavost lze dále snížit zředěním vodíku v héliu, a to i při velmi vysokých teplotách.
Odkaz OSN pro přepravu nebezpečných věcí
- Název (francouzsky): Stlačený vodík
- Třída: 2
- číslo: 1049
- Název (francouzsky): Chlazený kapalný vodík
- Třída: 2
- číslo: 1966
- Název (anglicky): Hydrogen in a metal hydride storage device
- Třída: 2
- číslo: 3468
Poznámky a odkazy
- vodíkové , bezpečnostní list (y) z mezinárodního programu o bezpečnosti chemických látek , konzultovat 9. května 2009,
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Vázaná kniha ( ISBN 978-1-4200-9084-0 ).
- Jean-Louis Vignes ( r. A člen francouzské chemické společnosti) a kol. , „ Dihydrogen: Fyzikálně-chemické údaje “ , propagace a vzdělávací místo týkající se chemických prvků (z periodické tabulky o Dmitrije Mendeleïev ), na lelementarium.fr , Paříži a Puteaux , Société Chimique de France a France Chimie (přístupné 3. listopadu 2019 ) .
- Pierre Ravarini (chemický inženýr a hydrolog), „ Gaz-Hydrogen “ , místo pro vědecké, technické a ekologické informace o vodě, Côte de Nacre ( Calvados ), 2019(přístup 3. listopadu 2019 ) .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 str. ( ISBN 978-0-387-69002-5 a 0-387-69002-6 , číst online ) , s. 294
- (en) Robert H. Perry a Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- „ Vlastnosti různých plynů “ na adrese flexwareinc.com (přístup 12. dubna 2010 )
- Zápis z Mezinárodní výbor pro míry a váhy , 78 th zasedání, 1989, pp. T1-T21 (a str. T23-T42, anglická verze).
- (in) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , s. 14-40.
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. června 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online prezentace ) , s. 5-89
- Magalie Roy-Auberger, Pierre Marion, Nicolas Boudet, Zplyňování uhlí , ed. Techniques of the Engineer, reference J5200 , 10 December 2009, p. 4
- „ Úřad pro radiační, chemickou a biologickou bezpečnost (ORCBS) “ (přístup k 16. dubnu 2009 )
- Nařízení ES n o 1272/2008 , 16 prosince 2008 [PDF] na EUR-Lexu , str. 923 : příloha VI, tabulka 3.1, indexové číslo .
- „ Vodík “ v databázi chemických produktů Reptox z CSST (quebecká organizace odpovědná za bezpečnost a ochranu zdraví při práci), zpřístupněno 23. dubna 2009
- „vodík“ , na ESIS , zpřístupněno 15. února 2009
- „ Objev zdrojů vodíku otevírá cestu k nové energii “ , Le Monde .
- „ Přírodní vodík, energie El Dorado? » , Sciences et Avenir .
- Lavoisierovy experimenty , na lavoisier.cnrs.fr
- „ Vodíková energie “ , o znalostech energií ,30. srpna 2011(zpřístupněno 10. prosince 2019 ) (aktualizováno9. dubna 2015).
- výtěžek vodíkového řetězce (technický list), Ademe ,ledna 2020( číst online [PDF] ).
- „ Detekce přirozených vyzařování vodíku pomocí satelitních snímků - zahájení projektu sen4H2 “ , na IFP Énergies nouvelles (přístup 6. dubna 2019 ) .
- „ Hlubinné nerostné zdroje “ na Ifremer (přístup 28. října 2019 ) .Článek představuje mapu mořského dna, která udává známé hadovité rozdělení podél hřebenů.
- Sylvestre Huet , „ Nativní vodík, nový zdroj energie? » , Na sciences.blogs.liberation.fr , Liberation ,23.dubna 2013(přístup 28. října 2019 ) .
- „ Reakce mořského pláště: hadovitá formace “ , na Ifremeru (přístup 28. října 2019 ) .
- „ Syntéza vodíku, metanu a uhlovodíků v hlubokém moři, směrem k novým energetickým zdrojům ... “ , Ifremer (přístup 28. října 2019 ) .
- " Vodík, to ano, ale přírodní vodík " , na La Tribune ,28. června 2018(přístup 3. října 2020 ) .
- Přírodní vodík: příspěvek ke skladbě zdrojů energie? , IFP Nové energie ,11. dubna 2013.
- Julia Guélard , Charakterizace přirozeného vyzařování vodíku v intrakratonickém kontextu: příklad interakce plyn / voda / hornina v Kansasu (disertační práce z geochemie), Pierre-et-Marie-Curie University a IFP Énergies nouvelles ,2016( online prezentace , čtení online ).
- (in) J. Guélard , V. Beaumont , V. Rouchon a F. Guyot , „ Přírodní H2 v Kansasu: Hluboký zlatý mělký původ? » , Geochemistry, Geophysics, Geosystems , vol. 18, n o 5,3. dubna 2017, str. 1841–1865 ( ISSN 1525-2027 , DOI 10.1002 / 2016GC006544 , abstrakt , číst online , přístup 28. října 2019 ).
- Alain Prinzhofer, Eric Deville, přírodní vodík - další energetická revoluce? , Ed. Belin, 2015 ( ISBN 978-27011-83848 ) .
- J. Guélard a kol. „ Přírodní H 2 v Kansasu: Hluboký nebo mělký původ? ", Geochemie, Geofyzika, Geosystémy ,dubna 2017( DOI 10.1002 / 2016GC006544 , online prezentace , čtení online [PDF] , přístup 25. října 2109 ).
- (in) Isabelle Moretti, Emyrose Brouilly, Keanu Loiseau, Alain Prinzhofer Eric Deville, „ Hydrogen Fumes in Intracratonic Areas: New Guide Lines for Early Screening Basin Exploration “ na hmdpi.com ,22. března 2021(zpřístupněno 16. června 2021 )
- (in) Maria Rosanne Fabian Rupin Louis Gorintin Julio Aguilar, Helena-Fog, Werly Julien Olivier Lhote, Xi Yao, „ SYSTÉM PARHYS: NOVÝ PŘÍSTUP K MĚŘENÍM KONCENTRACE H2 V PODPOVRCHU “ na hnatsummit.com ,26. dubna 2021(zpřístupněno 16. června 2021 )
- (in) H. Hosgormez G. Etiope a MN Yalçin , „ Nové důkazy pro smíšený anorganický a organický původ olympijského ohně Chimaera (Turecko): širokoúhlý prosak plynu abiogenního “ , Geofluids , sv. 8, n O 4,25. listopadu 2008, str. 263–273 ( DOI 10.1111 / j.1468-8123.2008.00226.x ).
- " Bourakébougou: příslib vodíkové elektrárny " ,18. února 2013(přístup 28. října 2019 ) .
- „ Vodík podle Isabelle Moretti - Sciences et Avenir “ , Sciences et Avenir (přístup 2. června 2021 ) .
- (in) „Sopečné plyny: spalování vodíku u sopky Kilauea na Havaji“ na mendeley.com.
- (en) Deep Hydrogen na astrobio.net.
- (cs) GJ MacDonald (1988). „Hlavní otázky týkající se hlubokých kontinentálních struktur“ Hluboké vrtání v krystalickém podloží, v. 1 : 28–48 s., Berlín: Springer-Verlag. .
- „ Přírodní vodík je podle CNRS mnohem důležitějším zdrojem, než se domnívalo “ , na adrese http://erh2-bretagne.mystrikingly.com ,11. května 2019(přístup 12. listopadu 2019 ) .
- Isabelle Moretti, „ Přírodní vodík: geologická zvědavost nebo hlavní zdroj energie v budoucnosti?“ » , O znalostech energií .
- „ 15. dubna 1988 letí Tu-155 na vodík “ , na Aerobuzzu ,2. října 2020(přístup 12. listopadu 2020 )
- Vodík, nové energetické technologie. CEA klíče, n o 50/51, zima 2004-2005, ( ISSN 0298-6248 )
- Evropský projekt StorHy report, s. 8, míra ztráty vodíku
- Článek Tribune Evropa financuje obří baterii na skladování obnovitelné energie
- (in) T. Mitsui, MK Rose E. Fomin, DF Ogletree a M. Salmeron, „ Disociační adsorpce vodíku je palladium vyžaduje agregáty tří nebo více volných míst “ , Nature , sv. 422,17. dubna 2003, str. 705-707 ( DOI 10.1038 / nature01557 , číst online [PDF] ).
- (cs) Budoucnost vodíku - chopení se dnešních příležitostí [PDF] , International Energy Agency , červen 2019.
- (in) Cesty dekarbonizace plynů 2020-2050 , Plyn pro klima,duben 2020, 226 s. ( číst online [PDF] ) , str. 17.
- „ Plán obnovy: jaké místo pro energii? » , Na connancedesenergies.org ,4. září 2020.
- (in) „ Vodík vyrobený z jaderné energie bude považován za„ nízkouhlíkový “, uvádí úředník EU „ [„Vodík vyrobený z jaderné energie bude podle představitele EU považován za„ nízkouhlíkovou stopu “»], EURACTIV ,19. listopadu 2020.
- „ Francouzský vodíkový plán diskrétně potvrzuje oživení jaderné energie “ , na Reporterre ,2. února 2021.
- „ Přírodní vodík: geologická kuriozita nebo hlavní zdroj energie v budoucnosti?“ » , Na connancedesenergies.org ,22. května 2020.
- „ Zelený vodík, chybějící článek v přechodu “ , Alternatives économique (přístup k 8. srpnu 2020 ) .
- Interakce (dopis akcionářům Air Liquide), Air Liquide , září 2015 [PDF] , s. 5 .
- (in) Liz Gyekye [ https://biomarketinsights.com/australia-backs-tech-that-converts-biogas-into-hydrogen-and-graphite/ „Austrálie podporuje technologii, která přeměňuje bioplyn na vodík a grafit“] Biomarketingové památky , 4. září 2019.
- Jérôme Marin, „ Lhyfe bude vyrábět zelený vodík pomocí větrných turbín “ , La Tribune ,17. ledna 2020.
- „Ademe uvádí„ hlavní příspěvky “vodíku k energetickému přechodu“ , Connaissance des energies , 4. dubna 2018.
- Vodíkový vektor v energetickém přechodu , stanovisko ADEME, duben 2018 [PDF] .
- Séverine Fontaine, " ADEME chce vodíku z obnovitelných zdrojů energie ", L'automobily & L'Entreprise , n o 5,února 2016( číst online ).
- „ Evropská komise představila svůj plán rozvoje zeleného vodíku “ na EnerGeek ,10. července 2020(zpřístupněno 11. července 2020 ) .
- Vodík v energetickém přechodu , Ademe , únor 2016, 7 stran [PDF] .
- Joseph Martin , „ Vývoj vodíku, ADEME bilancuje “ , v časopise RSE Magazine (přístup 17. května 2019 ) .
- „ Vědci z Grenoble optimalizují umělou fotosyntézu na produkci vodíku “ , na placegrenet.fr ,21. dubna 2018(přístup 30. března 2019 ) .
- Véronique Pouzard, „ Vysokoteplotní elektrolýza CEA prováděná start-upem Sylfen “ , Les Échos ,26. února 2019(přístup 30. března 2019 ) .
- AFP (2019) „Zelený“ vodík: spolupráce mezi společnostmi Air Liquide, Engie a Durance, Lubéron, aglomerace Verdon ; 13. listopadu 2019
- McPhy ve středu největší jednotky na výrobu vodíku s nulovými uhlíky v Evropě , Les Échos , 22. ledna 2020.
- Plán obnovy: Francie mění měřítko vodíku , Les Échos , 3. září 2020.
- Vodík: Francie podrobně popisuje svůj plán na 7 miliard eur , Les Échos , 8. září 2020.
- Vodík: vláda chce vytvořit „Airbus pro elektrolýzu“ , Les Échos , 8. září 2020.
- (in) „ Vědci z KU Leuven prolomí kód cenově dostupného vodíkového plynu šetrného k životnímu prostředí “ , na KU Leuven (přístup k 31. říjnu 2019 ) .
- „ Belgičtí vědci vyvíjejí solární panel, který vyrábí vodík “ , na RTBF Info ,1 st 03. 2019(zpřístupněno 31. října 2019 ) .
- „ Skupina Colruyt: sázka na mobilitu vodíku “ , na RTBF Info ,8. října 2018(zpřístupněno 31. října 2019 ) .
- „ Colruyt a Fluxys chtějí postavit vodíkovou elektrárnu, první v Belgii “ , Le Soir ,8. října 2019(zpřístupněno 31. října 2019 ) .
- „ Jízda na vodík: naše zkušenosti “ , automobil Le Moniteur (přístup 31. října 2019 ) .
- (en) Monica Nagashima (Institute of Energy Economics, Japonsko), japonská vodíková strategie a její ekonomické a geopolitické důsledky , Institut français des relations internationales , říjen 2018 [PDF] .
- „„ Vodíková strategie “Japonska“ , Znalosti energií, 9. října 2018.
- (in) „ Alternativní paliva v datovém centru: Prázdniny na čerpací stanici na vodík “ , v datovém centru na alternativní paliva , ministerstvo energetiky USA (přístup k 31. říjnu 2019 ) .
- Benoît Le Floc'h, „ A co vodík pro lehká užitková vozidla? » , Na Caradisiac ,29. listopadu 2018(přístup 30. března 2019 ) .
- „ Kalifornie překonává milník 7500 vodíkových automobilů v oběhu “ , na www.h2-mobile.fr (přístup k 31. říjnu 2019 ) .
- (in) „ Německá vláda přijímá strategii vodíku “ [„Německá vláda přijímá strategii pro vodík“], o federální vládě (Německo) ,10. června 2020.
- Vodíková nehoda , ministerstvo ekologie, energetiky, udržitelného rozvoje a regionálního plánování , 18 s. ( číst online [PDF] ) , str. 4.
- Radisson, Laurent (2015) Vodíková rizika: Ministerstvo ekologie pracuje na nových textech; ; News env, publikováno 21. října 2015
- T. Rahn, JM Eiler, KA Boering, PO Wennberg, MC McCarthy, S. Tyler, S. Sc Chauffage, S. Donelly, E. Atlas, Extreme deuterium enrichment in stratosphere hydrogen and the global atmospheric budget of H2 , Nature 424 918-921, 2003.
- TK Tromp , RL Shia pan Allen , JM Eiler a YL Yung , " Potenciální dopad na životní prostředí vodíkové hospodářství na stratosféry ," Science , n o 300,2003, str. 1740-1742 ( DOI 10.1126 / věda.1085169 ).
- Céline Duguey, „ Výbušná zkušenost “ , na Espace des sciences ,září 2009(zpřístupněno 16. dubna 2020 ) .
- (v) Florent Tonus Mona Bahout , Paul F. Henry a SIAN E. Dutton , " Použití v situneutron difrakce pro sledování vysoké teploty, pevná látka / H2 plynů reakce " , Chemical Communications , n o 18,21. dubna 2009, str. 2556–2558 ( ISSN 1364-548X , PMID 19532888 , DOI 10.1039 / B822419F , číst online , přístup k 16. dubnu 2020 ).
Podívejte se také
Bibliografie
- Yver, Camille, Kvantifikace využití vodíku v půdě: od lokálního po globální měřítko , 2011 DOI: 10.4267 / 2042/47372 ( shrnutí - Prix Prud'homme 2011.
- Stephen Boucher, The Hydrogen Revolution. Směrem k čisté a efektivní energii? , předmluva Thierry Alleau, Paříž, Éd. du Felin, 2006, 160 s. , ( ISBN 2-86645-616-5 ) .
- Alain Prinzhofer, Eric Deville, Přírodní vodík - příští energetická revoluce? , Belin, 2015 ( ISBN 978-27011-83848 )
Související články
externí odkazy
- Francouzská asociace pro vodík
- Evropská síť / Pole kompetence
- Vývoj H2
- CEA Technologies, Hydrogen, new energy technologies , Clefs CEA n o 50-51), 23. března 2005
- Vodík viděný CEA
- INERIS: zažijte zpětnou vazbu spojenou s problémy s úložištěm
- Vodík viděný Francouzskou chemickou společností
- Spor o používání vodíku jako paliva
- Vše o vodíkové alternativě s tiskovou recenzí, internetovými odkazy a videi








