Octová kyselina
| Kyselina etanová | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
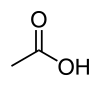
| Skeletální vzorec a 3D znázornění kyseliny octové | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Název IUPAC | kyselina ethanová | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Systematický název | octová kyselina | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyma |
ledová kyselina |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o ECHA | 100 000 528 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ne o EC | 200-580-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O RTECS | AF1225000 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC kód | G01 S02 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03166 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 176 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 15366 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O E | E260 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2006 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ÚSMĚVY |
CC (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H4O2 / c1-2 (3) 4 / h1H3, (H, 3,4) / f / h3H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | bezbarvá kapalina s pronikavým zápachem a silně octem. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hrubý vzorec |
C 2 H 4 O 2 [izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární hmotnost | 60,052 ± 0,0025 g / mol C 40%, H 6,71%, O 53,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 4,76 při 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolární moment | 1,70 ± 0,03 D. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekulární průměr | 0,442 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T. fúze | 16,64 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° vroucí | 117,9 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpustnost | Mísitelný s vodou, acetonem , alkoholem, benzenem , glycerolem , etherem, tetrachlormethanem ; Prakticky drzý. v sirouhlíku | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametr rozpustnosti δ | 20,7 MPa 1/2 ( 25 ° C ); 18,9 J 1/2 cm -3 / 2 ( 25 ° C ); |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
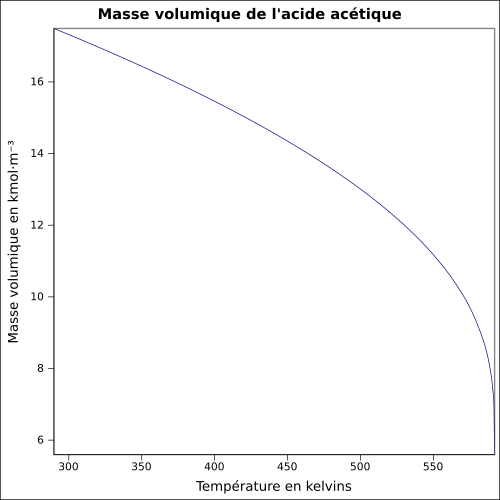
| Objemová hmotnost |
1,049 2 g cm −3 (kapalina, 20 ° C )
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota samovznícení | 465 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bod vzplanutí | 39 ° C (uzavřený kelímek) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Meze výbušnosti ve vzduchu | 5,4–16 % obj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak nasycených par |
1,5 kPa při 20 ° C
rovnice:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynamická viskozita | 1,22 mPa s při 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritický bod | 4,53 MPa při 319,56 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 plyn, 1 bar | 282,848 J mol −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 kapalina, 1 bar | 158,0 J mol -1 K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 plyn | −433 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 kapalina | -483,52 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 11,728 kJ mol -1 až 16,75 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 23,7 kJ mol −1 až 117,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C str |
123,1 J mol -1 K -1 (kapalina, 25 ° C ) 63,44 J mol -1 K -1 (plyn, 25 ° C ) rovnice:
rovnice:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 874,2 kJ mol -1 (kapalina) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -875,16 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionizační energie | 10,65 ± 0,02 eV (plyn) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Křišťálová třída nebo vesmírná skupina | Pna 21 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametry sítě |
a = 13,151 Á b = 3,923 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objem | 297,27 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optické vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Index lomu | 1,3720 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Opatření | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Nebezpečí H226, H314, P280, P305, P310, P338, P351, H226 : Hořlavá kapalina a páry H314 : Způsobuje těžké poleptání kůže a poškození očí P280 : Noste ochranné rukavice / ochranný oděv / ochranné brýle / obličejový štít. P305 : Při zasažení očí: P310 : Okamžitě volejte TOXIKOLOGICKÉ INFORMAČNÍ STŘEDISKO nebo lékaře. P338 : Vyjměte kontaktní čočky, pokud je oběť nosí a lze je snadno vyjmout. Pokračujte v oplachování. P351 : Několik minut opatrně opláchněte vodou. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  B3, E, B3 : Bod vzplanutí hořlavé kapaliny = 39 ° C uzavřený kelímek (metoda není uvedena) E : Žíravý materiál Přeprava nebezpečných věcí: třída 8 Zveřejnění 1,0% podle seznamu údajů o složce |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 3 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doprava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
83 : žíravý nebo vykazující menší stupeň korozivity a hořlavý (bod vzplanutí 23 až 60 ° C , včetně mezních hodnot) UN číslo : 2789 : ROZTOK KYSELINY OCTOVÉ obsahující více než 80% (hmotnostní) kyseliny; nebo KYSELINA GLACIÁLNÍ Třída: 8 Štítky: 8 : Žíravé látky 3 : Hořlavé kapaliny Balení: Obalová skupina II : středně nebezpečné látky;  
80 : žíravý nebo vykazující mírný stupeň žíravosti UN číslo : 2790 : KYSELINA KYSELINA OCTOVÁ Třída: 8 Štítek: 8 : Žíravé látky Balení: Obalová skupina II / III : mírně / mírně nebezpečné látky.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoxikologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 3,31 g kg -1 (potkan, orálně ) 525 mg kg -1 (myš, iv ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0,31 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prahová hodnota zápachu | nízká: 0,03 ppm vysoká: 0,15 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Související sloučeniny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izomer (y) | Glykolaldehyd | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jiné sloučeniny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednotky SI a STP, pokud není uvedeno jinak. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ethanové nebo kyselina octová je karboxylová kyselina s teoretickým C2 uhlíkovým řetězcem, podobně jako ethan , molární hmotnost 60 g / mol a chemický vzorec surový C 2 H 4 O 2 , částečně rozvinuté CH 3 - CO-OH nebo AcOH krátká formace , kde Ac znamená „ CH 3 CO “, od acetylové skupiny . Přídavné jméno běžného názvu pochází z latinského acetum , což znamená ocet . Kyselina octová ve skutečnosti představuje hlavní složku octa po vodě, protože jí dodává kyselou chuť a štiplavý zápach zjistitelný od 1 ppm .
Destilace octa, doložená ze středověku v Evropě, umožnila získat čistou kyselinu octovou, bezbarvou hořlavou kapalinu se silným octovým zápachem, s hustotou kolem 1,05 g cm −3 při 20 ° C, která ztuhne jednoduchým ponořením v lázni s ledovou vodou. To je ještě známé jako ledová kyselina octová nebo dříve silný ocet . Je to první známá průmyslová kyselina .
Tato velmi slabě vodivá, bezbarvá, hořlavá a hygroskopická kapalina představuje při teplotě místnosti jednu z nejjednodušších monokarboxylových kyselin spolu s kyselinou mravenčí . Obsah kyselin vyznačující se tím, vodném roztoku o pK = 4,76 pochází z jeho schopnosti dočasně ztratit proton své karboxylové funkce , čímž se transformuje ji na acetát ion CH 3 COO - . Je to slabá kyselina .
Tato kyselina koaguluje latex a má bakteriostatické vlastnosti, což umožňuje jeho použití jako dezinfekčního prostředku. Používá se také jako složka insekticidů a čisticích prostředků pro výrobu polovodičů. Je žíravý a jeho páry dráždí nos a oči.
Je velmi korozivní vůči organickým a živým tkáním, je třeba s ním zacházet opatrně. Ačkoli nebylo zjištěno, že je karcinogenní nebo škodlivý pro životní prostředí, může způsobit popáleniny a trvalé poškození úst, nosu, krku a plic. Při určitých dávkách a při chronické souběžné expozici s karcinogenním produktem je jeho dráždivá povaha nádorovým promotorem nádorů (benigních a maligních). To bylo experimentálně prokázáno na potkanech.
V lidském těle se kyselina octová normálně vyrábí po konzumaci alkoholu : ethanol se přemění na acetaldehyd, který se poté pomocí enzymu acetaldehyddehydrogenázy převede na kyselinu octovou a poté pomocí acetát-CoA ligázy na acetyl-coA .
Výroba
Globální poptávka po kyselině octové je přibližně 6,5 milionu tun ročně (Mt / a). Průmyslově se vyrábí oxidací n- butanu v kapalné fázi nebo se získává při výrobě acetátu celulózy nebo polyvinylalkoholu .
Použití
Jedná se o činidlo široce používané v průmyslu nebo laboratořích, zejména:
- jako rozpouštědlo: mísitelné s vodou a různými organickými rozpouštědly, jako je ethanol , diethylether , glycerol, ale nerozpustné v sirouhlíku , je také dobrým rozpouštědlem pro gumy , pryskyřice , fosfor , síru a halogenovodíkové kyseliny ? ;
- při výrobě anhydridu kyseliny octové , acetátu celulózy , monomeru vinylacetátu a jiných acetátů, jakož i léčiv , pesticidů , barviv , výroby fotografických produktů;
- v potravinách (výroba ovocných octů atd.), potravinářská přídatná látka ;
- textilní ;
- jako čisticí prostředek (pro polovodiče );
- koagulant ( přírodní latex );
- bakteriostatický (v roztoku);
- při výrobě plastů, jako je polyethylentereftalát (PET) nebo acetát celulózy , užitečné pro výrobu vinylacetátu (barvy, lepidla) a organických rozpouštědel;
- jako přísada do tabákových výrobků ( aromata ).
- leptání během barvení histologických řezů (např .: karmínově zelené barvení )
- proces hydrolýzy , kondenzace a / nebo gelace při výrobě katalyzátoru nebo během procesu sol-gel
- antibakteriální a žaludeční acidifikace v chovu, zejména u prasat.
Nomenklatura
Bývalý triviální název kyselina octová pochází z acetumového slova latina, což znamená ocet nebo aceti-vinum . Stále je nejpoužívanější ve frankofonním a anglicky mluvícím světě, ale IUPAC standardizoval termín kyselina ethanová místo starého francouzského chemického názvu kyselina ethylová . Více tolerantní než nomenklatura IUPAC v roce 1960, Chemical Abstracts si přesto zachovaly běžné názvy pro první dvě karboxylové kyseliny v C1 a C2, kyselinu mravenčí a kyselinu octovou.
Ledová kyselina octová je také triviální název, který se v laboratoři běžně označuje jako čistá kyselina octová. Podobně jako německý název „Eisessig“ (doslovně: ledový ocet), je tento název vysvětlen ledovými krystaly kyseliny octové, které se tvoří při teplotě mírně pod pokojovou teplotou (pod 17 ° C). , Bod tání čisté kyseliny octové kyselina).
Nejběžnější zkratka pro kyselinu octovou je AcOH nebo HOAc, Ac označující acetylovou funkční skupinu CH 3 -CO-.
Molekulární vzorec pro kyselinu octovou je C 2 H 4 O 2 . To je také často psaný CH 3 COOH nebo CH 3 CO 2 H, aby se lépe překládat jeho strukturu. Ion vznikající při ztrátě H + protonu se nazývá acetát. Acetát může také znamenat sůl obsahující tento anion nebo ester kyseliny octové.
Historický
Silný ocet je v Mezopotámii znám více než 3000 let před naším letopočtem. AD . Tyto kyseliny octové bakterie produkující kyselinu octovou z vína a kyslíku byly popsány lékárnou Louis Pasteur . Jsou přítomny po celém civilizovaném světě a každá kultura praktikující pivo nebo vaření vína nevyhnutelně objevila ocet, přirozený výsledek vývoje těchto alkoholických nápojů, který zůstal otevřený.
Použití kyseliny octové v chemii sahá až do starověku. Na III th století před naším letopočtem. AD , řecký filozof Theophrastus, popisuje, jak ocet působí na kov a produkuje tak pigmenty užitečné pro umění, včetně bílého olova ( uhličitan olovnatý ) a verdigris , zelené směsi solí mědi včetně octanu měďnatého II (všechny toxické produkty ). Staří Římané vařili „ kyselé víno “ v olověných nádobách a vyráběli velmi sladký sirup zvaný sapa . Sapa byl bohatý na octan olovnatý , sladká látka zvaná olovo cukr nebo Saturn cukr , a která způsobila mnoho olova otravy v římské aristokracie se nemoc odpovídající akutní nebo chronické olova otravy je pozoruhodně pojmenované otrava olovem . Perský alchymista Geber (Geber) koncentroval kyseliny octové z octa o destilační .
Během renesance byla „ledová“ kyselina octová připravována suchou destilací octanů kovů. Na XVI th století německý alchymista Andreas Libavius v popsaného postupu, a ve srovnání se čisté kyseliny takto vyrobeného kyselé. Přítomnost vody v octě má takový vliv na vlastnosti kyseliny octové, že po celá staletí mnoho chemiků věřilo, že ledová kyselina octová a kyselina v octě jsou dvě různé látky. Byl to francouzský chemik Pierre Auguste Adet, který dokázal, že jde o stejnou chemickou sloučeninu.
V roce 1847 německý chemik Hermann Kolbe poprvé syntetizoval kyselinu octovou z anorganických materiálů. Sekvence této reakce byl chlorace ze sirouhlíku do tetrachlormethanu a následnou pyrolýzou na tetrachlorethylen a chloračního vody v kyselině trichloroctové , a nakonec se uzavře s redukcí pomocí elektrolýzy k získání kyseliny octové.
Do roku 1910 byla většina ledové kyseliny octové získána z „pyroligenního louhu“ vyrobeného destilací dřeva. Kyselina octová byla izolována zpracováním s hydroxidem vápenatým a takto získaný octan vápenatý byl poté okyselen přidáním kyseliny sírové za účelem reformování kyseliny octové. V té době z toho Německo vyprodukovalo 10 000 tun ročně, z toho 30% bylo použito na výrobu indigového barviva .
Fyzikálně-chemické vlastnosti
Kyselost
Atom vodíku (H) karboxylové skupiny (–COOH) karboxylových kyselin, jako je kyselina octová, se může uvolňovat jako iont H + ( proton ). Je to schopnost uvolňovat tento proton, který mu dodává kyselost. Kyselina octová je slabá kyselina , mono-proton ve vodném roztoku, s pK asi 4,8 až 25 ° C . Roztok 1,0 mol / l (koncentrace octa pro domácnost) má pH 2,4, což znamená, že je disociováno pouze 0,4% molekul kyseliny octové.
Cyklický dimer
Krystalová struktura kyseliny octové ukazuje, že molekuly se párují do dimerů spojených vodíkovými vazbami . Tyto dimery mohou být také pozorovány v plynné formě při teplotě 120 ° C . Pravděpodobně jsou také přítomny v kapalné fázi čisté kyseliny octové, ale při nejmenší přítomnosti vody se rychle rozloží. Tato dimerizace existuje v jiných karboxylových kyselinách. Probíhá také ve vodném roztoku s asociační konstantou K D, jejíž hodnota je blízká 1.
Solventní
Kapalná kyselina octová je hydrofilní ( polární ) protické rozpouštědlo , podobné ethanolu a vodě . S průměrnou dielektrickou konstantou 6,2 může rozpouštět nejen polární sloučeniny, jako jsou anorganické soli a cukry , ale také nepolární sloučeniny, jako jsou oleje, nebo čisté látky, jako je síra a diod . Snadno se mísí s mnoha dalšími polárními nebo nepolárními rozpouštědly, jako je voda, chloroform nebo hexan . Tyto vlastnosti rozpouštědla a mísitelnost kyseliny octové ji činí široce používanou v chemickém průmyslu.
Chemické reakce
Kyselina octová korozivně působí na mnoho kovů , včetně železa , hořčíku a zinku . Tvoří vodík a kovové soli zvané acetáty . Hliníku vznikají při styku s kyslíkem tenká vrstva oxidu hlinitého je relativně odolná, která pokrývá jeho povrch. Hliníkové nádrže se proto často používají k přepravě kyseliny octové. Kovové acetáty může být vyroben ze směsi kyseliny octové a vhodné báze, jako je tomu v roztoku hydrogenuhličitanu + ocet reakce , která dává voda a CO 2 . S výraznou výjimkou octanu chromitého jsou téměř všechny acetáty rozpustné ve vodě.
- Mg ( s ) + 2 CH 3 COOH ( aq ) → (CH 3 COO) 2 Mg (aq) + H 2 ( g )
- NaHCO 3 (y) + CH 3 COOH (aq) → CH 3 COONa (aq) + CO 2 (g) + H 2 O ( l )

Kyselina octová také prochází typické reakce karboxylových kyselin , zejména tvorbu ethanolu o snížení a tvorbu derivátů, jako je například acetylchlorid podle nukleofilní substitucí acyl . Mezi další náhradní deriváty patří anhydrid kyseliny octové . Tento anhydrid je výsledkem ztráty jedné molekuly vody dvěma molekulami kyseliny octové. Estery kyseliny octové může být vyškolen v Fischer esterifikaci , a to může být také použit k výrobě amidů . Kyselina octová se při teplotě nad 440 ° C rozkládá na oxid uhličitý a metan nebo vodu a keten .
Detekce
Kyselinu octovou lze detekovat podle jejího charakteristického zápachu. Soli kyseliny octové rozpuštěné v roztoku chloridu železitého dávají tmavě červené zabarvení, které po okyselení zmizí. Zahříváním acetátů s oxidem arzenitým se získá kakodyloxid, který lze identifikovat podle jeho páchnoucích par.
Biochemie
Acetylová skupina , odvozený od kyseliny octové, je zásadní pro biochemii téměř celý život. Po propojení s koenzymu A , má velký význam v metabolismu ze sacharidů a lipidů . Koncentrace volné kyseliny octové v buňkách je však udržována nízká, aby nedošlo k narušení kontroly pH. Na rozdíl od jiných karboxylových kyselin s dlouhým uhlíkovým řetězcem ( mastných kyselin ) se kyselina octová neobjevuje při tvorbě přírodních triglyceridů . Existuje umělý triglycerid kyseliny octové, triacetin (glyceryltriacetát), který se běžně používá jako potravinářská přídatná látka (v kosmetice, potravinách a některých lécích) a jako rozpouštědlo .
Kyselina octová je přirozeně produkována a vylučována určitými bakteriemi, zejména Acetobacter a Clostridium acetobutylicum (en), jakož i kvasinkami Saccharomyces cerevisiae .
Tyto bakterie jsou přítomny v určitých potravinách, vodě, mléku ( bakterie mléčného kvašení ) a půdě a kyselina octová se přirozeně tvoří při rozpadu ovoce nebo jiných potravin. Kyselina octová je také součástí vaginálního mazání u lidí a jiných primátů , kde se zdá, že funguje jako antibakteriální látka .
Výroba a syntéza
Kyselina octová se vyrábí synteticky nebo bakteriální fermentací. Dnes se ekologická metoda týká pouze 10% produkce, ale pro výrobu octa je i nadále důležitá, protože ve většině zemí zákon stanoví, že ocet pro použití v potravinách musí být organického původu. Asi 75% kyseliny octové pro chemický průmysl se vyrábí karbonylací z methanolu , podrobnosti viz níže. Zbytek tvoří různé alternativní metody.
Celková produkce kyseliny octové se odhaduje na 5 Mt / rok (miliony tun ročně), z čehož asi polovina pochází ze Spojených států. Evropská produkce se pohybuje kolem 1 Mt / a klesá. Nakonec je v Japonsku vyrobeno 0,7 Mt / a . 1,5 Mt / a se recykluje, což zvyšuje světový trh na 6,5 Mt / a . Dva největší producenti jsou Celanese a BP Chimie. Hlavními producenty jsou také Millenium Chimie, Sterling Chimie, Samsung, Eastman a Svens Etanolkemi.
Karbonylace methanolu
Většina z nerecyklovaného kyseliny octové se vyrábí karbonylací z methanolu . V tomto procesu reaguje methanol a oxid uhelnatý za vzniku kyseliny octové podle rovnice: CH 3 OH + CO → CH 3 COOH
Tento proces využívá jako meziprodukt kyselinu jodovodíkovou a probíhá ve třech stupních. Pro karbonylaci je zapotřebí katalyzátor , obvykle kovový komplex (krok 2).
- CH 3 OH + HI → CH 3 I + H 2 O
- CH 3 I + CO → CH 3 COI
- CH 3 COI + H 2 O → CH 3 COOH + HI
Úpravou procesu lze ve stejné továrně vyrábět anhydrid kyseliny octové . Vzhledem k tomu, že metanol a oxid uhelnatý jsou běžnými surovinami, karbonylace methanolu se již dlouho stala atraktivní metodou pro výrobu kyseliny octové. Henry Dreyfus z British Celanese vyvinul pilotní karbonylační zařízení na metanol již v roce 1925. Avšak nedostatek adekvátního vybavení, které by obsahovalo korozivní reakční směs při nezbytných tlacích ( 200 atm nebo více), na nějakou dobu brzdilo komercializaci této metody. . První komercializovaný Způsob karbonylace methanolu, který používá kobalt jako katalyzátor, byl vyvinut německé chemické společnosti BASF v roce 1963. V roce 1968, nový katalyzátor na bázi rhodia ( cis - [Rh (CO) . Byla objevena 2 I 2 ] - ) schopné účinně působit při nízkém tlaku as velmi malým počtem vedlejších produktů. První závod využívající tento katalyzátor byl postaven americkou společností Monsanto v roce 1970 a karbonylace methanolu katalyzovaného rhodiem se stala dominantní metodou výroby kyseliny octové (známý jako Monsanto proces ). Ke konci 90. let 20. století uvedla společnost BP na trh katalyzátor Cativa ([Ir (CO) 2 I 2 ] - ), zvýhodněný rutheniem. Tento proces je šetrnější k životnímu prostředí a účinnější než ten předchozí a do značné míry nahradil proces společnosti Monsanto, často ve stejných továrnách.
Oxidace acetaldehydu
Předtím, než se proces Monsanto byl komerčně, většina kyseliny octové se vyrábí oxidací z acetaldehydu . Tato metoda zůstává druhým nejdůležitějším způsobem syntézy kyseliny octové, i když není kompetitivní s karbonylací methanolu. Acetaldehyd lze vyrábět oxidací butanu nebo lehké nafty, oxidací ethylenu nebo alternativně hydratací acetylenu .
Když se lehký butan nebo nafta zahřívá na vzduchu v přítomnosti různých kovových iontů, zejména manganu , kobaltu a chrómu , vytvoří se peroxid, který se následně rozloží na kyselinu octovou: 2 C 4 H 10 + 5 O 2 → 4 CH 3 COOH + 2 H 2 O Pracujeme s kombinací teploty a tlaku, aby byla reakční směs co nejteplejší při zachování butanu v kapalném stavu. 150 ° C a 55 atm jsou obvyklé podmínky. Lze také vytvořit několik vedlejších produktů, včetně butanonu , ethylacetátu , kyseliny mravenčí a kyseliny propanové . Tyto vedlejší produkty mají také tržní hodnotu a reakční podmínky lze změnit tak, aby vzniklo více z nich, pokud to má ekonomickou výhodu. Avšak oddělení kyseliny octové od jejích vedlejších produktů zvyšuje náklady na tento postup. Za podmínek a katalyzátorů podobných těm, které se používají k oxidaci butanu, může být acetaldehyd oxidován kyslíkem ve vzduchu za vzniku kyseliny octové: 2 CH 3 CHO + O 2 → 2 CH 3 COOH
Díky moderním katalyzátorům může tato reakce dosáhnout výtěžku přes 95%. Hlavními vedlejšími produkty jsou ethylacetát , kyselina mravenčí a formaldehyd . Všechny tyto sloučeniny mají nižší teplotu varu než kyselina octová a lze je snadno oddělit destilací .
Oxidace ethylenu
Acetaldehyd je možno připravit z ethylenu pomocí v procesu Wacker a potom oxiduje, jak je uvedeno výše. Nedávno komercializovala jednostupňovou transformaci ethylenu na kyselinu octovou společnost Shōwa Denkō , která v roce 1997 otevřela závod na oxidaci ethylenu v Oita v Japonsku. Proces je katalyzován kovovým katalyzátorem na bázi palladia za pomoci heteropolykyselina, jako je kyselina wolframokřemičitá. Tento proces by mohl konkurovat karbonylaci methanolu pro malé rostliny (100–250 kt / rok ) v závislosti na ceně ethylenu.
Malonic syntéza
- Malonic syntéza , za použití halogenmethanu jako substituentu (RX).
Obchod
V roce 2014 byla Francie podle francouzských zvyků čistým dovozcem kyseliny octové. Průměrná dovozní cena za tunu byla 430 EUR.
Rozličný
Kyselina octová, používaná lokálně v ORL, je součástí seznamu základních léků Světové zdravotnické organizace (seznam aktualizován v dubnu 2013).
Poznámky a odkazy
- KYSELINA octová, bezpečnostní listy Mezinárodního programu pro bezpečnost chemických látek , konzultovány 9. května 2009
- „KYSELINOU“ v nebezpečných látek databanka , přístupné 16.července 2012
- (in) David R. Lide, Příručka chemie a fyziky , CRC,16. června 2008, 89 th ed. , 2736 str. ( ISBN 142006679X a 978-1420066791 ) , s. 9-50
- (in) Yitzhak Marcus, The Properties of Solvents , sv. 4, Anglie, John Wiley & Sons Ltd,1999, 239 s. ( ISBN 0-471-98369-1 )
- vypočtená molekulová hmotnost od „ atomové hmotnosti prvků 2007 “ na www.chem.qmul.ac.uk .
- (en) W. M Haynes, CRC Příručka chemie a fyziky , Boca Raton, CRC Press / Taylor a Francis,2011, 91 th ed. , 2610 s. ( ISBN 978-143982-077-3 ) , s. 3-4
- (in) James E. Mark, Fyzikální vlastnosti příručky pro polymery , Springer,2007, 2 nd ed. , 1076 str. ( ISBN 0387690026 , číst online ) , s. 294
- (en) Şerban Moldoveanu, Příprava vzorku v chromatografii , Elsevier,2002, 930 s. ( ISBN 0444503943 ) , str. 258
- (en) Robert H. Perry a Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- Wagner, Frank S. (1978) „Kyselina octová“. In: Grayson, Martin (ed.) Kirk-Othmer Encyclopedia of Chemical Technology , 3. ročníku vydání, New York: Wiley.
- (en) „Kyselina octová“ , na NIST / WebBook , přístup 28. srpna 2009
- (in) Carl L. Yaws, Handbook of Thermodynamic Diagrams , sv. 1, Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 )
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. června 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , online prezentace ) , s. 5-89
- (in) David R. Lide, Příručka chemie a fyziky , CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205
- „ Kyselina octová “ , na www.reciprocalnet.org (přístup 12. prosince 2009 )
- Indexové číslo v tabulce 3.1 přílohy VI nařízení ES č. 1272/2008 (16. prosince 2008)
- SIGMA-ALDRICH
- „ Kyselina octová “ v databázi chemických produktů Reptox z CSST (Quebecská organizace odpovědná za bezpečnost a ochranu zdraví při práci), přístup k 24. dubnu 2009
- (in) „ Kyselina octová “ na ChemIDplus , přístup 28. srpna 2009
- „ Kyselina octová “ na adrese hazmap.nlm.nih.gov (přístup 14. listopadu 2009 )
- „kyselina octová“ , na ESIS , přístup 3. března 2010
- „ Acid acetic - Société Chimique de France “ , na www.societechimiquedefrance.fr (přístup 10. října 2020 )
- INRS, Toxikologické list , 8 s leták Ref FT 24, verze 2019
- Teplota tání je asi 16,6 ° C . Jeho teplota varu je o něco nižší než 117,9 ° C . Výrobek je hořlavý s bodem vzplanutí pod 40 ° C, zatímco teplota samovznícení se zvýší na 465 ° C .
- Khelifi, L., Ghorbel, A., Garbowski, E. a Primet, M. (1997). Příprava sol-gelu katalyzátorů Pt / Al2O3 pro katalytické spalování. Journal of Physical Chemistry , 94, 2016-2026.
- Rezgui, S., Ghorbel, A., & Gates, BC (1995). Řízení přípravy směsných oxidových katalyzátorů chrómu a hliníku procesy sol-gel . Journal of Physical Chemistry, 92, 1576-1588 | shrnutí .
- Barbara Brutsaert, „ Organické kyseliny a mastné kyseliny se středním řetězcem “, výroba prasat a drůbeže , 9. den ,2009( číst online )
- Pierre de Menten , Slovník chemie: Etymologický a historický přístup , De Boeck,2013, 395 s. ( ISBN 978-2-8041-8175-8 , číst online ) , s. 20
- Goldwhite, Harold (2003). New Haven Sect. Býk. Am. Chem. Soc. (Září 2003) .
- Martin, Geoffrey (1917). Průmyslová a výrobní chemie , část 1, organická. Londýn, Crosby Lockwood, str. 330–31 .
- Schweppe, Helmut (1979). "Identifikace barviv na starých textiliích" . J. Am. Inst. Zachování 19 (1/3), 14–23.
- Jones, RE; Templeton, DH (1958). "Krystalová struktura kyseliny octové". Acta Crystallogr. 11 (7), 484–87.
- J. Chen, CL Brooks a H. Sherega, „Přehodnocení dimerů karboxylových kyselin ve vodném roztoku“, J. Phys. Chem. B , sv. 112, strany 242-249, 2008.
- Lafon-Lafourcade, S., Lucmaret, V., & Joyeux, A. (1980). Některá pozorování tvorby kyseliny octové mléčnými bakteriemi. OENO One, 14 (3), 183-194 | shrnutí .
- Slovník organických sloučenin ( 6. vydání) , sv. 1 (1996). London: Chapman & Hall. ( ISBN 978-0-412-54090-5 )
- Yoneda, Noriyki; Kusano, Satoru; Yasui, Makoto; Pujado, Peter; Wilcher, Steve (2001). Appl. Catal. A: Gen. 221 , 253–265.
- „Zpráva o výrobě“. Chem. Eng. News (11. července 2005), 67–76.
- Suresh, Bala (2003). "Kyselina octová" . Zpráva CEH 602.5000, SRI International.
- Lancaster, Mike (2002) Zelená chemie, úvodní text , Cambridge, Royal Society of Chemistry, str. 262–266 . ( ISBN 978-0-85404-620-1 ) .
- Sano, Ken-ichi; Uchida, Hiroši; Wakabayashi, Syoichirou (1999). Katalyzátorové průzkumy z Japonska 3 , 55–60.
- „ Ukazatel dovozu / vývozu “ , na Generálním ředitelství cel. Uveďte NC8 = 29152100 (přístup 7. srpna 2015 )
- WHO Model List of Essential Medicines, 18. seznam , duben 2013
Bibliografie
- Avom, J., Mbadcam, JK, Matip, MRL, & Germain, P. (2001). Izotermická adsorpce kyseliny octové uhlíkem rostlinného původu . African Journal of Science and Technology, 2 (2).
- Brodzki, D., Denise, B., & Pannetier, G. (1977). Katalytické vlastnosti komplexů drahých kovů: karbonylace methanolu na kyselinu octovou v přítomnosti sloučenin iridia (I). Journal of Molecular Catalysis, 2 (3), 149-161.
- Pastor L (1862). Nový průmyslový proces výroby octa . Mallet-Bachelier.