Akutní myeloidní leukémie
Akutní myeloidní leukémie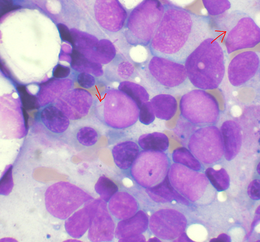 Akutní myeloidní leukémie, šipky označují Auerovy tyčinky.
Akutní myeloidní leukémie, šipky označují Auerovy tyčinky.
| Specialita | Onkologie a hematologie |
|---|
| ICD - 10 | C92.0 |
|---|---|
| CIM - 9 | 205,0 |
| ICD-O | M 9861/3 |
| OMIM | 601626 |
| NemociDB | 203 |
| MedlinePlus | 000542 |
| eMedicína | 197802 |
| eMedicína | med / 34 |
| Pletivo | D015470 |
| Příznaky | infekce, krvácení |
| Komplikace | reakce štěpu proti hostiteli (GvH) |
| Příčiny | záření, benzen |
| Diagnostický | krevní obraz, myelogram, cytogenetika |
| Léčba | chemoterapie rakoviny, cílená léčba, alogenní transplantace kostní dřeně |
| Lék | Idarubicin , mitoxantron , etoposid , cyklofosfamid , daunorubicin , hydrát thioguanin ( d ) , gemtuzumab ozogamicin , dasatinib monohydrát ( d ) , énasidénib , vénétoclax , doxorubicin , hydroxymočovina , cytarabin , everolimus , azacitidin , methotrexát , deferasirox , tretinoin , nivolumab , klofarabin , decitabin , midostaurin , busulfan , sorafenib , ruxolitinib a 6-thioguanin |
| UK pacient | Acute-myeloid-leukemia-pro |
Akutní myeloidní leukémie (AML), také známý jako myeloidní akutní leukémie je rakovina typ hematologickou malignitou ovlivnění hematopoetických buněk v kostní dřeni . Leukemické buňky, nazývané blasty , se vyznačují neschopností diferenciace na zralé buňky a nekontrolovanou proliferací . Tato dysfunkce kostní dřeně zabraňuje normální tvorbě krevních buněk a vede k různým klinickým syndromům, někdy velmi závažným ( infekce , krvácení atd.). AML se klasicky vyskytuje u dospělých nad 40 let, zejména u starších osob, i když jsou také identifikovány u dětských rakovin . Řízení zajišťují hematologové , většinou v nemocnicích . Diagnóza využívá molekulární biologii k identifikaci zejména genetických mutací , což umožňuje určit podtyp AML. Tyto diagnostické prvky jsou poté brány v úvahu pro stanovení prognózy onemocnění spolu s dalšími prvky, jako je věk nebo odpověď na léčbu. Kombinace intenzivní chemoterapie a alogenní transplantace kostní dřeně vede k úplné a trvalé remisi nebo dokonce k léčbě přibližně u 20 až 40% pacientů.
V oblasti zájmu lékařského výzkumu došlo v letech 2000 a 2010 k významnému pokroku . Příchod nových vysoce výkonných technik v buněčné hematologii, molekulární biologii a cytogenetice umožnil lepší pochopení mechanismů podílejících se na vývoji AML. Identifikace nových terapeutických cílů umožňuje nabídnout cílené terapie jako alternativu k cytotoxické chemoterapii. U konkrétního podtypu, akutní promyelocytární leukémie , tedy konvenční chemoterapie již nemá tendenci být nabízena jako první linie léčby.
Epidemiologie
Dopad
AML se může objevit v jakémkoli věku, ale většinou postihuje dospělé po 50 letech. Během desetiletí roku 2010 byl střední věk diagnózy mezi 64 a 72 lety v závislosti na zemi a roce.
| Epidemiologie AML | ||||
| Nastavení | Francie | Evropa | Spojené státy | |
|---|---|---|---|---|
| Prevalence (na 100 000 obyvatel ) | 11 | |||
| Incidence (na 100 000 obyvatel ) | 2,3 (F) / 3,1 (M) (2018) | 2 - 3 | 3,5 (F) - 5,2 (M) (2012-2016) | |
| Poměr pohlaví (M / F) | 1.3 | 1.2 | 1.5 | |
| Podíl hemopatií | 7,6% | |||
| Podíl rakoviny | 0,9% | 1,2% | ||
Dětská populace (0–19 let) je AML ovlivněna jen málo: výskyt je nízký, v roce 2017 byl výskyt 0,9%. Tito pacienti jsou více postiženi dalším podtypem leukémie: akutní lymfoblastickou leukémií, což představuje přibližně 80% případů dětské leukémie oproti 20% pro AML.
Úmrtnost
Věkově standardizovaná míra úmrtnosti spojená s AML se odhaduje na 1,3 na 100 000 lidí v roce 2017 podle Global Burden of Disease . U pediatrické populace (0 až 19 let) je nižší, 0,4 na 100 000 lidí.
Patogeneze, příčiny, rizikové faktory
Patogeneze
Tyto hematologických zhoubných nádorů , včetně AML části, mohou být obecně charakterizovány dva atributy: na zrání a proliferaci . U AML jsou tyto dvě charakteristiky pozměněny: blasty ztratily schopnost diferenciace na zralé krvinky ( polymorfy , monocyty , krevní destičky , červené krvinky ) a dělení buněk probíhá bez kontroly s nadměrnou proliferací. Toto defektní zrání a proliferace souvisí s defektem buněčného cyklu: obecně určité geny odpovědné za řízení těchto funkcí prošly mutacemi, které narušují fyziologickou kontrolu buněčného dělení. Identifikace těchto změn slouží jako základ pro diagnostiku, klasifikaci a léčbu AML.
Příčiny
Rakoviny a leukémie nemají jedinou známou příčinu, ale jejich vývoj je nicméně spojen s určitými faktory prostředí a / nebo genetickými abnormalitami. Mezinárodní agentura pro výzkum rakoviny , agenturou WHO , je zodpovědný zejména pro hodnocení a klasifikaci fyzikálních, chemických a biologických činitelů podle jejich karcinogenní účinky . Některé z nich zvláště upřednostňují výskyt leukémie, včetně AML. Celkově je jakákoli expozice, která může změnit, upravit nebo denaturovat DNA buněk, potenciálním rizikovým faktorem. K posouzení rizika, které tato expozice představuje, jsou však zapotřebí epidemiologické údaje a studie buněčných účinků.
Ionizující radiaceIonizujícího záření jsou energetické dost rozbít částice chemické vazby mezi atomy a tím měnit molekuly . Objev radioaktivity a jeho rostoucí použití v XX tého století byly rychle ukazují riziko ozáření na zdraví. Vývoj radiobiologie následně umožnil stanovit, že záření způsobuje abnormality v DNA a zvyšuje riziko vzniku rakoviny a zejména leukémie. Marie Curie a Irène Joliot-Curie tak zemřely na pravděpodobně radiačně indukovanou leukémii kvůli své práci na radioaktivitě .
Studie INWORKS, publikovaná v Lancet Hematology v roce 2015, zahrnující kohortu více než 300 000 pracovníků v oblasti jaderné energetiky ve 3 zemích, dospěla k závěru, že riziko leukémie se zvyšuje i při nízké expozici.
Chemické látkyJako poskytovatelé leukémie jsou identifikováni chemická činidla včetně léků a zejména cytotoxické chemoterapie.
Expozice benzenu je známou příčinou vývoje AML; Je tedy zařazen od roku 1979 jako skupiny 1 karcinogen u IARC (prokázáno karcinogen).
Glyfosát je klasifikován jako pravděpodobně karcinogenní pro člověka (skupina 2A), ale není nalezen ve spojení s AML s vysokou úrovní důkazů ; i když jsou údaje omezené, existuje podezření na odkaz.
Léky identifikované jako leukemogenní:
- jsou antracykliny ( doxorubicin , daunorubicin , atd. ) a spojené ( mitoxantron ) jsou léky proti rakovině je známo, že leukemogenní;
- jsou alkylační činidla ( busulfan , atd );
- antimetabolity (cytarabin);
- epidofylotoxiny: etoposid .
- Leukemogenní chemická látka
-
Benzen
-
Doxorubicin
-
Etoposid
Nástup akutní myeloidní leukémie může následovat po transformaci (nebo akutizaci ) jiného krevního onemocnění, jako je myelodysplastický syndrom nebo myeloproliferativní syndrom (chronická myeloidní leukémie atd. ). Různé vrozené onemocnění představuje rizikový faktor ( trizomie 21 , Klinefelterova syndromu , Fanconiho anémie , atd ).
Zdá se, že historie infekce některými viry nebo bakteriemi nesouvisí se zvýšeným rizikem AML.
Klinické příznaky
Když nadměrné množení výbušnin napadne kostní dřeň a / nebo jiné orgány lidského těla a naruší jejich funkci, což způsobí výskyt klinických příznaků. Klinický obraz však obecně není příliš konkrétní a diagnóza nemůže být stanovena pouze na základě symptomů.
Selhání kostní dřeně
Invaze do kostní dřeně od leukemických buněk naruší krvetvorbu, to znamená, že fyziologický proces vytváření nových krevních buněk. V dřeni se obvykle produkují tři typy buněk (nebo linií): červené krvinky ( erytrocyty ), bílé krvinky (zejména polymorfonukleární neutrofily ) a krevní destičky (trombocyty). Dysfunkce kostní dřeně se může pohybovat od cytopenie (jedna postižená buněčná linie) až po aplastickou anémii (úplný nedostatek krevních buněk ze všech tří linií). Související příznaky závisí na typu cytopenie. Cytopenie může být diagnostikována před projevy klinických příznaků nebo rutinním laboratorním vyšetřením u asymptomatického jedince.
Onemocnění červené krevní linieKvantitativní deficit červených krvinek je doložen celkovou koncentrací hemoglobinu v krvi a nazývá se anémie . Tolerance pacienta k anémii je obecně spojena s rychlostí nástupu: v případě instalace s nízkou hlučností se tělo adaptuje pomocí kompenzačních systémů; příznaky mohou chybět. Rychlý nástup bude naopak doprovázen klinickou odezvou, zejména dušností , astenií , bledostí.
Nemoc bílé čáryHlavním problémem je pokles polynukleárních neutrofilů (PNN): tyto buňky patří do přirozeného imunitního systému a tvoří první linii obrany proti infekcím, zejména bakteriálním a plísňovým . Podle velikosti deficitu budeme hovořit o neutropenii nebo agranulocytóze . Neutropenický subjekt je extrémně citlivý na infekce . Výskyt horečky se v tomto kontextu nazývá febrilní neutropenie a představuje terapeutický stav, který nejčastěji vyžaduje léčbu v nemocničním prostředí podáním antibiotika .
Můžeme hovořit o „hyperleukocytární“ leukémii (tj. S nadbytkem bílých krvinek) při pozorování neutropenie: vysoké procento leukocytů ve skutečnosti odpovídá blastům cirkulujícím v krvi se současným poklesem počtu normální polynukleární buňky.
Zapojení počtu destičekSnížení počtu krevních destiček v krvi zvyšuje riziko závažného nebo spontánního krvácení . Klinicky mohou kožní známky jako purpura , petechie nebo podlitiny odrážet neúčinnou hemostázu.
Významné poruchy srážlivosti jsou pozorovány zejména během počáteční fáze akutní promyelocytární leukémie . Spotřeba krevních destiček a koagulační faktory způsobené diseminovanou intravaskulární koagulací mohou trombocytopenie zhoršit.
Syndrom nádoru
Syndrom nádoru je spojen s šířením výbuchů mimo kostní dřeň a akumulací v orgánech. Klinicky to může vyústit:
- zvýšení objemu některých orgánů : splenomegalie , hepatomegalie ;
- bolest kloubů;
- poškození kůže (noční pocení);
- poškození sliznice včetně hypertrofie dásní (zvýšený objem dásní);
- neuromeningeální poškození při napadení centrálního nervového systému , které může být doprovázeno neurologickými příznaky.
Když je nádorová hmota (tj. Počet výbuchů) velmi velká, může začít syndrom lýzy nádoru . Souvisí to s ničením výbuchů, ať už spontánních nebo souvisejících s léčbou. Poté se intracelulární obsah uvolní do krve, což způsobí narušení koncentrací iontů v krvi (draslík, fosfát), které jsou viditelné na ionogramu. To může vést k hyperkalemii , která je škodlivá pro srdeční frekvenci, nebo ke zvýšení kyseliny močové (hyperurikemie), což může vést k poškození ledvin tvorbou krystalů urátu. Léčba syndromu lýzy má za cíl obnovit normální ionogram hydratací a podáním elektrolytů; hyperurikemii lze léčit rasburikázou , což je enzym, který štěpí kyselinu močovou.
Syndrom leukostasis je pozorována v případě masivní infiltrace orgánů podle leukemických buněk. Projevuje se vysokou koncentrací blastů v krvi (blastóza), horečkou a respiračními a / nebo neurologickými příznaky. Tento syndrom představuje terapeutickou nouzovou situaci, jejíž výsledek může být fatální v důsledku dýchacích potíží .
Diagnostický
Klinické vyšetření pacienta umožňuje především detekovat příznaky maligní hemopatie. Diagnóza je v zásadě založena na rozšířeném biologickém hodnocení zahrnujícím: krevní obraz ( CBC ), myelogram nebo biopsii kostní dřeně , imunofenotypizaci , karyotyp , cytogenetiku a genové sekvenování .
Vyšetření kostní dřeně definuje morfologický vzhled buněk a je prvním krokem při stanovení diagnózy. Diagnóza akutní leukémie je stanovena v přítomnosti více než 20% nezralých buněk, výbuchů. Zkoumání exprese různých receptorů ( DC ) pomocí imunofenotypizace umožňuje klasifikaci stadia a linie, ke které buňky patří.
Karyotyp a studium genomu umožňují identifikaci chromozomálních abnormalit (delece, inverze, translokace); 50 až 60% AML má abnormality karyotypu. Hledají se také genetické mutace . Tyto analýzy jsou rozhodující při hodnocení prognózy a možností léčby.
Před vývojem fenotypizačních a cytogenetických technik byla diagnóza AML založena hlavně na morfologii buněk a řídila se francouzsko-americko-britskou (FAB) klasifikací. Nové techniky pro studium DNA umožnily vytvořit novou klasifikaci WHO, která nahradila FAB: její kategorizace je jemnější a je založena na chromozomálních a / nebo genetických abnormalitách.
Kromě klasifikace můžeme rozlišit také 3 typy AML:
- AML de novo ;
- AML sekundární k myelodysplastickému syndromu nebo myeloproliferativnímu syndromu ;
- AML vyvolaný cytotoxickými látkami a / nebo zářením.
Klasifikace
Vzhledem k ovlivněným buňkám a zapojeným mutacím jsou akutní myeloidní leukémie nesourodou sadou, která byla předmětem kategorizace. FAB (francouzsko-americko-britský) je nejstarší a byl nahrazen klasifikací WHO zveřejněnou v roce 2008. Ačkoli je FAB zastaralý, je stále obvyklé splňovat související diagnostické pojmy (LAM0, LAM3 atd. ).
Světová zdravotnická organizaceKlasifikace WHO pro AML se v současnosti používá pro diagnostiku. Původně publikováno v roce 2008, bylo aktualizováno v roce 2016 a publikováno v Blood (referenční hematologický deník).
| Klasifikace WHO 2016 pro akutní myeloidní leukémie a související neoplazie | ||
| Příjmení | Popis | ICD-O |
|---|---|---|
| AML s opakujícími se cytogenetickými abnormalitami |
|
Násobek |
| AML s abnormalitami spojenými s myelodysplasiemi | Zahrnuje AML spojené s MDS bez výše zmíněných molekulárních abnormalit; obecně jsou spojeny s nepříznivou prognózou.
|
M 9895/3 |
| AML po léčbě | Skupina včetně leukémií vyskytujících se po chemoterapii nebo ozáření. | M 9920/3 |
| LAM, bez další indikace | Skupina včetně podtypů, které nespadají do jiných kategorií.
|
|
| Myeloidní sarkom | ||
| Proliferace myeloidů spojená s trizomií 21 |
|
M 9861/3 |
| Leukémie odvozená z plazmacytoidních dendritických buněk | Dříve známá jako NK buněčná leukémie / lymfom
Také se nazývá: Plasmacytoid Blast Dendritic Cell Neoplasm (NCDPB) |
|
| Akutní leukémie nejednoznačné linie | ||
Klasifikace FAB (francouzsko-americko-britská, 1976) je stará klasifikace, nyní opuštěná. Je založen na morfologii a množství buněk pozorovaných na myelogramu.
| FAB klasifikace AML | ||
| LAM | Popis | Podíl |
|---|---|---|
| LAM 0 | nediferencovaný | 5% případů |
| LAM 1 | myeloblastický bez rozlišení | 15% případů |
| LAM 2 | myeloblastický s diferenciací | 25% případů |
| LAM 3 | promyelocytární | 10% případů |
| LAM 4 | myelomonocytární | 20% případů |
| LAM 4Eo | myelomonocytické s eosinofilií | 5% případů |
| LAM 5 | monoblast (bez rozlišení: M5a, s rozlišením: M5b) | 10% případů |
| LAM 6 | erytroblastická nebo erytroleukémie | 5% případů |
| LAM 7 | megakaryoblastický | 5% případů |
Na rozdíl od analýzy zaměřené na studium mutovaných genů nemá tato klasifikace žádný dopad, pokud jde o prognózu nebo léčbu, která má být provedena.
Léčba
Léčebná léčba akutní myeloidní leukémie je chemoterapie intenzivně asociovaná s alogenními hematopoetickými kmenovými buňkami (s výjimkou promyelocytické akutní leukémie (" LA ")). Řízení závisí na mnoha prvcích souvisejících jak s pacientem, tak s leukémií. Věk, celkový stav , komorbidity a přání pacienta jsou obzvláště důležitými faktory. Možnosti léčby v průběhu léčby určují typ akutní leukémie, různé detekované mutace a klinické odpovědi na předchozí léčbu. Rozhodnutí o léčbě se přijímají na konci multidisciplinárních konzultačních setkání (RCP).
Klasická léčba je sledem chemoterapeutických kurzů v několika fázích: indukce, konsolidace, pak, pokud je pacient vhodný, intenzifikace terapie alogenní transplantací kostní dřeně. Záření není standardní léčba AML, protože neexistuje jediný umístění onemocnění jako solidní nádor. Používá se však k prevenci nebo léčbě neuro-meningeálních onemocnění, to znamená, když se leukemické buňky nacházejí v centrálním nervovém systému ( mozek , mícha ). Další zvláštní situace mohou vyžadovat použití radioterapie (lokalizace varlat , myeloidní sarkom ).
Léčba akutní promyelocytární leukémie (APL) je zvláštním případem: role klasické cytotoxické chemoterapie je méně významná, protože vývoj spojení kyselé all-trans retinové kyseliny ( ATRA ) a oxidu arsenitého pro dosažení míry remise vyšší než 90% .
Vedení leukémie a rakoviny je spojena s mnoha zásadní podpůrnou léčbou : prevenci a řízení těchto nežádoucích účinků chemoterapie, podpora transfúze ke zmírnění cytopenie , nutriční monitorování , screening depresivních symptomů , léčby bolesti a start-up místo. Vhodnou paliativní péče Pokud je potřeba.
Indukce
Indukce si klade za cíl vyvolat úplnou remisi ( CR ) klinicky a biologicky chemoterapií. Obvykle je předepsán protokol 3 + 7 založený na cytarabinu a antracyklinech ( daunorubicin nebo idarubicin ); tato léčba způsobí, že pacient trpí hlubokou aplastickou anémií trvající tři až čtyři týdny, během níž musí být tato anémie pečlivě sledována ve specializované hematologické službě, aby se zabránilo riziku krvácení a infekce.
Jako alternativu ke klasické indukci lze použít i jiné molekuly, například decitabin .
Konsolidace
Další léčba závisí do značné míry na prognóze AML, reakci na indukční chemoterapii (dosažení úplné remise), pacientovi (věk, komorbidity atd. ) A na jejich přání. Konsolidační léčba má za cíl eliminovat zbytkové leukemické buňky a zabránit tak jejich opakování. Alogenní transplantace kostní dřeně je preferenční léčba, která umožňuje dosáhnout nejvyšší trvalé míry remise, ale za cenu poměrně náročné léčby.
Pokud je alogenní transplantace odmítnuta nebo nevhodná, lze pokračovat standardní chemoterapií, například vysokými dávkami cytarabinu , azacitidinu nebo klofarabinu . Další možnosti léčby jsou cílené terapie. Autologní kostní dřeně je velmi vzácný.
Aloštěp
Alogenní transplantace kostní dřeně je jedinou kurativní léčbou AML. Cílem je zničit patologickou kostní dřeň pacienta a poté z ní rekonstituovat novou kostní dřeň pomocí hematopoetických kmenových buněk shromážděných od zdravého jedince . Terapeutický správa je složitá a vyžaduje vhodnou hematologie nabízí pokoje chráněné a další nemocniční zařízení ( buněčná terapie jednotky , chemoterapie příprava jednotky , atd. ).
Vhodnost pro transplantaci se posuzuje kolektivně a rozhoduje se po dohodě s pacientem . Léčba vyžadovaná pro transplantaci má určitou toxicitu a vyvolává dlouhé období aplázie a imunosuprese s vysokým rizikem komplikací a infekcí. Alogenní transplantace je proto obecně vyhrazena „mladým“ subjektům (do 60 let) a / nebo ve velmi dobrém celkovém stavu, kteří budou schopni tuto léčbu podporovat a mít z transplantace dlouhodobý prospěch.
Můžeme zhruba rozlišit 3 fáze. Za prvé, klimatizace pacient se skládá z celotělového ozařování , podávání imunosupresiv a intenzivní chemoterapie. Jejím cílem je vymýtit leukemické buňky a vyvolat významnou imunosupresi, která umožní co nejvíce snížit odmítnutí transplantátu . Tyto heterologní kmenové buňky se pak znovu vstřikuje. Pokračování léčby spočívá ve zvládnutí prodloužené aplastické anémie vyvolané úpravou a možných komplikací a nežádoucích účinků. Ve střednědobém horizontu hematolog sleduje zdraví štěpu a sleduje účinné vymizení leukemických buněk.
Na imunologické úrovni může zavedení do těla buněk, které jsou pacientovi cizí (nazývané „ jiné než já “), vyvolat imunitní reakci namířenou proti pacientovým buňkám nebo proti leukémii: tyto účinky se nazývají „ štěp vs. hostitel “(GvH) a„ štěp vs. leukémie “(GvL). První je více či méně závažný nežádoucí účinek, který se může objevit na různých místech (zažívací, kožní atd. ) A odpovídá napadení transplantovaných buněk na orgány hostitele; může to být akutní nebo chronické. Účinek GvL je naopak prospěšný, protože imunitní buňky štěpu budou útočit na leukemické buňky, a tak budou mít protirakovinový účinek. Kromě GvH zahrnují alogenní transplantační komplikace: infekce související s imunosupresí a aplázií, zvýšené riziko sekundárních rakovin, dlouhotrvající cytopenie vyžadující transfuze, venookluzivní onemocnění jater a další nežádoucí účinky chemoterapie.
Pro křehké nebo starší pacienty, kteří nemohou odolat standardnímu aloštěpu, existují tzv. Protokoly „snížené intenzity“, kde krok úpravy (chemoterapie a radioterapie) zahrnuje snížené dávky: toto řešení je kompromisem pro zachování výhody alogenního transplantace při zohlednit nižší toleranci pacienta.
V roce 2016 bylo ve Francii provedeno přes 700 aloštěpů k léčbě AML. V roce 201 identifikovala Evropská společnost pro transplantaci krve a kostní dřeně (EBMT) pro indikaci 6943 aloštěpů a 293 autotransplantátů s akutní myeloidní leukémií.
Cílené terapie
Během diagnostiky umožňuje sekvenování genomu leukemických buněk identifikovat přítomné mutace. Některé z nich se podílejí na proliferaci a selhání zrání blastů: mohou například vést k syntéze abnormálního proteinu, který by trvale aktivoval buněčný cyklus , což by vedlo k nekontrolovanému dělení buněk. Zastavení škodlivého působení mutovaných genů nebo pozměněných proteinů proto představuje potenciální terapeutický cíl: takto byly v onkologii vyvinuty určité léky působící specificky na tyto abnormality . Jsou seskupeny pod názvem cílené terapie na rozdíl od klasické cytotoxické chemoterapie; toto označení zahrnuje i další léky s různými mechanismy účinku, například monoklonální protilátky cílené na receptory na povrchu buněk ( diferenciační klastry ).
V roce 2016 odhad literatury odhadoval, že 50% až 80% případů AML má škodlivé mutace. Z nejčastěji dotčených genů lze zmínit FLT3 nebo NPM1 (mutace mohou být doprovodné). V rámci péče o pacienta znalost mutovaných genů umožňuje nejen kategorizovat leukémii, stanovit prognózu, ale také předpovědět, jaké cílené terapie mohou být u tohoto pacienta předepsány. Ačkoli dosud neexistuje molekula, která by dokázala čelit každému genu, několik z nich bylo vyvinuto během desetiletí roku 2010 a někdy dostalo souhlas zdravotnických úřadů. Bylo například zjištěno, že mutace v isocitrát dehydrogenáze (IDH), což je enzym podílející se na metabolismu buněčné energie , mohou podporovat proliferaci leukemických buněk. Proto byly vyvinuty inhibitory HDI: enasidenib (cílení na IDH2 ) a ivosidenib (cílení na IDH1 ). Mohou být předepsány různé jiné cílené terapie nebo jsou předmětem klinického výzkumu, jako je glasdegib , venetoklax atd.
| cílová | Typ | Příklad cílené terapie |
|---|---|---|
| FLT3 | Protein | Midostaurin , gilteritinib (en) quizartinib (en) |
| HDI | Protein | Ivosidenib (IDH1), enasidenib (IDH2) |
| Bcl-2 | Protein | Venetoclax |
| CD33 | Membránový receptor | Gemtuzumab ozogamicin |
Použití androgenních hormonů - které nejsou striktně řečeno cílenou terapií, ale spadají pod hormonální terapii - bylo také studováno v klinickém výzkumu. V Zejména norethandrolon Zdá se, že zlepšení přežití a remise u starších pacientů.
A konečně, některé chemoterapie, i když mají klasický mechanismus interferující se syntézou DNA, mohou mít také další cílené vlastnosti. Azacitidin má, například, hypomethylating akce: to může vyvolat stažení methyl chemických skupin (-CH 3 )řetězce DNA, a tak umožňují re-expresi určitých genů kontrolujících buněčné dělení buňky.
Jiné situace
Rekurentní nebo refrakterní formy AML jsou léčeny specifickými protokoly, obvykle chemoterapií (záchranná nebo život zachraňující léčba).
Pokud jde o imunoterapii , je gemtuzumab ozogamicin jedinou monoklonální protilátkou schválenou pro léčbu AML. Immunocheckpoint inhibitory (jako je například ipilimumabu , The nivolumab ) nebo T-buněk SAR (lymfocytů geneticky modifikovaných) nejsou, v roce 2020, je uvedeno v léčení AML, ale jsou předmětem studie pro klinický výzkum.
Přežití
Prognóza je obvykle vyjádřena v celkovém přežití po 5 letech, to znamená, že tím, že podíl pacientů stále naživu 5 let po diagnóze, s přihlédnutím ke všem příčinám úmrtí v kombinaci (ať už v souvislosti s LAM, jejích důsledků, na druhou nesouvisející událost, například dopravní nehoda). V onkologii lze k odhadu prognózy v průběhu léčby nebo v klinických studiích použít jiné prostředky : můžeme hovořit o přežití bez relapsu, přežití bez progrese nebo odpovědi na léčbu (úplná odpověď, částečná atd.).
U dospělých se přežití po 5 letech odhaduje na přibližně 25% a klesá s věkem: je to 40% před 65 lety a poté 5% po. V pediatrii se pravděpodobnost celkového pětiletého přežití zvýšila z 50% v 90. letech na přibližně 60-70% v roce 2010 (u akutní lymfoblastické leukémie dosáhla 90% v roce 2010). Šance na přežití malých dětí jsou opět o něco vyšší než u dospívajících.
Tyto údaje neplatí pro akutní promyelocytární leukémii (ex-AML 3). Nové léčby (kombinace ATRA / ATO ), které byly dříve spojeny s pochmurnou prognózou, od roku 2000 umožnily dosáhnout dlouhodobé remise u 90% pacientů.
Dějiny
První popis případu leukémie v lékařské literatuře pochází z roku 1827. Alfred Velpeau popsal případ 63letého květinářství trpícího nemocí s horečkou, únavou, ledvinovými kameny a velkými zvětšenými játry a slezinou . Zjistil, že krev pacienta měla ovesnou konzistenci, a předpokládal, že tento vzhled může být způsoben bílými částicemi. V roce 1845 popsal patolog JH Bennett sérii případů pacientů, kteří zemřeli s rozšířenou slezinou a „změnami v barvě jejich konzistence krve“; potom k popisu tohoto stavu používá výraz „leukocytémie“.
Slovo „leukémie“ poprvé použil německý patolog Rudolf Virchow v roce 1856. Pomocí mikroskopu popsal přebytek bílých krvinek u jedinců vykazujících příznaky popsané Velpeauem a Benettem. Virchow neznal původ této anomálie, pojmenoval ji čistě popisným termínem leukémie (v řečtině bílá krev ).
Poznámky a odkazy
Poznámky
(fr) Tento článek je částečně nebo zcela převzat z článku anglické Wikipedie s názvem „ Akutní myeloidní leukémie “ ( viz seznam autorů ) .- Anglicismus od akutní , „akutní“, což znamená přechod z chronického onemocnění do akutního stadia; přidružené sloveso je „akutizér“.
Reference
- Terminologique velkého slovníku , Office québécois de la langue française, „ akutní leukémie “ ,2019(zpřístupněno 28. prosince 2019 )
- MSD , Ashkan Emadi, Jennie York Law, „ Acute Myeloid Leukemia (AML) - Hematology and Oncology - Professional Edition of the MSD Manual “ ,prosince 2018(zpřístupněno 29. prosince 2019 )
- (en) National Cancer Institute , „ Adult Acute Myeloid Leukemia Treatment (PDQ®) -Health Professional Version “ ,8. února 2019(zpřístupněno 28. prosince 2019 )
- Institut National Du Cancer, „ Shrnutí - Národní odhady výskytu a úmrtnosti na rakovinu v kontinentální Francii v letech 1990 až 2018 - Ref: SYNINCNAT2019 “ , na www.e-cancer.fr ,července 2019(zpřístupněno 8. září 2019 )
- INSERM, „ Orphanet: Akutní myeloidní leukémie “ , na orpha.net ,červen 2014(zpřístupněno 8. září 2019 )
- (in) D. Weber, E. Fromm, S. Erhardt, pan Lübbert W. Fiedler, T. Kindler, J. Krauter, P. Brossart, A. Kündgen, HR Salih J. Westermann, G. Wulf, B Hertenstein, M. Wattad, K. Götze, D. Kraemer, T. Heinicke, M. Girschikofsky, HG Derigs, HA Horst, C. Rudolph, M. Heuser, G. Göhring, V. Teleanu, L. Bullinger, F Thol, VI Gaidzik, P. Paschka, K. Döhner, A. Ganser, Hartmut Döhner, RF Schlenk, německo-rakouská studijní skupina AML (AMLSG) Gabriele Nagel , „ Epidemiologická, genetická a klinická charakterizace podle věku nově diagnostikované akutní myeloidní leukémie na základě akademické populační registrační studie (AMLSG BiO) “ , Annals of Hematology , sv. 96, N O 1231. října 2017, str. 1993 ( DOI 10.1007 / s00277-017-3150-3 , / pmc / articles / PMC5691091 /? Zpráva = abstrakt, číst online )
- SEER, „ Acute Myeloid Leukemia - Cancer Stat Facts, “ na adrese seer.cancer.gov (přístup k 8. září 2019 )
- Visser O a kol., „ Incidence, přežití a prevalence myeloidních malignit v Evropě. » , Na www.ncbi.nlm.nih.gov ,listopadu 2012(zpřístupněno 8. září 2019 )
- Globální studie zátěže nemocí, „ Globální zátěž rakoviny dětí a dospívajících v roce 2017: analýza studie Global Burden of Disease Study 2017 “ , na www.thelancet.com ,29. července 2019(zpřístupněno 14. září 2019 )
- Smith MA, Ries LA, Gurney JG, et al., „ Výskyt rakoviny a přežití u dětí a dospívajících: United States SEER Program 1975-1995 “ , na seer.cancer.gov ,31. ledna 2019(zpřístupněno 15. září 2019 )
- Globální studie zátěže nemocí, „ Globální, regionální a národní úmrtnost specifická podle věku a pohlaví u 282 příčin úmrtí ve 195 zemích a teritoriích, 1980–2017: systematická analýza studie Global Burden of Disease Study 2017 “ , na www .thelancet.com ,10. listopadu 2018(zpřístupněno 14. září 2019 )
- VJ Cogliano , R. Baan , K. Straif , Y. Grosse , B. Lauby-Secretan , F. El Ghissassi , V. Bouvard , L. Benbrahim-Tallaa , N. Guha , C. Freeman , L. Galichet a CP Wild , „ Preventable Exposures Associated with Human Cancer “, JNCI Journal of the National Cancer Institute , sv. 103, n o 24,2011, str. 1827–1839 ( ISSN 0027-8874 , DOI 10.1093 / jnci / djr483 )
- " Klasifikace IARC podle stránek s rakovinou | Rakovina a životní prostředí “ (přístup 24. listopadu 2019 )
- Musée Curie , „ Životopis Marie Curie “ (přístup k 24. listopadu 2019 )
- Musée Curie , „ Biografie Irene a Frédéric Joliot-Curie “ (přístup k 24. listopadu 2019 )
- Klervi Leuraud , David B Richardson , Elisabeth Cardis , Robert D Daniels , Michael Gillies , Jacqueline O'Hagan , Ghassan B Hamra , Richard Haylock , Dominique Laurier , Monika Moissonnier , Mary K Schubauer-Berigan , Isabelle Thierry-Chef a Ausrele Kesminiene „ Ionizující záření a riziko úmrtí na leukémii a lymfomy u pracovníků sledovaných zářením (INWORKS): mezinárodní kohortní studie “, The Lancet Hematology , sv. 2, n O 7,2015, e276 - e281 ( ISSN 2352-3026 , DOI 10.1016 / S2352-3026 (15) 00094-0 )
- INRS, „ benzen (FT 49). Patologie - Toxikologie - Toxikologický list - INRS ” ,2011(zpřístupněno 8. září 2019 )
- Loomis A., „ Karcinogenita benzenu “ , na www.thelancet.com ,26. října 2017(zpřístupněno 8. září 2019 )
- IARC, „ Benzen - monografie IARC o hodnocení karcinogenních rizik pro člověka “ , na iarc.fr ,2018(zpřístupněno 8. září 2019 )
- Kathryn Z Guyton , Dana Loomis , Yann Grosse , Fátiha El Ghissassi Lamia Benbrahim-Tallaa , Neela Guha , Chiara Scoccianti Heidi Mattock a Kurt Straif , " karcinogenitu tetrachlorvinfos, parathion, malathion, diazinon, a glyfosát ," The Lancet Oncology , sv . 16, n o 5,2015, str. 490–491 ( ISSN 1470-2045 , DOI 10.1016 / S1470-2045 (15) 70134-8 )
- Gabriella Andreotti , Stella Koutros , Jonathan N Hofmann , Dale P Sandler , Jay H Lubin , Charles F Lynch , Catherine C Lerro , Anneclaire J De Roos , Christine G Parks , Michael C Alavanja , Debra T Silverman a Laura E Beane Freeman , “ Užívání glyfosátu a výskyt rakoviny ve studii zemědělského zdraví “, JNCI: Journal of the National Cancer Institute , sv. 110, n o 5,2018, str. 509–516 ( ISSN 0027-8874 , DOI 10.1093 / jnci / djx233 )
- Centrum Léon-Bérard , IARC, „ Klasifikace IARC podle rakovinných míst | Rakovina a životní prostředí “ ,29. listopadu 2019(zpřístupněno 29. prosince 2019 )
- Center National Hospitalier d'Information sur le Médicament (CNHIM), „ Adverse response sheet “ , na theriaque.org (přístup 15. září 2019 )
- (in) Sachiko Ezoe , „ Secondary Leukemia Associated with the Anti-Cancer Agent, Etoposide, a Topoisomerase II Inhibitor “ , International Journal of Environmental Research and Public Health , sv. 9, n o 7,30. listopadu 12, str. 2444 ( DOI 10.3390 / ijerph9072444 , / pmc / articles / PMC3407914 /? Report = abstrakt, číst online )
- Barbara Deschler a Michael Lübbert , „ Akutní myeloidní leukémie: epidemiologie a etiologie “, Cancer , sv. 107, n o 9,2006, str. 2099–2107 ( ISSN 0008-543X , DOI 10.1002 / cncr.22233 )
- LLSCanada, " www.llscanada.org " (k dispozici na 1. st březen 2020 )
- Hoffman, Ronald a kol. (2005). Hematologie: Základní principy a praxe (4. vyd.). St. Louis, Mo.: Elsevier Churchill Livingstone. p. 1074–75
- Akutní myeloidní leukémie , N Engl J Med 1999; 341.
- Botton 2017 , s. 500-501
- Schmidt, Cornu, Angellilo-Scherrer a kol. , „ Fyziopatologických báze obecně hematologie: a pomocné paměti pro hematologii “ [PDF] , na www.2bib.ch ,2015(přístup 10. prosince 2019 ) , s. 149
- Ifrah 2018 , s. 68
- Francouzská hematologická společnost, „ Akutní leukémie, 3 - biologické příznaky a diagnóza “ [html] ,1 st 04. 2010(zpřístupněno 15. prosince 2019 )
- Botton 2017 , s. 500
- (in) James W. Vardiman , „ Revize klasifikace myeloidních novotvarů a akutní leukémie Světové zdravotnické organizace z roku 2016 “ , Blood , American Society of Hematology, sv. 127, n o 20,19. května 2016, str. 2391-2405 ( ISSN 1528-0020 , DOI 10.1182 / krev-2016-03-643544 , abstrakt , číst online )
- (in) Karen Seiter, Emmanuel C. Besa et al. , „ Akutní myeloidní leukémie Staging - FAB a WHO Klasifikace pro akutní myeloidní leukémie “ , na emedicine.medscape.com ,30. prosince 2015(zpřístupněno 23. dubna 2016 ) .
- „Aktualizace akutní myeloidní leukémie, září 2016, str. 3/16“
- " Vše o darování | Don de Moelle Osseuse ” , na www.dondemoelleosseuse.fr (přístup 11. listopadu 2018 )
- Hartmut Döhner , Elihu Estey , David Grimwade , Sergio Amadori , Frederick R. Appelbaum , Thomas Büchner , Hervé Dombret , Benjamin L. Ebert , Pierre Fenaux , Richard A. Larson , Ross L. Levine , Francesco Lo-Coco , Tomoki Naoe , Dietger Niederwieser , Gert J. Ossenkoppele , Miguel Sanz , Jorge Sierra , Martin S. Tallman , Hwei-Fang Tien , Andrew H. Wei , Bob Löwenberg a Clara D. Bloomfield , „ Diagnostika a řízení AML u dospělých: Doporučení ELN 2017 od mezinárodního panelu odborníků “, Blood , sv. 129, n O 4,2017, str. 424-447 ( ISSN 0006-4971 , DOI 10.1182 / krev-2016-08-733196 )
- Martin S. Tallman , Eunice S. Wang , Jessica K. Altman , Frederick R. Appelbaum , Vijaya Raj Bhatt , Dale Bixby , Steven E. Coutre , Marcos De Lima , Amir T. Fathi , Melanie Fiorella , James M. Foran , Aric C. Hall , Meagan Jacoby , Jeffrey Lancet , Thomas W. LeBlanc , Gabriel Mannis , Guido Marcucci , Michael G. Martin , Alice Mims , Margaret R. O'Donnell , Rebecca Olin , Deniz Peker , Alexander Perl , Daniel A. Pollyea , Keith Pratz , Thomas Prebet , Farhad Ravandi , Paul J. Shami , Richard M. Stone , Stephen A. Strickland , Matthew Wieduwilt , Kristina M. Gregory , Lydia Hammond a Ndiya Ogba , „ Akutní myeloidní leukémie, verze 3.2019 , NCCN Clinical Practice Guidelines in Oncology ”, Journal of the National Comprehensive Cancer Network , sv. 17, n O 6,2019, str. 721–749 ( ISSN 1540-1405 , DOI 10.6004 / jnccn.2019.0028 )
- (in) Cancer Research UK, „ Radioterapie mozku - akutní myeloidní leukémie “ ,16. července 2019(zpřístupněno 29. prosince 2019 )
- (en + es) American Cancer Society, „ Radiační terapie pro akutní myeloidní leukémii (AML) “ ,21. srpna 2018(zpřístupněno 29. prosince 2019 )
- Miguel A. Sanz , Pierre Fenaux , Martin S. Tallman , Elihu H. Estey , Bob Löwenberg , Tomoki Naoe , Eva Lengfelder , Hartmut Döhner , Alan K. Burnett , Sai-Juan Chen , Vikram Mathews , Harry Iland , Eduardo Rego , Hagop Kantarjian , Lionel ADES , Giuseppe Avvisati , Pau Montesinos , Uwe Platzbecker , Farhad Ravandi , Nigel H. Russell a Francesco Lo-Coco , „ řízení akutní promyelocytární leukémie: aktualizováno doporučení expertního panelu Evropské LeukemiaNet “, Blood , vol . 133, n o 15,2019, str. 1630–1643 ( ISSN 0006-4971 , DOI 10.1182 / krev-2019-01-894980 )
- Gustave Roussy , „ Podpůrná péče - Gustave Roussy “ (přístup 18. března 2020 )
- Institut Curie , „ Pomáháme vám během léčby Institut Curie “ (přístup 18. března 2020 )
- (in) . Redakční rada pro léčbu PDQ dospělých, „ Léčba akutní myeloidní leukémie dospělých (PDQ®) - souhrny informací o rakovině PDQ - knihovna NCBI “ [html] , Bethesda (MD): National Cancer Institute (USA)8. února 2019(zpřístupněno 17. prosince 2019 )
- Evropská agentura pro léčivé přípravky , „ Dacogen “ ,13. května 2019(zpřístupněno 3. ledna 2020 )
- Botton 2017 , s. 504
- Agentura pro biomedicínu, „ Národní transplantační aktivita CSH (2016) “ [PDF] , na www.agence-biomedecine.fr , 2017(zpřístupněno 7. ledna 2020 )
- Carreras 2019 , s. 27
- EMA , „ Bulsilvex (busulfan) - souhrn údajů o přípravku “ [PDF] ,31. srpna 2017(zpřístupněno 23. června 2020 )
- Canadian Cancer Society, „ Transplantace kmenových buněk pro akutní myeloidní leukémii “ (přístup 23. června 2020 )
- Ifrah 2018 , s. 77
- „ Hematologie. Onko-hematologie - prezentace - EM konzulát » ,5. prosince 11(zpřístupněno 7. ledna 2020 )
- (in) Cancer Research UK, „ Total body radiotherapy (TBI) Acute myeloid leukemia “ ,16. července 2019(zpřístupněno 29. prosince 2019 )
- The Leukemia & Lymphoma Society of Canada, „ Stem Cell Allogeneic Transplant “ (přístup k 7. lednu 2020 )
- Kanadská společnost pro leukémii a lymfomy, „ Transplantace alogenních kmenových buněk se sníženou intenzitou “ (přístup 23. června 2020 )
- (en) Evropská společnost pro transplantace krve a dřeně , „ Výroční zpráva 2019 “ [2019]2019(zpřístupněno 23. června 2020 ) ,s. 68
- Jeanette Prada-Arismendy , Johanna C. Arroyave a Sarah Röthlisberger , „ Molekulární biomarkery u akutní myeloidní leukémie “, Blood Reviews , sv. 31, n o 1,2017, str. 63–76 ( ISSN 0268-960X , DOI 10.1016 / j.blre.2016.08.005 )
- (in) American Cancer Society, „ What's New in Acute Myeloid Leukemia (AML) Research? " ,24. června 2019(zpřístupněno 23. června 2020 )
- Elihu Estey , Judith E. Karp , Ashkan Emadi , Megan Othus a Robert Peter Gale , „ Nedávné schválení léků pro nově diagnostikovanou akutní myeloidní leukémii: dary nebo trojský kůň? », Leukemia , roč. 34, n o 3,2020, str. 671–681 ( ISSN 0887-6924 , DOI 10.1038 / s41375-019-0704-5 )
- (in) " isocitrátdehydrogenáza mutace v myeloidní malignit " (Review " leukémie " publikoval on-line 11.11.2016), Nature (časopis) , n o 31,2017, str. 272–281 ( DOI 10.1038 / leu.2016.275 , číst online )
- „Ash, Clinicak News, 21. října 2016, klinické výsledky AG-221 slibují„ revoluční “přístup v AML“
- Starr P, „ Midostaurin, první cílená terapie ke zlepšení přežití v AML: Potenciálně se měnící praxe “, Am Health Drug Benefits , sv. 9, n o vydání vydání,února 2016, str. 1–21 ( PMID 27014400 , PMCID 4782225 )
- Alexander E. Perl , Giovanni Martinelli , Jorge E. Cortes , Andreas Neubauer , Ellin Berman , Stefania Paolini , Pau Montesinos , Maria R. Baer , Richard A. Larson , Celalettin Ustun , Francesco Fabbiano , Harry P. Erba , Antonio Di Stasi Robert Stuart , Rebecca Olin , Margaret Kasner , Fabio Ciceri , Wen-Chien Chou , Nikolai Podoltsev Christian Recher , Hisayuki Yokoyama , Naoko Hosono , Sung-Soo Yoon , I-Hwan Lee , Timothy Pardee , T. Amir Fathi , Chaofeng Liu , Nahla Hasabou , Xuan Liu , Erkut Bahceci a Mark J. Levis , „ Gilteritinib nebo chemoterapie pro relabující nebo refrakterní FLT3-mutovanou AML “, New England Journal of Medicine , sv. 381, n o 18,2019, str. 1728–1740 ( ISSN 0028-4793 , DOI 10.1056 / NEJMoa1902688 )
- Arnaud Pigneux , Marie C. bene , Philippe Guardiola , Christian Recherche , Jean-Francois Hamel , Mathieu Sauvezie , Jean-Luc Harousseau Olivier Tournilhac , Francis Witz , Christian Berthou , Martine Escoffre-Barbe , Denis Guyotat , Nathalie Fegueux Chantal Himberlin , Mathilde Hunault , Martine Delain , Bruno Lioure , Eric Jourdan , Frederic Bauduer , Francois Dreyfus , Jean-Yves Cahn , Jean-Jacques Sotto a Norbert Ifrah , „ Přídavek androgenů zlepšuje přežití u starších pacientů s akutní myeloidní leukémií: studie GOELAMS “ , Journal of Clinical Oncology , sv. 35, n O 4,2017, str. 387–393 ( ISSN 0732-183X , DOI 10.1200 / JCO.2016.67.6213 )
- Evropská agentura pro léčivé přípravky , „ VIDAZA - Souhrn údajů o přípravku “ [PDF] , na www.ema.europa.eu ,9. července 2019(zpřístupněno 25. června 2020 )
- Evropská agentura pro léčivé přípravky , „ www.ema.europa.eu “ [PDF] ,25. října 2019(zpřístupněno 18. března 2020 )
- Ceylad, „ Celyad uvádí první úplnou odpověď u pacienta s refrakterní a relabující AML ve studii THINK “ , na webu ,3. října 2017(zpřístupněno 18. března 2020 )
- Yuxin Liu , Jan Philipp Bewersdorf , Maximilian Stahl a Amer M. Zeidan , „ Imunoterapie u akutní myeloidní leukémie a myelodysplastických syndromů: úsvit nové éry? ”, Blood Reviews , roč. 34,2019, str. 67–83 ( ISSN 0268-960X , DOI 10.1016 / j.blre.2018.12.001 )
- (in) American Society of Clinical Oncology , „ Leukemia - Acute Myeloid - AML: Statistics | Cancer.Net ” , na www.cancer.net ,ledna 2020(zpřístupněno 27. června 2020 )
- (en) National Cancer Institute , „ Adult Acute Myeloid Leukemia Treatment (PDQ®) -Health Professional Version “ na www.cancer.gov ,22. ledna 2020(zpřístupněno 27. června 2020 )
- (in) Cancer Research UK , „ Přežití | Akutní myeloidní leukémie | Cancer Research UK ” , na www.cancerresearchuk.org ,19. července 2019(zpřístupněno 27. června 2020 )
- Mareike Rasche , Martin Zimmermann , Lisa Borschel , Jean-Pierre Bourquin , Michael Dworzak , Thomas Klingebiel , Thomas Lehrnbecher , Ursula Creutzig , Jan-Henning Klusmann a Dirk Reinhardt : „ Úspěchy a výzvy v léčbě dětské akutní myeloidní leukémie: retrospektiva analýza studií AML-BFM od roku 1987 do roku 2012 “, Leukemia , sv. 32, n o 10,2018, str. 2167–2177 ( ISSN 0887-6924 , DOI 10.1038 / s41375-018-0071-7 )
- ARC Foundation, „ Co je to dětská leukémie?“ | ARC Foundation for Cancer Research “ , na webu ,14. února 2020(zpřístupněno 18. března 2020 )
- Americká rakovinová společnost , „ Míra odpovědi na léčbu akutní myeloidní leukémie (AML), “ na www.cancer.org ,21. srpna 2018(zpřístupněno 27. června 2020 )
- Hoffman a kol. 2005, s. 1071.
- Bennett JH, „ Dva případy hypertrofie sleziny a jater, při nichž došlo k smrti z hnisání krve “, Edinburgh Med Surg J , sv. 64,1845, str. 413
- (de) R Virchow , Gesammelte Abhandlungen zur Wissenschaftlichen Medizin , Frankfurt, Meidinger,1856( číst online ) , „Die Leukämie“ , 190
Bibliografie
![]() : dokument použitý jako zdroj pro tento článek.
: dokument použitý jako zdroj pro tento článek.
-
Norbert Ifrah ( ředitel a koordinátor), Marc Maynadié ( ředitel a koordinátor) a kol. Francouzská společnost pro hematologii, hematologie , Issy-les-Moulineaux, Elsevier Masson, kol. "Úložiště vysokých škol",Květen 2018, 3 e ed. , 400 s. ( ISBN 978-2-294-75108-0 a 9782294752636 , EAN 9782294752636 , oznámení BNF n o FRBNF45533912 ).

-
R. Costello, G. Venton, J. Colle, V. Ivanov, C. Mercier, L. Delassus a V. Baccini (článek 13-018-G-50), Akutní myeloidní leukémie u dospělých , Elsevier Masson , kol. "EMC / Hematologie",2018, 13 str. ( ISBN 978-2-84299-505-8 , ISSN 1155-1984 , OCLC 726481102 , DOI 10.1016 / S1155-1984 (18) 83321-0 , číst online [html] ). .

-
Stéphane Vignot ( vyd. A editor), Jean-Charles Soria ( vyd. ) A Stéphane de Botton , Gustave Roussy & Université Paris Sud XI, kurz protinádorové chemoterapie a léčby rakoviny , Paříž,ledna 2018, 32 th ed. , 534 s. ( ISBN 978-2-9555469-9-4 ) , kap. 83 („Akutní myeloidní leukémie“).

-
(en) Enric Carreras , Carlo Dufour , Mohamad Mohty a Nicolaus Kröger , Evropská společnost pro transplantaci kostní dřeně, Příručka EBMT: Transplantace hematopoetických kmenových buněk a buněčné terapie , Cham, Švýcarsko, Springer,2019, 688 s. ( ISBN 978-3-030-02277-8 (nesprávně upraveno) a 978-3-030-02278-5 , DOI 10.1007 / 978-3-030-02278-5 , číst online [PDF] ).

Podívejte se také
Související články
externí odkazy
Široká veřejnost- Orphanet
- Průvodce pro pacienty vydaný Evropskou společností pro lékařskou onkologii (ESMO)
- Francouzská společnost pro hematologii
- rakovina. být
- rakovina.ca
- Nadace ARC
- Laurette Fugain , sdružení odhodlané bojovat proti leukémii
- (en + es) National Cancer Institute
- Hématocell.fr (hematologická laboratoř Fakultní nemocnice v Angers)
- (en) European LeukemiaNet
- (en + es) National Cancer Institute